
【題目】甲烷和乙炔的混合氣體20 mL,完全燃燒需45 mL氧氣(同溫同壓下),則此混合氣體中甲烷和乙炔的體積比是( )
A.1∶1B.2∶1C.3∶1D.4∶1
科目:高中化學 來源: 題型:
【題目】合金貯氫材料具有優異的吸收氫性能,在配合氫能的開發中起到重要作用。
(1)一定溫度下,某貯氫合金(M)的貯氫過程如圖所示,縱軸為平衡時氫氣的壓強(P),橫軸表示固相中氫原子與金屬原子的個數比(H/M)。

在OA段,氫溶解于M中形成固溶體MHx,隨著氫氣壓強的增大,H/M逐慚增大;在AB段,MHx與氫氣發生氫化反應生成氫化物MHy,氫化反應方程式為:zMHx(s)+H2(g)==ZMHy(s) △H(Ⅰ);在B點,氫化反應結束,進一步增大氫氣壓強,H/M幾乎不變。反應(I)中z=________ (用含x和y的代數式表示)。溫度為T1時,2g某合金4min內吸收氫氣240mL,吸氫速率v=___________mL·g-lmin-1。反應的焓變△H1_____0(填“>”“<”或“=”)。
(2)η表示單位質量貯氫合金在氫化反應階段的最大吸氫量占其總吸氫量的比例,則溫度為Tl、T2時,η(T1)____η(T2)(填“>”“<”或“=”)。當反應(I )處于圖中a點時,保持溫度不變,向恒容體系中通入少量氫氣,達到平衡后反應(I)可能處于圖中的 ________點(填“b” “c”或“d”),該貯氫合金可通過________或____的方式釋放氫氣。
(3)貯氫合金ThNi5可催化由CO、H2合成CH4的反應,溫度為T時,該反應的熱化學方程式為___________。己知溫度為 T 時:CH4(g)+2H2O=CO2(g)+4H2(g) △H=+165kJ/mol CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41kJ/mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知高錳酸鉀在常溫下能與鹽酸溶液反應,其反應的化學方程式如下:2KMnO4+16HC1=2KCl+2MnCl2+5Cl2↑+8H2O
(1)用雙線橋表示電子轉移的方向和數目__________________________。
(2)上述反應中氧化劑是__________,氧化產物是__________。
(3)上述反應中氧化劑與還原劑的物質的量之比為__________。
(4)若反應中轉移了0.6mol 電子,產生的氣體在標準狀況下的體積是__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列圖示與對應的敘述相符的是
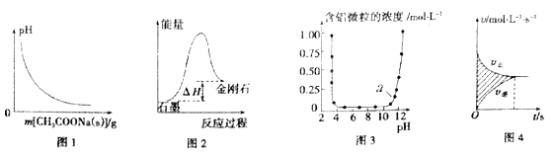
A. 圖1表示向0.1mol/L CH3COOH溶液中逐步加入CH3COONa固體后,溶液pH的變化
B. 圖2表示石墨轉化為金剛石反應過程中的能量變化,可判斷石墨比金剛石穩定
C. 圖3表示Al3+與OH-反應時溶液中含鋁微粒濃度變化曲線,圖中a點溶液中大量存在Al3+
D. 圖4表示某可逆反應的v-t曲線,圖中陰影部分面積的含義是(v正-v逆)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】既可以用來鑒別乙烯和甲烷,又可用來除去甲烷中混有的乙烯的方法是
A.通入足量溴水中B.與酸性高錳酸鉀溶液反應
C.在導管中處點燃D.一定條件下與H2反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】通過海水曬鹽可以得到粗鹽,粗鹽除含 NaCl 外,還含有少量 MgCl2、CaCl2、Na2SO4、KCl 以及泥沙等物質。以下是甲、乙同學在實驗室中粗鹽提純的操作流程。

提供的試劑:Na2CO3 溶液、K2CO3溶液、NaOH 溶液、BaCl2 溶液、75%乙醇。
(1)欲除去溶液 I 中的 MgCl2、CaCl2、Na2SO4,從提供的試劑中選出 a 所代表的試劑,按滴加順序依次為____。
A. 過量的 NaOH 溶液、Na2CO3 溶液、BaCl2 溶液
B. 過量的 NaOH 溶液、K2CO3、BaCl2 溶液
C. 過量的 NaOH 溶液、BaCl2 溶液、Na2CO3 溶液
D. 過量的 NaOH 溶液、BaCl2 溶液、K2CO3 溶液
(2)如何檢驗所加 BaCl2 溶液已過量____。
(3)在濾液中加鹽酸的作用是_____。鹽酸____(填“是”或“否”)可以過量。
(4)在洗滌的時候,可以使用的最佳洗滌劑是_____。
(5)乙同學欲使用提純得到的精鹽配制 100mL 1mol/L 的 NaCl 溶液,需要稱量 NaCl____g,需使用的玻 璃儀器除了燒杯、玻璃棒和膠頭滴管還有_____。
(6)甲同學觀察乙同學的操作,認為他配制的溶液濃度偏低,乙同學可能做的錯誤操作有____。
A. 定容時,仰視讀數
B. 洗滌容量瓶后沒有進行干燥
C. 未洗滌燒杯和玻璃棒 2 次~3 次
D. 在定容時加水超過刻度線,再用膠頭滴管吸出多余部分
E. 加水至刻度線后,搖勻過程中,發現液面低于刻度線
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學是材料科學、.生命科學、環境科學和能源科學的重要基礎。下列 有關說法正確的是( )
A.合金、合成纖維、合成橡膠、塑料都是有機高分子材料
B.香煙、酒精、嗎啡、海洛因都是毒品
C.二氧化硫、二氧化氮、一氧化碳都是大氣污染物
D.石油、煤、天然氣、氫氣都是不可再生的化石燃料
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】合成氨是人類科學技術上的一項重大突破,其反應原理為N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ·mol-1。一種工業合成氨的簡式流程圖如下:
2NH3(g) △H=-92.4kJ·mol-1。一種工業合成氨的簡式流程圖如下:

(1)天然氣中的H2S雜質常用氨水吸收,產物為NH4HS。一定條件下向NH4HS溶液中通入空氣,得到單質硫并使吸收液再生,寫出再生反應的化學方程式:____________________________。
(2)步驟Ⅱ中制氫氣的原理如下:
①CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
②CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
對于反應①,一定可以提高平衡體系中H2的百分含量,又能加快反應速率的措施是_________。
a.升高溫度 b.增大水蒸氣濃度 c.加入催化劑 d.降低壓強
利用反應②,將CO進一步轉化,可提高H2的產量。若1 mol CO和H2的混合氣體(CO的體積分數為20%)與H2O反應,得到1.18 mol CO、CO2和H2的混合氣體,則CO的轉化率為________。
(3)圖(a)表示500 ℃、60.0 MPa條件下,原料氣投料比與平衡時NH3體積分數的關系。根據圖中a點數據計算N2的平衡體積分數:_________。
(4)依據溫度對合成氨反應的影響,在圖(b)坐標系中,畫出一定條件下的密閉容器內,從通入原料氣開始,隨溫度不斷升高,NH3物質的量變化的曲線示意圖。_____

(5)上述流程圖中,使合成氨放出的能量得到充分利用的主要步驟是(填序號)_________。簡述本流程中提高合成氨原料總轉化率的方法:______________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com