
| ||
| △ |
| ||
| △ |
 ,故答案為:
,故答案為: ;
;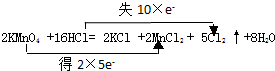 ,當標準狀況下有5mol氯氣生成時,該反應的電子轉移數為10NA,當標準狀況下有0.5mol即11.2L氯氣生成時,該反應的電子轉移數為NA.
,當標準狀況下有5mol氯氣生成時,該反應的電子轉移數為10NA,當標準狀況下有0.5mol即11.2L氯氣生成時,該反應的電子轉移數為NA.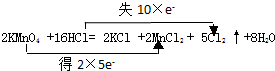 ; NA;
; NA;

 小學期末標準試卷系列答案
小學期末標準試卷系列答案科目:高中化學 來源: 題型:
| A、NaHS水解反應:HS-+H2O?H3O++S2- |
| B、1mol的Cl2通入含1mol FeI2的溶液中:2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2 |
| C、碳酸氫鈉溶液中加入過量Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+CO32-+2H2O |
| D、向明礬溶液中加入碳酸氫鈉:Al3++3HCO3-═Al(OH)3↓+3CO2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、1L 0.1 mol?L-1 NaCl溶液中含0.1NA個Na+ |
| B、22.4L NH3含4NA個原子 |
| C、標準狀況下,22.4L H2O中含有10NA個電子 |
| D、NA個SO2分子的質量為64 g/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| 溫度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡總壓強(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡氣體總濃度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |

查看答案和解析>>
科目:高中化學 來源: 題型:
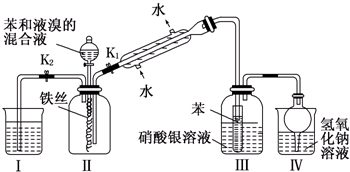
 某同學用如圖所示裝置探究SO2的性質及其有關實驗.
某同學用如圖所示裝置探究SO2的性質及其有關實驗.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com