
下列說法正確的是
A.反應熱就是反應中放出的能量
B.在101 kPa時,1 mol碳燃燒所放出的熱量為碳的燃燒熱
C.由C(s,石墨)= C(s,金剛石),ΔH=+1.9 kJ·mol-1可知,金剛石比石墨穩定
D.等量的硫蒸氣和硫固體分別完全燃燒,前者放出的熱量多
科目:高中化學 來源:2016屆廣東省等六校高三第一次聯考化學試卷(解析版) 題型:選擇題
已知下列反應: 反應Ⅰ:Co2O3 + 6HCl(濃) 2CoCl2 + Cl2↑+ 3H2O
2CoCl2 + Cl2↑+ 3H2O
反應Ⅱ:5Cl2 + I2 + 6H2O 10HCl + 2HIO3 下列說法正確的是
10HCl + 2HIO3 下列說法正確的是
A.反應Ⅰ中HCl是氧化劑 B.反應Ⅱ中Cl2發生氧化反應
C.還原性:CoCl2 > HCl > I2 D.氧化性:Co2O3 > Cl2 >HIO3
查看答案和解析>>
科目:高中化學 來源:2016屆黑龍江省高三上期中測試化學試卷(解析版) 題型:選擇題
我國知名企業比亞迪公司開發了具有多項專利的鋰釩氧化物二次電池,其成本較低,對環境無污染,能量密度遠遠高于其他電池,電池總反應為V2O5+xLi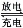 LixV2O5。下列說法合理的是
LixV2O5。下列說法合理的是
A.電池在放電時,Li+向負極移動
B.鋰在放電時作正極,充電時作陽極
C.該電池充電時陽極的反應為LixV2O5 _ xe-=V2O5 + xLi+
D.V2O5只是鋰發生反應的載體,不參與電池反應
查看答案和解析>>
科目:高中化學 來源:2015-2016學年吉林省高一上期中測試化學試卷(解析版) 題型:填空題
(4分)今有11種物質:①鋁線;②石墨;③氯氣;④BaSO4晶體;⑤純硫酸;⑥金剛石;⑦石灰水;⑧乙醇;⑨熔融的KNO3;⑩NH3;⑪鹽酸。其中:
(1)能導電的是(填序號,下同)____________________________;
(2)屬于電解質的是___________________________________;
(3)屬于非電解質的是_______________________________;
(4)既不是電解質又不是非電解質的是_____________________。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧師大附屬中學高二10月月考化學試卷(解析版) 題型:填空題
(8分)過氧化氫和臭氧都是常見的綠色氧化劑,工業生產中有著重要用途。
(1)火箭發射常以液態肼(N2H4)為燃料,液態過氧化氫為助燃劑。
已知:N2H4(l)+O2(g)===N2(g)+2H2O(g),ΔH=-534 kJ·mol-1
H2O2(l)===H2O(l)+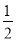 O2(g),ΔH=-98 kJ·mol-1
O2(g),ΔH=-98 kJ·mol-1
H2O(l)===H2O(g),ΔH=+44 kJ·mol-1
試寫出N2H4和液態H2O2反應生成氣態水的熱化學方程式_________________________。
(2)新型O3氧化技術對燃煤煙氣中的NOx和SO2脫除效果顯著,鍋爐煙氣中的NOx 95%以上是以NO形式存在的,可發生反應NO(g)+O3(g) NO2(g)+O2(g)。在一定條件下,將NO和O3通入絕熱恒容密閉容器中發生上述反應,正反應速率隨時間變化的示意圖如圖所示。由圖可得出的正確說法是________________。
NO2(g)+O2(g)。在一定條件下,將NO和O3通入絕熱恒容密閉容器中發生上述反應,正反應速率隨時間變化的示意圖如圖所示。由圖可得出的正確說法是________________。
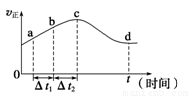
a.反應在c點達到平衡狀態
b.反應物濃度:b點小于c點
c.該反應為放熱反應
d.Δt1=Δt2時,NO的轉化量:a~b段小于b~c段
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山東壽光中學高二上10月月考化學試卷(解析版) 題型:選擇題
糕點包裝中常見的脫氧劑組成為還原性鐵粉、氯化鈉、炭粉等,其脫氧原理與鋼鐵的吸氧腐蝕相同。下列分析正確的是
A.脫氧過程是吸熱反應,可降低溫度,延長糕點保質期
B.脫氧過程中鐵作原電池正極,電極反應為:Fe-3e- →Fe3+
C.脫氧過程中碳做原電池負極,電極反應為:2H2O+O2+4e-→4OH-
D.含有1.12g鐵粉的脫氧劑,理論上最多能吸收氧氣336mL(標準狀況)
查看答案和解析>>
科目:高中化學 來源:2016屆河北省高三上學期四調考試化學試卷(解析版) 題型:選擇題
將一定量的銅粉加入到100mL某濃度的稀硝酸中充分反應后,容器中剩有m1g銅粉,此時共收集到NO氣體448mL(標準狀況).然后向上述混合物中加入足量稀硫酸至不再反應為止,容器剩有銅粉m2g,則(m1-m2)為
A.5.76 B.2.88 C.1.92 D.0
查看答案和解析>>
科目:高中化學 來源:2015-2016學年四川省高二上10月月考化學試卷(解析版) 題型:填空題
(12分)(1)Mn.Fe均為第四周期過渡元素,兩元素的部分電離能數據列于下表:
元 素 | Mn | Fe | |
電離能/kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
回答下列問題:Mn元素價電子層的電子排布式為 ,比較兩元素的I2.I3可知,氣態Mn2+再失去一個電子比氣態Fe2+再失去一個電子難。對此,你的解釋是
(2)白色的無水硫酸銅粉末溶于水得到藍色溶液,請解釋這一現象的原因(用離子方程式) ,向藍色溶液中加入氨水,首先形成藍色沉淀,繼續加入氨水,沉淀溶解得到深藍色透明溶液,請寫出沉淀溶解過程的離子方程式 。
(3)ZnS在熒光體、光導體材料、涂料、顏料等行業中應用廣泛。晶體結構如下圖所示,其晶胞邊長為540.0 pm,晶胞中Zn原子的配位數為 ,列式表示并計算立方ZnS晶體的密度(g·cm-3) 。
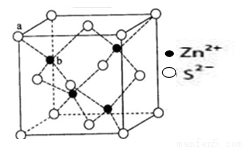
查看答案和解析>>
科目:高中化學 來源:2015-2016學年甘肅蘭州一中高二上期中測試理科化學試卷(解析版) 題型:選擇題
下圖表示反應N2(g)+3H2(g) 2NH3(g)ΔH=-92.2kJ/mol。在某段時間t0~t6中反應速率與反應過程的曲線圖如下,則氨的百分含量最高的一段時間是
2NH3(g)ΔH=-92.2kJ/mol。在某段時間t0~t6中反應速率與反應過程的曲線圖如下,則氨的百分含量最高的一段時間是
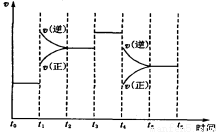
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com