

分析 (1)銅鋅原電池中,活潑金屬作負極,在正極上有氣體生成;若電解質為硫酸銅溶液,則在正極上析出銅;
(2)根據反應“2FeCl3+Fe=3FeCl2”可知,反應中鐵失電子而被氧化,應為原電池負極,Fe3+在正極得到電子而被還原,電解質溶液為FeCl3,依次分析解答;
(3)Mg、Al兩種金屬做電極,若電解質溶液是稀硫酸,Mg失電子是負極;若電解質溶液換作稀氫氧化鈉溶液,Al失電子是負極;
(4)堿性溶液中負極反應為2H2-4e-+4OH-=4H2O,正極反應為O2+4e-+2H2O=4OH-,電池總反應都為2H2+O2=2H2O;把KOH改為稀H2SO4作電解質,溶液中不可能生成OH-,故負極反應為H2-2e-=2H+,正極反應為O2+4H++4e-=2H2O,以此解答該題.
解答 解:(1)將Zn棒和Cu棒用導線連接后,若電解質溶液為稀硫酸,則鋅為負極,銅為正極,負極反應為Zn-2e-=Zn2+,正極反應為:2H++2e-=H2↑,在正極上有氣體生成;將Zn棒和Cu棒用導線連接后,若電解質為硫酸銅溶液,則在正極上析出銅,鋅為負極,負極反應為Zn-2e-=Zn2+,正極反應為Cu2++2e-=Cu,
故答案為:2H++2e-=H2↑;Cu2++2e-=Cu;
(2)由反應“2FeCl3+Fe=3FeCl2”可知,反應中鐵失電子而被氧化,應為原電池負極,負極上鐵失電子發生氧化反應,正極上鐵離子得電子發生還原反應,其電極反應式為:負極為Cu-2e-=Cu2+,正極為2Fe3++2e-=2Fe2+,
故答案為:Fe;Fe-2e-=Fe2+;
(3)Mg、Al兩種金屬做電極,若電解質溶液是稀硫酸,Mg失電子是負極,電極反應式為:Mg-2e-=Mg2+;若電解質溶液換作稀氫氧化鈉溶液,Al失電子是負極,Mg為正極,正反應的離子方程式為:2Al+2H2O+2OH-=2AlO2-+3H2↑,
故答案為:Mg-2e-=Mg2+;正極;
(4)堿性溶液中負極反應為2H2-4e-+4OH-=4H2O,正極反應為O2+4e-+2H2O=4OH-,電池總反應都為2H2+O2=2H2O,溶液體積增大,OH-濃度減小,則pH減小,
故答案為:2H2-4e-+4OH-=4H2O;O2+4e-+2H2O=4OH-;
如把KOH改為用稀H2SO4作電解質溶液,則負極的電極方程式為:H2-2e-=2H+,正極:O2+4H++4e-=2H2O;
故答案為:H2-2e-=2H+;O2+4H++4e-=2H2O.
點評 本題考查原電池的設計及原電池的工作原理、電極反應式書寫,題目難度不大,利用基礎知識可以解答.


科目:高中化學 來源: 題型:選擇題
| A. | ⅠA族元素的金屬性比ⅡA族元素的金屬性強 | |
| B. | ⅥA族元素的氫化物中,穩定性最好的其沸點也最高 | |
| C. | 同周期非金屬氧化物對應的水化物的酸性從左到右依次增強 | |
| D. | 短周期中次外層電子數是最外層電子數2倍的元素一定是非金屬元素 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 制催化劑的材料 | B. | 半導體材料 | ||
| C. | 制農藥的材料 | D. | 耐高溫、耐腐蝕的合金材料 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
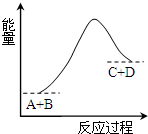
| A. | 該反應反應物A的能量大于生成物D的能量 | |
| B. | 該反應為吸熱反應 | |
| C. | 反應物的總能量高于生成物的總能量 | |
| D. | 該反應只有在加熱條件下才能進行 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 高純度的硅單質廣泛用于制作光導纖維,光導纖維遇強堿會“斷路” | |
| B. | 氮的固定只有在高溫、高壓、催化劑的條件下才能實現 | |
| C. | 服用鉻含量超標的藥用膠囊會對人體健康不會造成危害 | |
| D. | 高鐵酸鉀(K2FeO4)是一種新型、高效、多功能水處理劑,既能殺菌消毒又能凈水 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用A表示的反應速率是0.4 mol/(L•min) | |
| B. | 用B表示的反應速率是0.3 mol/(L•min) | |
| C. | 2 min末時的反應速率,用B表示是0.3 mol/(L•min) | |
| D. | 用D表示的反應速率為0.1 mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
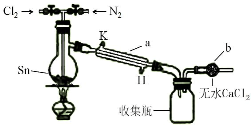 四氯化錫(SnCl4)在電子、化工等領域有重要用途.某興趣小組擬用Sn和Cl2反應制備SnCl4.
四氯化錫(SnCl4)在電子、化工等領域有重要用途.某興趣小組擬用Sn和Cl2反應制備SnCl4.| 實驗內容 | 實驗現象 | 結論 |
| 實驗1:滴入KI溶液,再加淀粉溶液 | 溶液最終變為藍色 | 產品中含有Cl2 |
| 實驗2:① | ② | |
| 實驗3:③ | ④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
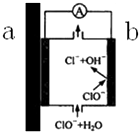 自來水管道經歷了從鑄鐵管→鍍鋅管→PVC管→PPR熱熔管等階段,鑄鐵管、鍍鋅管被棄用的原因之一,可以用原電池原理來解釋,示意圖如圖所示,下列有關說法不正確的是( )
自來水管道經歷了從鑄鐵管→鍍鋅管→PVC管→PPR熱熔管等階段,鑄鐵管、鍍鋅管被棄用的原因之一,可以用原電池原理來解釋,示意圖如圖所示,下列有關說法不正確的是( )| A. | 如果是鍍鋅管,則a端為Zn,是負極,產生Zn2+,不但會造成管道銹蝕,Zn2+溶于自來水也對人體有害 | |
| B. | b端發生的電極反應為:ClO-+H2O-2e-═Cl-+2OH- | |
| C. | 由于該原電池原理的存在,一定程度上減弱了自來水中余氯的殺菌消毒功能 | |
| D. | 從自來水廠到用戶,經過該類管道的長期接觸,自來水的酸堿性發生了變化 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com