
【題目】對氨基苯甲酸酯類是一類局部麻醉藥,化合物M是該類藥物之一。合成M的一種路線如下:

已知以下信息:
①核磁共振氫譜顯示B只有一種化學環境的氫,H苯環上有兩種化學環境的氫。
② 。
。
③E為芳香烴,其相對分子質量為92。
④![]() (苯胺,易被氧化)。
(苯胺,易被氧化)。
回答下列問題:
(1)A的結構簡式為_________________,其化學名稱是_____________________。
(2)由E生成F的化學方程式為_________________________________________。
(3)由G生成H的反應類型為__________________,H在一定條件下可以發生聚合反應,寫出該聚合反應的化學方程式__________________________________________________。
(4)M的結構簡式為________________________________。
(5)D的同分異構體中不能與金屬鈉反應生成氫氣的共有_________種(不考慮立體異構),其中核磁共振氫譜只有兩組峰,且峰面積比為6:1的是_________________(寫結構簡式)。
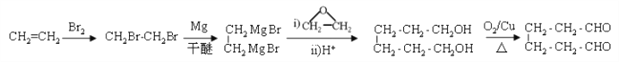
(6)參照上述合成路線,以乙烯和環氧乙烷為原料(無機試劑任選)制備1,6-己二醛,設計合成路線 ___________________________________________________________________。
【答案】 ![]() 2—甲基丙烯
2—甲基丙烯 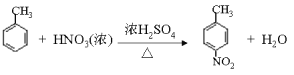 還原反應 n
還原反應 n ![]()
![]()
![]() +(n—1)H2O
+(n—1)H2O 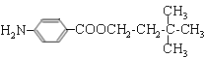 15
15 ![]()
【解析】A與溴化氫發生加成反應生成B,磁共振氫譜顯示B只有一種化學環境的氫,則B的結構簡式為CBr(CH3)3,則A的結構簡式為CH2=C(CH3)2。根據已知信息②可知C與環氧乙烷反應生成D,則D的結構簡式為(CH3)3CCH2CH2OH。E為芳香烴,其相對分子質量為92,則E是甲苯,甲苯發生硝化反應生成F,由于H苯環上有兩種化學環境的氫,這說明硝基在甲基的對位,即F的結構簡式為![]() 。由于氨基易被氧化,所以F生成G是甲基的氧化反應,引入羧基,即G的結構簡式為
。由于氨基易被氧化,所以F生成G是甲基的氧化反應,引入羧基,即G的結構簡式為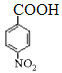 。G中的硝基被還原轉化為氨基,則H的結構簡式為
。G中的硝基被還原轉化為氨基,則H的結構簡式為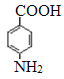 。H和D發生酯化反應生成M,則M的結構簡式為
。H和D發生酯化反應生成M,則M的結構簡式為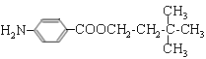 。
。
(1)根據以上分析可知A的結構簡式為![]() ,其化學名稱是 2-甲基丙烯。(2)由E生成F的化學方程式為
,其化學名稱是 2-甲基丙烯。(2)由E生成F的化學方程式為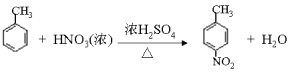 。(3)由G生成H的反應類型為還原反應,H分子中含有羧基和氨基,在一定條件下可以發生聚合反應,該聚合反應的化學方程式 n
。(3)由G生成H的反應類型為還原反應,H分子中含有羧基和氨基,在一定條件下可以發生聚合反應,該聚合反應的化學方程式 n![]()
![]()
![]() +(n—1)H2O。(4)M的結構簡式為
+(n—1)H2O。(4)M的結構簡式為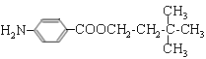 。(5)D的同分異構體中不能與金屬鈉反應生成氫氣,說明含有醚鍵,可以是甲醇和戊醇形成,戊基有8種,相應醚有8種;可以是乙醇和丁醇形成,丁醇有4種,相應醚有4種;可以是2分子丙醇形成,丙醇有2種,相應的醚類有3種,共計15種(不考慮立體異構),其中核磁共振氫譜只有兩組峰,且峰面積比為6:1的是
。(5)D的同分異構體中不能與金屬鈉反應生成氫氣,說明含有醚鍵,可以是甲醇和戊醇形成,戊基有8種,相應醚有8種;可以是乙醇和丁醇形成,丁醇有4種,相應醚有4種;可以是2分子丙醇形成,丙醇有2種,相應的醚類有3種,共計15種(不考慮立體異構),其中核磁共振氫譜只有兩組峰,且峰面積比為6:1的是![]() 。(6)參照上述合成路線和題干信息可知以乙烯和環氧乙烷為原料(無機試劑任選)制備1,6-己二醛的合成路線為
。(6)參照上述合成路線和題干信息可知以乙烯和環氧乙烷為原料(無機試劑任選)制備1,6-己二醛的合成路線為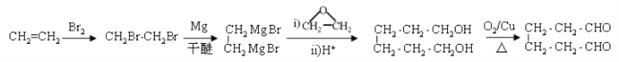 。
。


科目:高中化學 來源: 題型:
【題目】以“物質的量”為中心的計算是化學計算的基礎,下列與“物質的量”相關的計算正確的是
A.現有CO、CO2、O3三種氣體,它們分別都含有1 mol O,則三種氣體的物質的量之比為3∶2∶1
B.n g Cl2中有m個Cl原子,則阿伏加德羅常數NA的數值可表示為![]()
C.標準狀況下,11.2 L X氣體分子的質量為16 g,則X氣體的摩爾質量是32
D.5.6 g CO和22.4 L CO2中含有的碳原子數一定相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氣態中性基態原子的原子核外電子排布發生如下變化,吸收能量最多的是( )
A. 1s22s22p63s23p2→1s22s22p63s23p1
B. 1s22s22p63s23p3→1s22s22p63s23p2
C. 1s22s22p63s23p4→1s22s22p63s23p3
D. 1s22s22p63s23p63d104s24p1→1s22s22p63s23p63d104s2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物X是一種醫藥中間體,其結構簡式如圖所示。下列有關化合物X的說法正確的是

A.分子中兩個苯環一定處于同一平面
B.不能與飽和Na2CO3溶液反應
C.在酸性條件下水解,水解產物只有一種
D.1 mol化合物X最多能與2 mol NaOH反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】填寫下列空白:
(1) ______mol H2O中含有的氧原子數與1.5 mol CO2中含有的氧原子數相等。
(2)將等物質的量的NH3和CH4混合,混合氣體中NH3與CH4的質量比為______。
(3)要使NH3與CH4含相同數目的H原子,則NH3和CH4的物質的量之比為______。
(4)標準狀況下,密度為0.75 g·L1的NH3與CH4組成的混合氣體中,NH3的體積分數為______,該混合氣體對氫氣的相對密度為______。
(5)某結晶水合物的化學式為A·nH2O,A的相對分子質量為M。如將a g該結晶水合物加熱至結晶水全部失去,剩余的殘渣為b g,則n=______。
(6)已知a g A和b g B恰好完全反應生成0.2 mol C和d g D,則C的摩爾質量為______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮和鈉可形成化合物Na3N,它能與水劇烈反應產生NH3,下列敘述正確的是:( )
A. Na3N與水的反應是氧化還原反應
B. Na3N 是共價化合物
C. Na3N中4個離子均滿足最外層8電子穩定結構
D. Na3N中鈉離子半徑大于氮離子半徑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,根據表中列出的10種元素,回答下列問題。
族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0 |
2 | C | N | O | Ne | ||||
3 | Na | Mg | Al | Si | S | Cl |
(1)O和S中,原子半徑較大的是________;(填元素符號或化學,以下同)
(2)CH4和NH3中,熱穩定性較強的是________;
(3)新制氯水有漂白作用,是因為其中含有________;
(4)元素最高價氧化物對應水化物中,堿性最強的是________,存放該溶液的試劑瓶蓋不能用玻璃塞,請寫出該反應的離子方程式_____________________________________;元素最高價氧化物對應水化物中,兩性氫氧化物是__________;
(5)為了除去甲烷混有的少量乙烯可用________試劑;
(6)乙酸與乙醇在一定條件下可制備具有特殊香味的物質,請寫出該反應的化學方程式____________________;試驗中用到了飽和碳酸鈉溶液,其作用有____________________。
(7) 在2 L的密閉容器中,充入2 mol N2和3 mol H2,在一定條件下發生反應,3 s后測得N2為1.9 mol,則以H2的濃度變化表示的反應速率為__________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用電解乙二醛制備乙二酸(HOOC-COOH)的裝置如圖所示,通電后,Pt2電極上產生的氯氣將乙二醛氧化為乙二酸,下列說法正確的是

A. Pt2接電源的負極,發生還原反應
B. 鹽酸的作用是提供Cl-和增強導電性
C. 電路上每轉移1mol電子產生45g乙二酸
D. Pt1極上的電極反應為:2H2O-4e-=== O2↑ + 4H+
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com