
| 元素代號 | L | M | X | R | T |
| 原子半徑/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合價 | +2 | +3 | +6、-2 | +2 | -2 |
| A. | R的氧化物對應的水化物可能具有兩性 | |
| B. | X單質可在氧氣中燃燒生成XO3 | |
| C. | 離子半徑大小:r (M3+)>r (T2-) | |
| D. | L2+和X2-的核外電子數相等 |
分析 短周期主族元素中,元素最高正化合價與其族序數增大,最低負化合價=族序數-8,原子電子層數越多其原子半徑越大,同一周期元素,原子半徑隨著原子序數增大而減小;
根據表中數據知,L、R屬于第IIA族元素,原子半徑L>R,則L是Mg、R是Be元素;
M屬于第IIIA族元素,原子半徑M>R,則M是Al元素;
X、T最低負價是-2,則X和T屬于第VIA族元素,X有正化合價、T沒有正化合價,所以X是S、T是O元素,
A.R是Be元素,氫氧化鈹具有兩性;
B.X是S元素,S單質在氧氣中燃燒生成二氧化硫;
C.M是Al元素、T是O元素,電子層結構相同的離子,離子半徑隨著原子序數增大而減小;
D.L是Mg元素、X是S元素,鎂離子核外有10個電子、硫離子核外有18個電子.
解答 解:短周期主族元素中,元素最高正化合價與其族序數增大,最低負化合價=族序數-8,原子電子層數越多其原子半徑越大,同一周期元素,原子半徑隨著原子序數增大而減小;
根據表中數據知,L、R屬于第IIA族元素,原子半徑L>R,則L是Mg、R是Be元素;
M屬于第IIIA族元素,原子半徑M>R,則M是Al元素;
X、T最低負價是-2,則X和T屬于第VIA族元素,X有正化合價、T沒有正化合價,所以X是S、T是O元素,
A.R是Be元素,根據對角線規則知,Al和Be性質相似,所以氫氧化鈹可能具有兩性,故A正確;
B.X是S元素,S單質在氧氣中燃燒生成二氧化硫,二氧化硫和氧氣在催化劑、加熱條件下反應生成三氧化硫,故B錯誤;
C.M是Al元素、T是O元素,電子層結構相同的離子,離子半徑隨著原子序數增大而減小,所以離子半徑r(M3+)<r(T2-),故C錯誤;
D.L是Mg元素、X是S元素,鎂離子核外有10個電子、硫離子核外有18個電子,所以兩種離子核外電子數不等,故D錯誤;
故選A.
點評 本題考查原子結構和元素性質,側重考查分析推斷能力,明確主族元素化合價與族序數的關系、原子半徑規律即可解答,注意元素周期表中元素性質遵循對角線規則,題目難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題

| A. | 一定狀況下,氣體摩爾體積(y)與該氣體的物質的量(x)的關系 | |
| B. | 鐵在氯氣中燃燒,生成FeCl3的物質的量(y)與消耗氯氣的物質的量(x)的關系 | |
| C. | 將鐵在常溫下放入濃硫酸中,生成氣體的物質的量(y)與消耗濃硫酸的物質的量(x)的關系 | |
| D. | H2SO4溶液的物質的量濃度(y)與其質量分數(x) 的關系 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | J | F | H | I |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
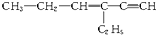 ,分子中含有四面體結構的碳原子(即飽和碳原子)數為a,在同一直線上的碳原子數為b,一定在同一平面上的碳原子數為c,則a、b、c分別為( )
,分子中含有四面體結構的碳原子(即飽和碳原子)數為a,在同一直線上的碳原子數為b,一定在同一平面上的碳原子數為c,則a、b、c分別為( )| A. | 4,3,5 | B. | 4,3,6 | C. | 2,5,4 | D. | 4,6,4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 日常生活中無水乙醇常用于殺菌消毒 | |
| B. | 棉、麻、絲、毛及合成纖維完全燃燒都只生成CO2和H2O | |
| C. | 加熱能殺死流感病毒式因為病毒的蛋白質受熱變性 | |
| D. | 人造纖維、合成纖維和光導纖維都是有機高分子化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 原子序數小于36的X、Y、Z、W四種元素,其中X是形成化合物種類最多的元素之一,Y的基態原子最外層電子數是其內層電子總數的2倍,Z的基態原子2p軌道上有3個未成對電子,W的原子序數為29.
原子序數小于36的X、Y、Z、W四種元素,其中X是形成化合物種類最多的元素之一,Y的基態原子最外層電子數是其內層電子總數的2倍,Z的基態原子2p軌道上有3個未成對電子,W的原子序數為29.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com