
 2NH3(g) ΔH<0 反應(yīng)中NH3的物質(zhì)的量濃度的變化的情況如圖所示:
2NH3(g) ΔH<0 反應(yīng)中NH3的物質(zhì)的量濃度的變化的情況如圖所示: 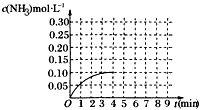
科目:高中化學(xué) 來源: 題型:
(9分)在一容積為2 L的密閉容器內(nèi)加入0.2 mol的N2和0.6 mol的H2,在一定條件下發(fā)生如下反應(yīng):N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,反應(yīng)中NH3的物質(zhì)的量濃度的變化情況如下圖:
2NH3(g) ΔH<0,反應(yīng)中NH3的物質(zhì)的量濃度的變化情況如下圖:
請回答下列問題:
(1)該反應(yīng)的化學(xué)平衡常數(shù)K表達(dá)式為______________________;
升高溫度K值 (填“變大”、“變小”或“不變”)
(2)根據(jù)上圖,計算從反應(yīng)開始到平衡時,平均反應(yīng)速率v(H2)為____________。
(3)判斷該反應(yīng)達(dá)到平衡狀態(tài)的標(biāo)志是 (填字母);
a.N2和NH3濃度相等 b.NH3百分含量保持不變
c.容器中氣體的壓強不變 d.NH3的生成速率與H2的消耗速率相等
e.容器中混合氣體的密度保持不變
(4)反應(yīng)達(dá)到平衡后,第5分鐘末,保持其它條件不變,若改變反應(yīng)溫度,則NH3的物質(zhì)的量濃度不可能為_______________。
a. 0.20 mol/L b. 0.12 mol/L c.0.10 mol/L d.0.08 mol/L
(5)在第5分鐘末將容器的體積縮小一半后,若在第8分鐘末達(dá)到新的平衡(此時NH3的濃度約為0.25mol/L),請在上圖中畫出第5分鐘末達(dá)到此平衡時NH3濃度的變化曲線。
查看答案和解析>>
科目:高中化學(xué) 來源:2012-2013學(xué)年福建省晉江市養(yǎng)正中學(xué)高二下學(xué)期第一次月考化學(xué)試卷(帶解析) 題型:填空題
(16分)氮是地球上含量豐富的一種元素,氮及其化合物在工農(nóng)業(yè)生產(chǎn)、生活中有著重要作用,合成氨工業(yè)在國民生產(chǎn)中有重要意義。以下是關(guān)于合成氨的有關(guān)問題,請回答:
(1)若在一容積為2 L的密閉容器中加入0.2 mol的N2和0.6 mol的H2在一定條件下發(fā)生反應(yīng): N2(g) +3H2(g) 2NH3(g) ΔH<0,若在5分鐘時反應(yīng)達(dá)到平衡,此時測得NH3的物質(zhì)的量為0.2 mol。則前5分鐘的平均反應(yīng)速率v(N2)= 。平衡時H2的轉(zhuǎn)化率為 。?
2NH3(g) ΔH<0,若在5分鐘時反應(yīng)達(dá)到平衡,此時測得NH3的物質(zhì)的量為0.2 mol。則前5分鐘的平均反應(yīng)速率v(N2)= 。平衡時H2的轉(zhuǎn)化率為 。?
(2)平衡后,若要提高H2的轉(zhuǎn)化率,可以采取的措施有 。?
A.加了催化劑 B.增大容器體積?C.降低反應(yīng)體系的溫度 D.加入一定量N2?
(3)若在0.5 L的密閉容器中,一定量的氮氣和氫氣進(jìn)行如下反應(yīng):?
N2(g)+3H2(g) 2NH3(g) ΔH<0,其化學(xué)平衡常數(shù)K與溫度T的關(guān)系如表所示:?
2NH3(g) ΔH<0,其化學(xué)平衡常數(shù)K與溫度T的關(guān)系如表所示:?
| T/℃ | 200 | 300 | 400 |
| K | K1 | K3 | 0.5 |
 N2(g)+3H2(g)的化學(xué)平衡常數(shù)為 。當(dāng)測得NH3、N2和H2物質(zhì)的量分別為3 mol、2 mol和 1 mol時,則該反應(yīng)的v(N2)正 v(N2)逆(填“<”“>”或“=”)。?
N2(g)+3H2(g)的化學(xué)平衡常數(shù)為 。當(dāng)測得NH3、N2和H2物質(zhì)的量分別為3 mol、2 mol和 1 mol時,則該反應(yīng)的v(N2)正 v(N2)逆(填“<”“>”或“=”)。?查看答案和解析>>
科目:高中化學(xué) 來源:2011-2012學(xué)年江蘇省揚州市邗江區(qū)高二下學(xué)期期中考試化學(xué)試卷(帶解析) 題型:填空題
(10分)在一容積為2 L的密閉容器中加入2 molA和3 molB,保持溫度為30℃,在催化劑存在的條件下進(jìn)行下列反應(yīng):A(g)+2B(g) 3C(g),達(dá)到平衡后生成1.5 mol C,此時,平衡混合氣中C的體積分?jǐn)?shù)為ω;若將溫度升高到70℃后,其他條件均不變,當(dāng)反應(yīng)重新達(dá)到平衡時,C的物質(zhì)的量為1.2 mol。
3C(g),達(dá)到平衡后生成1.5 mol C,此時,平衡混合氣中C的體積分?jǐn)?shù)為ω;若將溫度升高到70℃后,其他條件均不變,當(dāng)反應(yīng)重新達(dá)到平衡時,C的物質(zhì)的量為1.2 mol。
請回答下列問題,
(1)該反應(yīng)的焓變△H 0(填“>”、“<”或“=”)。
(2)30℃時,平衡混合氣中C的體積分?jǐn)?shù)ω= ,A物質(zhì)的轉(zhuǎn)化率與B物質(zhì)的轉(zhuǎn)化率之比為 。
(3)30℃時,若在同一容器中加入1.5 mol A、 mol B和1.5 mol C,則平衡混合氣中C的體積分?jǐn)?shù)仍為ω,此時平衡體系中A的物質(zhì)的量濃度為 mol·L-1。
查看答案和解析>>
科目:高中化學(xué) 來源:2013屆四川省高二下學(xué)期期中考試化學(xué)試卷(解析版) 題型:填空題
(10分)在一容積為2 L的密閉容器中,加入0.2 mol的N2和0.6 mol的H2,在一定條件下發(fā)生反應(yīng):N2(g)+3H2(g)  2NH3(g) ΔH<0
2NH3(g) ΔH<0
反應(yīng)中NH3的物質(zhì)的量濃度的變化情況如下圖所示,請回答下列問題:

(1)根據(jù)上圖,計算從反應(yīng)開始到平衡時,平均反應(yīng)速率v(NH3)為______________.
(2)該反應(yīng)達(dá)到平衡時H2的轉(zhuǎn)化率________.
(3)反應(yīng)達(dá)到平衡后,第5分鐘末,保持其它條件不變,若改變反應(yīng)溫度,達(dá)到新平衡時NH3的物質(zhì)的量濃度不可能為____________.(填序號)
A、0.20 mol·L-1 b、0.12 mol·L-1 c、0.10 mol·L-1 d、0.08 mol·L-1
(4)在第5分鐘末將容器的體積縮小一半后,若在第8分鐘末達(dá)到新的平衡(此時NH3的濃度約為0.25 mol·L-1),請在上圖中畫出第5分鐘末到此平衡時NH3濃度的變化曲線.
(5)如果上述反應(yīng)在相同溫度和容器中進(jìn)行,欲使反應(yīng)達(dá)到平衡時NH3的物質(zhì)的量分?jǐn)?shù)與原平衡相等,起始加入的三種物質(zhì)的物質(zhì)的量n(N2)、n(H2)、n(NH3)分別為a、b、c,則a、b、c之間應(yīng)該滿足的關(guān)系式為:
(6)若該反應(yīng)在298K、398K時的化學(xué)平衡常數(shù)分別為K1、K2,則K1 K2(填“>” “=” 或 “<” )。
查看答案和解析>>
科目:高中化學(xué) 來源:2013屆廣東省高二上學(xué)期期中考試化學(xué)試卷 題型:填空題
(20分)在一容積為2 L的密閉容器內(nèi)加入0.2 mol 的N2和0.6 mol 的H2,在一定條件下發(fā)生如下反應(yīng):N2(g)+3H2(g) 2NH3(g) △H<0,反應(yīng)中NH3的物質(zhì)的量濃度的變化的情況如右圖:
2NH3(g) △H<0,反應(yīng)中NH3的物質(zhì)的量濃度的變化的情況如右圖:

(1)根據(jù)右圖,計算從反應(yīng)開始到平衡時,平均反應(yīng)速率v(NH3)為____ _。
(2)該反應(yīng)的化學(xué)平衡常數(shù)表達(dá)式K = ____ _ 。
(3)反應(yīng)達(dá)到平衡后,第5分鐘末,保持其它條件不變,若改變反應(yīng)溫度,則NH3的物質(zhì)的量濃度不可能為________。
a. 0.20 mol/L b. 0.12 mol/L c. 0.10 mol/L d. 0.08 mol/L
(4)反應(yīng)達(dá)到平衡后,第5分鐘末,保持其它條件不變,若只把容器的體積縮小一半,平衡_________________________移動(填“向逆反應(yīng)方向”、“向正反應(yīng)方向”或“不”),化學(xué)平衡常數(shù)________________(填“增大”、“減小”或“不變”)。
(5)在第5分鐘末將容器的體積縮小一半后,若在第8分鐘末達(dá)到新的平衡(此時NH3的濃度約為0.25 mol/L)。請在上圖中畫出第5分鐘末到此平衡時NH3濃度的變化曲線。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com