
【題目】某化學興趣小組利用下列裝置制取氨氣并探究氨氣的有關性質。

(1)圖一是實驗室制取氨氣的發生裝置,試管中反應的化學方程式為_______________。
(2)圖二可用于實驗室快速制取氨氣,A中燒瓶內試劑可選用________(填序號,下同)。
a.堿石灰 b.濃硫酸 c.生石灰 d.五氧化二磷
(3)為探究氨氣的溶解性,先利用圖三裝置收集氨氣,氨氣的進氣口為_____(填“a”或“b”),在實驗過程中觀察到圖三中的燒瓶內產生了紅色噴泉,則說明氨氣具有的物理性質是___。
(4)通過上面裝置制得的NH3進行如下實驗(實驗前旋塞1、2均關閉)。

①先打開旋塞1,D瓶中的現象是_____________,原因是_______________(用化學方程式表示);
②穩定后,關閉旋塞1,再打開旋塞2,觀察到的現象是___________________。
(5)為防止環境污染,以下裝置(除⑤標明外,其余盛放的液體均為水)可用于吸收多余氨氣的是____________(填序號)。

【答案】Ca(OH)2+2NH4Cl![]() CaCl2+2H2O+2NH3↑ ac a 極易溶于水 出現白煙 NH3+HCl= NH4Cl 水倒流入D中 ②④⑤
CaCl2+2H2O+2NH3↑ ac a 極易溶于水 出現白煙 NH3+HCl= NH4Cl 水倒流入D中 ②④⑤
【解析】
(1)根據實驗室用加熱氯化銨和氫氧化鈣的混合物制取氨氣,書寫反應的化學方程式;
(2)根據圖二,用于實驗室快速制取氨氣的基本原理是利用氨氣的揮發性,能夠加快氨氣揮發的都可以;
(3)根據氨氣的密度比空氣小,極易溶于水分析解答;
(4)根據氯化氫和氨氣化合生成氯化銨固體顆粒分析解答;
(5)氨氣極易溶于水,用溶液吸收多余氨氣時,需要防止倒吸,據此分析判斷。
(1)實驗室用加熱氯化銨和氫氧化鈣的混合物制取氨氣,反應的化學方程式為Ca(OH)2+2NH4Cl![]() CaCl2+2H2O+2NH3↑,故答案為:Ca(OH)2+2NH4Cl
CaCl2+2H2O+2NH3↑,故答案為:Ca(OH)2+2NH4Cl![]() CaCl2+2H2O+2NH3↑;
CaCl2+2H2O+2NH3↑;
(2)a.堿石灰溶于水放熱,加快氨氣的揮發,可以快速制取氨氣,故a正確;b.濃硫酸能夠與氨氣反應,不能用于制備氨氣,故b錯誤;c.生石灰與水反應是放熱反應,溶液溫度升高,促進氨氣放出,可以快速制取氨氣,故c正確;d.五氧化二磷的水溶液為磷酸,能夠與氨氣反應,不能用于制備氨氣,故d錯誤;故答案為:ac;
(3)氨氣的密度比空氣小,因此收集氨氣時的進氣口為a,在實驗過程中觀察到燒瓶內產生了紅色噴泉,說明氨氣極易溶于水,故答案為:a;極易溶于水;
(4)①先打開旋塞1,氯化氫和氨氣化合生成氯化銨固體顆粒,NH3+HCl= NH4Cl,因此D瓶中的現象是出現白煙,故答案為:出現白煙;NH3+HCl= NH4Cl;
②生成的氯化銨為固體,使得瓶中氣體的壓強減小,穩定后,關閉旋塞1,再打開旋塞2,可以觀察到水倒流入D中,故答案為:水倒流入D中;
(5)氨氣極易溶于水,為防止環境污染,用溶液吸收多余氨氣時,需要防止倒吸,根據圖示,裝置②④⑤均可防止倒吸,故答案為:②④⑤。


 學而優暑期銜接南京大學出版社系列答案
學而優暑期銜接南京大學出版社系列答案 Happy holiday歡樂假期暑假作業廣東人民出版社系列答案
Happy holiday歡樂假期暑假作業廣東人民出版社系列答案科目:高中化學 來源: 題型:
【題目】某固體酸燃料電池以CaHSO4固體為電解質傳遞H+,其基本結構見圖,電池總反應可表示為: 2H2+O2=2H2O,下列有關說法錯誤的是

A. 電子通過外電路從a極流向b極
B. b極上的電極反應式為:O2+4H++4e-=2H2O
C. H+由b極通過固體酸電解質傳遞到a極
D. 每轉移0.1 mol電子,標準狀況下需消耗1.12 L的H2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,其中甲池的總反應式為2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列說法正確的是
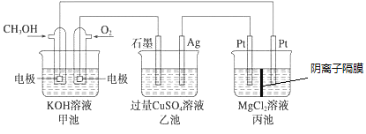
A. 甲池是電能轉化為化學能的裝置,乙、丙池是化學能轉化電能的裝置
B. 甲池通入CH3OH的電極反應式為CH3OH-6e-+2H2O=CO32-+8H+
C. 反應一段時間后,向乙池中加入一定量Cu(OH)2固體能使溶液恢復原濃度
D. 甲池中消耗4.48L(標準狀況下)O2,此時丙池中理論上最多產生23.2 g固體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖所示裝置中,甲、乙、丙三個燒杯依次分別盛放100 g 5.00%的NaOH溶液、足量的CuSO4溶液和100 g 10.00%的K2SO4溶液,電極均為石墨電極。
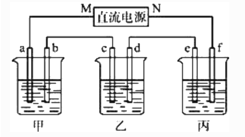
接通電源,經過一段時間后,測得丙中K2SO4的質量分數變為10.47%,乙中c電極質量增加。
①電源的N端為________極;
②電極b上發生的電極反應式為___________________________________________;
③電極b上生成的氣體在標準狀況下的體積___________L;
④電極c的質量變化是________g;
⑤電解前后溶液的pH保持不變的是________。
A.甲溶液 B.乙溶液 C.丙溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】芳綸可以制成防彈衣、防彈頭盔、防彈裝甲等,對位芳綸纖維J(聚對苯二甲酰對苯二胺)是重要的國防軍工材料。化合物A、乙烯、苯制備J的一種合成路線如下:

回答下列問題:
(1)A的化學名稱為____________________。
(2)A→B的反應類型是____________________。
(3)實驗室由苯制備F所需試劑、條件分別為____________________。
(4)G中官能團的名稱是____________________。
(5)E與I反應生成J的化學方程式為____________________。
(6)寫出與D互為同分異構體的只含酯基的結構簡式(核磁共振氫譜為四組峰,峰面積比為2:2:1:1____________________。
(7)參照上述合成路線,以1,3-戊二烯和丙烯為原料(無機試劑任選),設計制備鄰苯二甲酸的合成路線____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下在一容積不變的密閉容器中發生可逆反應2X(g) ![]() Y(g)+Z(s),以下不能說明該反應達到化學平衡狀態的是( )
Y(g)+Z(s),以下不能說明該反應達到化學平衡狀態的是( )
A. 混合氣體的密度不再變化 B. 反應容器中Y的質量分數不變
C. X的分解速率與Y的消耗速率相等 D. 單位時間內生成1 mol Y的同時生成2 mol X
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知X、Y、Z、W為短周期主族元素,在周期表中的相對位置如圖,有下列說法:

①若HmXOn為強酸,則X的氫化物溶于水一定顯酸性(m、n均為正整數)
②若四種元素均為金屬,則Z的最高價氧化物對應的水化物一定為強堿
③若四種元素均為非金屬,則W的最高價氧化物對應的水化物一定為強酸
④若四種元素只有一種為金屬,則Z與Y的最高價氧化物對應的水化物一定為強酸。
其中正確的說法有幾項( )
A. 1項 B. 2項 C. 3項 D. 4項
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com