
【題目】固定和利用CO2能有效地利用資源,并減少空氣中的溫室氣體.CO2與化合物Ⅰ反應生成化合物Ⅱ,如反應所示(其他試劑、產物及反應條件均省略).
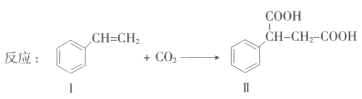
(1)化合物Ⅰ的官能團名稱為___________,分子式為______,1 mol該物質完全燃燒需消耗_______mol O2 .
(2)寫出化合物Ⅰ在一定條件下的加聚反應方程式___________。(不需要注明反應條件).
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】某原電池反應的離子方程式為Fe+2H+=Fe2++H2↑,則下列說法正確的是
A. 硝酸可能為電解質溶液
B. 鋅可能為原電池正極
C. 鐵的質量不變
D. 銅可能為原電池正極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】N2O5在一定溫度下可發生下列反應:2N2O5(g)![]() 4NO2(g)+O2(g) ΔH>0。T1溫度下的部分實驗數據為:
4NO2(g)+O2(g) ΔH>0。T1溫度下的部分實驗數據為:
t/s | 0 | 500 | 1 000 | 1 500 |
c(N2O5)/mol/ L | 5.00 | 3.52 | 2.50 | 2.50 |
下列說法不正確的是
A.500 s內N2O5分解速率為2.96×10-3 mol/(L·s)
B.T1溫度下的平衡常數為K1=125,1 000 s時轉化率為50%
C.其他條件不變時,T2溫度下反應到1 000 s時測得N2O5(g)濃度為2.98 mol/L,則T1<T2
D.T1溫度下的平衡常數為K1,T3溫度下的平衡常數為K3,若K1>K3,則T1>T3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列對化學反應速率和化學平衡的分析中,不正確的是
①在一密閉容器中充入1 mol H2和1 mol I2,達到平衡后,保持恒壓,向其中再加入1 mol H2和1 mol I2,重新達到平衡時,反應速率增大
②已達平衡的反應N2(g)+3H2(g)![]() 2NH3(g) △H<0,升高溫度,可以增大正反應速率,減小逆反應速率
2NH3(g) △H<0,升高溫度,可以增大正反應速率,減小逆反應速率
③在2 L密閉容器中充入2 mol A氣體和1 mol B氣體,在一定條件下發生反應:2A(g)+B(g)![]() 2C(g),達到平衡時,C的濃度為0.6 mol/L,則A的轉化率為30%
2C(g),達到平衡時,C的濃度為0.6 mol/L,則A的轉化率為30%
④Mg、Al在相同條件下分別與0.1 mol/L鹽酸反應,反應速率相同
A.①② B.①②③ C.②③④ D.①②③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖為實驗室某濃硫酸試劑瓶標簽上的有關數據,試根據標簽上的有關數據回答下列問題:

(1)該濃硫酸的物質的量濃度為___________________。
(2)用此濃硫酸配制 240mL 1.0 mol·L-l 稀硫酸所需濃硫酸的體積是____________,量取濃硫酸所用的量筒的規格是_________(從下列量筒的規格中選用)
A.10mL B.20mL C.50mL D.100mL
(3)稀釋濃硫酸的操作為_________________________________________________;
(4)容量瓶上標有以下五項中的______________;
A.溫度 B.濃度 C.規格 D.壓強 E.刻度線
(5)配制過程中,下列操作會引起結果偏高的是_______(填序號);
① 未洗滌燒杯、玻璃棒 ② 量取濃硫酸時仰視 ③ 定容時俯視刻度線
④ 容量瓶不干燥,含有少量蒸餾水 ⑤ 溶液未冷卻至室溫就轉移到容量瓶
(6)100 mL 1.0 mol·L-l 稀硫酸與300 mL 1.0 mol·L-l BaCl2溶液混合,所得溶液中H+的物質的量濃度為_______________ (忽略混合時溶液體積的變化)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有下列各組物質:(A) O2和O3; (B) ![]() ;
; 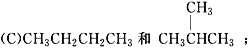
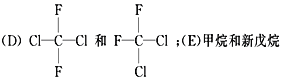
(1)__________組兩物質互為同位素;(2)__________組兩物質互為同素異形體;
(3)__________組兩物質互為同系物;(4)__________組兩物質互為同分異構體;
(5) _________組兩物質互為同一物質。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com