
| A. | 1L0.5mol/L的FeCl3溶液充分水解后,所得Fe(OH)3膠粒的數目為0.5NA | |
| B. | 將1molNH4NO3溶于稀氨水中使溶液呈中性,溶液中NH4+數目為NA | |
| C. | 室溫下,1L pH=1的H2SO4溶液中,由水電離出的H+數目為0.1NA | |
| D. | ag某氣體含分子數為b,c g該氣體在標況下的體積為$\frac{22.4ab}{c{N}_{A}}$L |
分析 A.膠體為多個粒子的集合體;
B.依據電荷守恒解答;
C.依據酸、堿對水的電離產生抑制解答;
D.ag某氣體的分子數為b,則cg氣體中分子個數為$\frac{bc}{a}$,其體積V=$\frac{N}{N{\;}_{A}}$×Vm.
解答 解:A.膠體為多個粒子的集合體,所以1L0.5mol/L的FeCl3溶液充分水解后,所得Fe(OH)3膠粒的數目小于為0.5NA,故A錯誤;
B.將1molNH4NO3溶于稀氨水中使溶液呈中性,則溶液中存在電荷守恒:n(NH4+)+n(H+)=n(OH-)+n(NO3-),則硝酸根離子個數等于銨根離子個數,故B正確;
C.室溫下,1L pH=1的H2SO4溶液中,水的電離受到抑制,溶液中氫離子濃度為0.1mol/L,則由水電離產生的氫離子濃度等于由水電離產生的氫氧根離子濃度為:10-13mol/L,1L pH=1的H2SO4溶液中,由水電離出的H+數目為10-13NA,故C錯誤;
D.ag某氣體的分子數為b,則cg氣體中分子個數為$\frac{bc}{a}$,其在標況下的體積V=$\frac{N}{N{\;}_{A}}$×Vm=$\frac{22.4bc}{aN{\;}_{A}}$,故D錯誤;
故選:B.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大,注意溶液中電荷守恒規律的應用.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 等質量的硫蒸氣和硫固體分別完全燃燒,后者放出的熱量多 | |
| B. | 需要加熱才能發生的反應一定是吸熱反應 | |
| C. | 在101 kPa時,2 g H2完全燃燒生成液態水,放出285.8 kJ熱量,氫氣燃燒的熱化學方程式為:2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ/mol | |
| D. | 稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,濃H2SO4與含1 mol NaOH的溶液混合,放出的熱量大于57.3 kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用鈉可以檢驗某無水酒精中是否含有水 | |
| B. | 140℃時,無水乙醇與濃硫酸共熱可制備乙烯 | |
| C. | 制取乙酸乙酯時,試劑加入的順序是:先加入乙醇,后慢慢加入濃硫酸,最后加入乙酸 | |
| D. | 在蔗糖溶液中加入少量稀硫酸,水浴加熱后,再加入少量新制的氫氧化銅懸濁液,加熱至沸騰,沒有磚紅色沉淀生成,說明蔗糖沒有水解 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
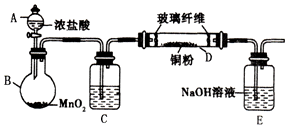 實驗室采用如圖所示的裝置制取氯化銅(部分儀器和夾持裝置已略去).
實驗室采用如圖所示的裝置制取氯化銅(部分儀器和夾持裝置已略去).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 苯與液溴FeBr3作催化劑的條件下發生取代反應,生成溴苯 | |
| B. | 分子式為C5H10Q2,且能與NaHCO3反應的有機物有3種 | |
| C. | 乙醇制備乙烯和乙醇制備乙酸乙酯均為取代反應 | |
| D. | 2-甲基戊烷和4-甲基戊烷互為同分異構體 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
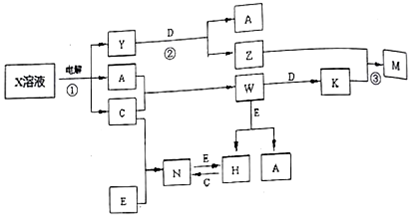
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com