
固定和利用CO2,能有效地利用資源,并減少空氣中的溫室氣體。工業上正在研究利用CO2來生產甲醇燃料的方法,該方法的化學方程式是:
CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g) △H= -49.0 kJ·mol-1
CH3OH(g) + H2O(g) △H= -49.0 kJ·mol-1
某科學實驗將6 mol CO2和8 mol H2充入一容積為2 L的密閉容器中(溫度保持不變),測得H2的物質的量隨時間變化如右圖中實線所示(圖中字母后的數字表示對應的坐標):
回答下列問題:
(1)該反應在 條件下能自發進行(填編號)。
A、高溫 B、低溫 C、任何溫度
(2)該反應在0~8min內CO2的平均反應速率是 mol/(L•min)。
(3)該反應的平衡常數K= 。
(4)僅改變某一條件再進行實驗,測得H2的物質的量隨時間變化如圖中虛線所示。與實線相比,曲線Ⅰ改變的條件可能是 ,曲線Ⅱ改變的條件可能是 。
若實線對應條件下平衡常數為K,曲線Ⅰ對應條件下平衡常數為K1,曲線Ⅱ對應條
件下平衡常數為K2,則K、K1和K2的大小關系是 。
(5)根據化學反應速率與化學平衡理論,聯系化工生產實際,你認為下列說法不正確的是
。
A.化學反應速率理論可指導怎樣在一定時間內快出產品
B.有效碰撞理論可指導怎樣提高原料的轉化率
C.勒夏特列原理可指導怎樣使用有限原料多出產品
D.催化劑的使用是提高產率的有效方法
E.正確利用化學反應速率和化學反應限度都可以提高化工生產的綜合經濟效益
科目:高中化學 來源: 題型:
 (2014?濱州一模)固定和利用CO2,能有效地利用資源,并減少空氣中的溫室氣體.工業上正在研究利用CO2來生產甲醇燃料的方法,該方法的化學方程式是:
(2014?濱州一模)固定和利用CO2,能有效地利用資源,并減少空氣中的溫室氣體.工業上正在研究利用CO2來生產甲醇燃料的方法,該方法的化學方程式是:查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 (2011?閔行區二模)固定和利用CO2,能有效地利用資源,并減少空氣中的溫室氣體.工業上正在研究利用CO2來生產甲醇燃料的方法,該方法的化學方程式是:
(2011?閔行區二模)固定和利用CO2,能有效地利用資源,并減少空氣中的溫室氣體.工業上正在研究利用CO2來生產甲醇燃料的方法,該方法的化學方程式是:| [CH3OH]?[H2O] |
| [CO2]?[H2]3 |
| [CH3OH]?[H2O] |
| [CO2]?[H2]3 |
查看答案和解析>>
科目:高中化學 來源:2011屆遼寧省沈陽二中高三第五次模擬考試(理綜)化學部分 題型:填空題
固定和利用CO2,能有效地利用資源,并減少空氣中的溫室氣體。工業上正在研究利用CO2來生產甲醇燃料的方法,該方法的化學方程式是:
CO2(g) + 3H2(g) CH3OH(g) + H2O(g) △H=" -49.0" kJ·mol-1
CH3OH(g) + H2O(g) △H=" -49.0" kJ·mol-1
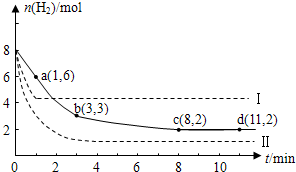
某科學實驗將6 mol CO2和8 mol H2充入一容積為2 L的密閉容器中(溫度保持不變),測得H2的物質的量隨時間變化如右圖中實線所示(圖中字母后的數字表示對應的坐標):
回答下列問題:
(1)該反應在 條件下能自發進行(填編號)。
A、高溫 B、低溫 C、任何溫度
(2)該反應在0~8 min內CO2的平均反應速率是 mol/(L?min)。
(3)該反應的平衡常數K= 。
(4)僅改變某一條件再進行實驗,測得H2的物質的量隨時間變化如圖中虛線所示。與實線相比,曲線Ⅰ改變的條件可能是 ,曲線Ⅱ改變的條件可能是 。
若實線對應條件下平衡常數為K,曲線Ⅰ對應條件下平衡常數為K1,曲線Ⅱ對應條
件下平衡常數為K2,則K、K1和K2的大小關系是 。
(5)根據化學反應速率與化學平衡理論,聯系化工生產實際,你認為下列說法不正確的是
。
A.化學反應速率理論可指導怎樣在一定時間內快出產品
B.有效碰撞理論可指導怎樣提高原料的轉化率
C.勒夏特列原理可指導怎樣使用有限原料多出產品
D.催化劑的使用是提高產率的有效方法
E.正確利用化學反應速率和化學反應限度都可以提高化工生產的綜合經濟效益
查看答案和解析>>
科目:高中化學 來源:2010-2011學年遼寧省高三第五次模擬考試(理綜)化學部分 題型:填空題
固定和利用CO2,能有效地利用資源,并減少空氣中的溫室氣體。工業上正在研究利用CO2來生產甲醇燃料的方法,該方法的化學方程式是:
CO2(g) + 3H2(g) CH3OH(g) + H2O(g)
△H= -49.0 kJ·mol-1
CH3OH(g) + H2O(g)
△H= -49.0 kJ·mol-1
某科學實驗將6 mol CO2和8 mol H2充入一容積為2 L的密閉容器中(溫度保持不變),測得H2的物質的量隨時間變化如右圖中實線所示(圖中字母后的數字表示對應的坐標):

回答下列問題:
(1)該反應在 條件下能自發進行(填編號)。
A、高溫 B、低溫 C、任何溫度
(2)該反應在0~8 min內CO2的平均反應速率是 mol/(L•min)。
(3)該反應的平衡常數K= 。
(4)僅改變某一條件再進行實驗,測得H2的物質的量隨時間變化如圖中虛線所示。與實線相比,曲線Ⅰ改變的條件可能是 ,曲線Ⅱ改變的條件可能是 。
若實線對應條件下平衡常數為K,曲線Ⅰ對應條件下平衡常數為K1,曲線Ⅱ對應條
件下平衡常數為K2,則K、K1和K2的大小關系是 。
(5)根據化學反應速率與化學平衡理論,聯系化工生產實際,你認為下列說法不正確的是
。
A.化學反應速率理論可指導怎樣在一定時間內快出產品
B.有效碰撞理論可指導怎樣提高原料的轉化率
C.勒夏特列原理可指導怎樣使用有限原料多出產品
D.催化劑的使用是提高產率的有效方法
E.正確利用化學反應速率和化學反應限度都可以提高化工生產的綜合經濟效益
查看答案和解析>>
科目:高中化學 來源:2013屆山東省濰坊市高二寒假作業化學(二)試卷 題型:填空題
固定和利用CO2,能有效地利用資源,并減少空氣中的溫室氣體。工業上正在研究利用CO2來生產甲醇燃料的方法,該方法的化學方程式是:CO2(g) + 3H2(g) 
 CH3OH(g)
+H2O(g)
CH3OH(g)
+H2O(g)
△H=-49.0 kJ·mol-1。某科學實驗將6 mol CO2和8 mol H2充入一容積為2 L的密閉容器中(溫度保持不變),測得H2的物質的量隨時間變化如下圖中實線所示(圖中字母后的數字表示對應的坐標)
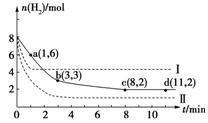
回答下列問題:
(1)該反應在0~8 min內CO2的平均反應速率是 mol/(L•min)。
(2)該反應的平衡常數K= 。
(3)僅改變某一條件再進行實驗,測得H2的物質的量隨時間變化如圖中虛線所示。與實線相比曲線Ⅰ改變的條件可能是 ,曲線Ⅱ改變的條件可能是 。若實線對應條件下平衡常數為K,曲線Ⅰ對應條件下平衡常數為K1,曲線Ⅱ對應條件下平衡常數為K2,則K、K1和K2的大小關系是
(4)根據化學反應速率與化學平衡理論,聯系化工生產實際,你認為下列說法不正確的
A.化學反應速率理論可指導怎樣在一定時間內快出產品
B.有效碰撞理論可指導怎樣提高原料的轉化率
C.勒夏特列原理可指導怎樣使用有限原料多出產品
D.催化劑的使用是提高產率的有效方法
E.正確利用化學反應速率和化學反應限度都可以提高化工生產的綜合經濟效益
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com