
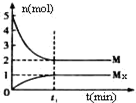
 E是非金屬性最強的元素,M是E的氣態氫化物,在固定體積的密閉容器中,氣體M存在如下關系:xM(g)?Mx(g),反應物和生成物的物質的量隨時間的變化關系如圖.下列說法正確的是( )
E是非金屬性最強的元素,M是E的氣態氫化物,在固定體積的密閉容器中,氣體M存在如下關系:xM(g)?Mx(g),反應物和生成物的物質的量隨時間的變化關系如圖.下列說法正確的是( )| A、該反應的化學方程式是2HF?(HF)2 | ||
B、t1時刻,保持溫度不變,再充入1molM,重新達到平衡時,
| ||
| C、平衡時混合氣體的平均摩爾質量是33.3 | ||
| D、M的沸點比同主族下一周期元素的氣態氫化物沸點低 |


 寒假大串聯黃山書社系列答案
寒假大串聯黃山書社系列答案 寒假創新型自主學習第三學期寒假銜接系列答案
寒假創新型自主學習第三學期寒假銜接系列答案科目:高中化學 來源: 題型:
| HCl |
| NH3?H2O |
| △ |

查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、離子半徑:Al3+<Mg2+<F- |
| B、酸性:H2SiO3<H3PO4<H2SO4<HClO4 |
| C、熱穩定性:HI>HBr>HCl>HF |
| D、堿性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、反應過程中,氣體的密度始終不變 |
| B、當容器中氣體壓強不變時,反應達到平衡 |
| C、升高溫度,v(正)增大、v(逆)減小,平衡向正反應方向移動 |
| D、當2v正(X)=v逆(Z)時,反應達平衡 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、v(SO3)=4 mol?L-1?min-1 |
| B、v(O2)=2 mol?L-1?min-1 |
| C、v(SO2)=5 mol?L-1?min-1 |
| D、v(SO2)=0.1 mol?L-1?S-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| ||
| △ |
| 實驗編號 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | y | 9 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com