
已知25 ℃時弱電解質的電離平衡常數:
Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13。
(1)將20 mL 0.10 mol·L-1 CH3COOH溶液和20 mL 0.10 mol·L-1的HSCN溶液分別與0.10 mol·L-1的NaHCO3溶液反應,實驗測得產生CO2氣體體積(V)與時間t的關系如圖所示。

反應開始時,兩種溶液產生CO2的速率明顯不同的原因是________;反應結束后所得溶液中c(SCN-)________c(CH3COO-)(填“>”、“=”或<)。
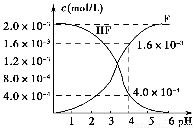
(2)2.0×10-3 mol·L-1的氫氟酸水溶液中,調節溶液pH(忽略調節時體積變化),測得平衡體系中c(F-)、c(HF)與溶液pH的關系如圖所示。則25 ℃時,HF電離平衡常數為Ka(HF)=________(列式求值)。
(3)難溶物質CaF2溶度積常數為Ksp=1.5×10-10,將4.0×10-3 mol·L-1 HF溶液與4.0×10-4 mol·L-1的CaCl2溶液等體積混合,調節溶液pH=4(忽略調節時溶液體積變化),試分析混合后是否有沉淀生成?________(填“有”或“沒有”),簡述理由:____________________________________________。
(1)Ka(HSCN)>Ka(CH3COOH),溶液中c(H+):HSCN>CH3COOH,
c(H+)大反應速率快 >
(2)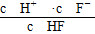 =
=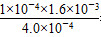 =4×10-4
=4×10-4
(3)有 溶液中離子積Qc=c(Ca2+)·c2(F-)=5.12×10-10>Ksp(CaF2)=1.5×10-10
【解析】 (1)由Ka(CH3COOH)、Ka(HSCN)的數據知,相同物質的量濃度溶液HSCN的酸性比CH3COOH強,HSCN溶液中c(H+)大,所以反應開始時HSCN溶液與NaHCO3溶液反應的速率快。反應結束后所得兩溶液分別為CH3COONa溶液和NaSCN溶液,由于HSCN的酸性比CH3COOH強,則SCN-的水解程度比CH3COO-弱,所以c(SCN-)>c(CH3COO-)。(2)當pH=4時,由圖像可知,c(F-)=1.6×10-3 mol·L-1,c(HF)=4.0×10-4mol·L-1,c(H+)=1×10-4mol·L-1,代入Ka(HF)=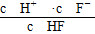 即可。(3)當pH=4時,溶液中的c(F-)=1.6×10-3 mol·L-1,溶液中c(Ca2+)=2.0×10-4 mol·L-1,溶液中離子積Qc=c(Ca2+)·c2(F-)=5.12×10-10>Ksp(CaF2)=1.5×10-10,故有沉淀產生。
即可。(3)當pH=4時,溶液中的c(F-)=1.6×10-3 mol·L-1,溶液中c(Ca2+)=2.0×10-4 mol·L-1,溶液中離子積Qc=c(Ca2+)·c2(F-)=5.12×10-10>Ksp(CaF2)=1.5×10-10,故有沉淀產生。


 孟建平錯題本系列答案
孟建平錯題本系列答案 超能學典應用題題卡系列答案
超能學典應用題題卡系列答案科目:高中化學 來源:2013-2014學年高考化學二輪提分訓練 專題1物質組成性質分類及化學用語練習卷(解析版) 題型:選擇題
下列說法不正確的是( )。
A.明礬[KAl(SO4)2·12H2O]在水中能形成Al(OH)3膠體,可用作凈水劑
B.江河入海口三角洲的形成通常與膠體的性質有關
C.淀粉溶液具有丁達爾效應
D.向煮沸的1 mol·L-1 NaOH溶液中滴加FeCl3飽和溶液制備Fe(OH)3膠體
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 高考模擬演練1練習卷(解析版) 題型:選擇題
下列實驗操作能夠達到實驗目的的是( )。

A.用激光筆鑒別淀粉溶液和蔗糖溶液
B.實驗室采用上圖所示裝置收集SO2
C.除去NaHCO3溶液中的Na2CO3,可加入Ca(OH)2溶液后過濾
D.配制一定物質的量濃度溶液時,容量瓶用蒸餾水洗滌后再用待裝溶液潤洗
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第8講電化學練習卷(解析版) 題型:填空題
電解是最強有力的氧化還原手段,在化工生產中有著重要的應用。請回答下列問題:
(1)以銅為陽極,以石墨為陰極,用NaCl溶液作電解液進行電解,得到半導體材料Cu2O和一種清潔能源,則陽極反應式為________,陰極反應式為________。
(2)某同學設計如圖所示的裝置探究金屬的腐蝕情況。下列判斷合理的是
___________________________________________________(填序號)。

a.②區銅片上有氣泡產生
b.③區鐵片的電極反應式為2Cl--2e-=Cl2↑
c.最先觀察到變成紅色的區域是②區
d.②區和④區中銅片的質量均不發生變化
(3)最新研究發現,用隔膜電解法處理高濃度乙醛廢水的工藝具有流程簡單、能耗較低等優點,其原理是使乙醛分別在陰、陽極發生反應生成乙醇和乙酸,總反應式為2CH3CHO+H2O CH3CH2OH+CH3COOH
CH3CH2OH+CH3COOH

實驗室中,以一定濃度的乙醛-Na2SO4溶液為電解質溶液,模擬乙醛廢水的處理過程,其裝置如圖所示。
①若以甲烷堿性燃料電池為直流電源,則燃料電池中b極應通入________(填化學式),電極反應式為________。電解過程中,陰極區Na2SO4的物質的量________(填“增大”、“減小”或“不變”)。
②在實際工藝處理中,陰極區乙醛的去除率可達60%。若在兩極區分別注入1 m3乙醛含量為3 000 mg/L的廢水,可得到乙醇________kg(計算結果保留小數點后一位)。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第8講電化學練習卷(解析版) 題型:選擇題
下列與金屬腐蝕有關的說法,正確的是( )。

A.圖1中,插入海水中的鐵棒,越靠近底端腐蝕越嚴重
B.圖2中,往燒杯中滴加幾滴KSCN溶液,溶液變血紅色
C.圖3中,燃氣灶的中心部位容易生銹,主要是由于高溫下鐵發生化學腐蝕
D.圖4中,用犧牲鎂塊的方法來防止地下鋼鐵管道的腐蝕,鎂塊相當于原電池的正極
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第7講水溶液中的離子平衡練習卷(解析版) 題型:選擇題
25 ℃時,用濃度為0.100 0 mol·L-1的NaOH溶液滴定20.00 mL濃度均為0.100 0 mol·L-1的三種酸HX、HY、HZ,滴定曲線如圖所示。下列說法正確的是( )。

A.在相同溫度下,同濃度的三種酸溶液的導電能力順序:HZ<HY<HX
B.根據滴定曲線,可得Ka(HY)≈10-5
C.將上述HX、HY溶液等體積混合后,用NaOH溶液滴定至HX恰好完全反應時:c(X-)>c(Y-)>c(OH-)>c(H+)
D.HY與HZ混合,達到平衡時c(H+)=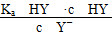 +c(Z-)+c(OH-)
+c(Z-)+c(OH-)
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第6講化學反應速率和化學平衡練習卷(解析版) 題型:填空題
(1)在100 ℃恒溫條件下將0.100 mol的N2O4充入體積為1 L的真空密閉容器中,發生反應:N2O4(g) 2NO2(g) ΔH>0。隔一定時間對該容器內的物質進行分析,得到如下數據:
2NO2(g) ΔH>0。隔一定時間對該容器內的物質進行分析,得到如下數據:
t/s c/(mol·L-1) | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4)/(mol·L-1) | 0.100 | a | 0.5b | 0.4b |
|
|
c(NO2)/(mol·L-1) | 0 | 0.060 | b | c1 | c2 | c3 |
請回答下列問題:
①表中a=________,在0~20 s內N2O4的平均反應速率為_______mol·(L·s)-1。
②已知100 ℃時該反應的平衡常數為0.36,則表中b、c1、c2的大小關系為________,c3=________mol·L-1,達到平衡時N2O4的轉化率為________________________________。
(2)室溫下,把SiO2細粉放入蒸餾水中,不斷攪拌,能形成H4SiO4溶液,反應原理如下:
SiO2(s)+2H2O(l)??H4SiO4(aq) ΔH
①寫出該反應的化學平衡常數K的表達式:____________________________。
②實際上,在地球的深處,由于壓強很大,固體、液體都會受到影響。在一定溫度下,在10 000 m以下的地球深處,上述反應的方向是________(填“正方向”、“逆方向”或“不移動”),理由是_______________________________。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第5講化學反應與能量練習卷(解析版) 題型:填空題
為保護環境并緩解能源危機,專家提出利用太陽能促使燃燒循環使用的構想,轉化關系如圖所示。

已知:
(1)過程Ⅰ可用如下反應表示:①2CO2 2CO+O2
2CO+O2
②2H2O(g) 2H2+O2
2H2+O2
③2N2+6H2O 4NH3+3O2
4NH3+3O2
④2CO2+4H2O 2CH3OH+3O2
2CH3OH+3O2
⑤2CO+4H2O ________+3O2。
________+3O2。
(2)25 ℃時,a g CH4完全燃燒釋放出b kJ熱量。下列說法不正確的是( )。
A.過程Ⅰ是將太陽能轉化成化學能
B.反應⑤的另一種產物為CH4
C.ΔH1=-ΔH2
D.表示甲烷燃燒熱的熱化學反應方程式為CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-16b kJ·mol-1
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第2講化學常用計量練習卷(解析版) 題型:選擇題
如圖所示,兩個連通容器用活塞分開,左右兩室體積相同,左室充入一定量NO,右室充入一定量O2,且恰好使兩容器內氣體密度相同。打開活塞,使NO與O2充分反應,下列判斷正確的是(不考慮NO2轉化為N2O4)

A.開始時左右兩室中的分子數相同
B.反應前后左室的壓強相同
C.反應后容器內的密度與反應前的相同
D.反應后容器內無O2存在
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com