
某學生對SO2與漂粉精的反應進行實驗探究:
操作 | 現象 |
取適量漂粉精固體,加入100mL水 | 部分固體溶解,溶液略有顏色 |
過濾,測漂粉精溶液的pH | pH試紙先變藍,后褪色 |
| 液面上方出現白霧; 稍后,出現渾濁,溶液變為黃綠色; 稍后,產生大量白色沉淀,黃綠色褪去 |
(1)寫出C12和Ca(OH)2制取漂粉精的化學方程式?????????????????????????????? ;???
(2)向水中持續通入SO2,未觀察到白霧。推測現象i的白霧由HCl小液滴形成,進行如下實驗:
a.用濕潤的碘化鉀淀粉試紙檢驗白霧,無變化;
b.用酸化的AgNO3溶液檢驗白霧,產生白色沉淀。
①實驗a目的是???????????????????????????????????????? ;
②由實驗a、b不能判斷白霧中含有HC1,理由是?????????????????????????????????????? ;
(3)將A瓶中混合物過濾、洗滌,得到沉淀X
①向沉淀X中加入稀HC1,無明顯變化。取上層清液,加入BaC12溶液,產生白色沉淀。則沉淀X中含有的物質是???????? ;
②用離子方程式解釋現象iii中黃綠色褪去的原因:??????????????????????????????????? 。
(4)測定漂粉精有效成分的質量分數。稱取2.000 g漂粉精于錐形瓶中,加水溶解,調節溶液的pH,以淀粉為指示劑,用0.2000 mol·L-1 KI溶液進行滴定,溶液出現穩定淺藍色時為滴定終點。反應原理為:3C1O-+ I- == 3C1-+ IO3-
IO3- + 5I- + 3H2O == 6OH-+ 3I2
實驗測得數據如下表所示。
滴定次數 | 1 | 2 | 3 |
KI溶液體積/mL | 19.98 | 20.02 | 20.00 |
該漂白粉中有效成分的質量分數為????????????????????????? 。
(1)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
(2)①驗證Cl2存在②與硝酸酸化的AgNO3產生的白色沉淀也可能是Ag2SO4或Ag2SO3
(3)①CaSO4? ②SO2+Cl2+2H2O=4H++SO42-+2Cl-? (4)42.90%(4分,數據對且符合有效數字要求)
【解析】
試題分析:(1) Cl2和Ca(OH)2生成氯化鈣、次氯酸鈣與水;(2)①反應中生成Cl2,用濕潤的碘化鉀淀粉試紙檢驗白霧中是否Cl2,排除Cl2干擾;②白霧中含有SO2,可以被硝酸氧化為硫酸,故SO2可以使酸化的AgNO3溶液產生白色沉淀;(3)①A瓶中混合物過濾、洗滌得沉淀X,向X中加入稀HC1,無明顯變化,不含CaSO3。取上層清液,加入BaC12溶液,產生白色沉淀,說明有SO42-。故X中含有的物質是CaSO4;②iii中黃綠色褪去的原因是SO2還原了Cl2的原因:SO2+Cl2+2H2O=4H++SO42-+2Cl-;(4)根據反應原理可知3~2KI,平均消耗KI為20.00mL,為20.00×10-3×0.2000mol=4.000 mol,即漂白粉含6.000×10-3mol Ca(C1O)2,即0.8580g,故該漂白粉中有效成分的質量分數為42.90%。
考點:實驗現象的解釋與含量計算。


 千里馬走向假期期末仿真試卷寒假系列答案
千里馬走向假期期末仿真試卷寒假系列答案科目:高中化學 來源: 題型:閱讀理解
| 操作 | 現象 |
| 取4g漂粉精固體,加入100mL水 | 部分固體溶解,溶液略有顏色 |
| 過濾,測漂粉精溶液的pH | pH試紙先變藍(約為12),后褪色 |
 |
i.液面上方出現白霧; ⅱ.稍后,出現渾濁,溶液變為黃綠色; ⅲ.稍后,產生大量白色沉淀,黃綠色褪去 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 操作 | 現象 |
| 取4g漂粉精固體,加入100mL水 | 部分固體溶解,溶液略有顏色 |
| 過濾,測漂粉精溶液的pH | pH試紙先變藍(約為12),后褪色 |
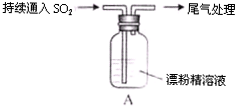 |
液面上方出現白霧; 稍后,出現渾濁,溶液變為黃綠色; 稍后,產生大量白色沉淀,黃綠色褪去 |
查看答案和解析>>
科目:高中化學 來源: 題型:
某學生對SO2與漂粉精的反應進行實驗探究:
| 操作 | 現象 |
| 取4g漂粉精固體,加入100mL水 | 部分固體溶解,溶液略有顏色 |
| 過濾,測漂粉精溶液的pH | pH試紙先變藍(約為12),后褪色 |
|
| i. 液面上方出現白霧; ii. 稍后,出現渾濁,溶液變為黃綠色; iii. 稍后,產生大量白色沉淀,黃綠色褪去 |
(1)Cl2和Ca(OH)2制取漂粉精的化學方程是 。
(2)pH試紙顏色的變化說明漂粉精溶液具有的性質是 。
(3)向水中持續通入SO2,未觀察到白霧。推測現象i的白霧由HCl小液滴形成,進行如下實驗:
a.用濕潤的碘化鉀淀粉試紙檢驗白霧,無變化;
b.用酸化的AgNO3溶液檢驗白霧,產生白色沉淀。
① 實驗a目的是 。
②由實驗a、b不能判斷白霧中含有HC1,理由是 。
(4)現象ii中溶液變為黃綠色的可能原因:隨溶液酸性的增強,漂粉精的有效成分和C1-發生反應。通過進一步實驗確認了這種可能性,其實驗方案是 。
(5)將A瓶中混合物過濾、洗滌,得到沉淀X
①向沉淀X中加入稀HC1,無明顯變化。取上層清液,加入BaC12溶液,產生白色沉淀。則沉淀X中含有的物質是 。
②用離子方程式解釋現象iii中黃綠色褪去的原因: 。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪專題沖刺第10講 非金屬及其化合物練習卷(解析版) 題型:實驗題
某學生對SO2與漂粉精的反應進行實驗探究:
操作 | 現象 |
取4 g漂粉精固體,加入100 mL水 | 部分固體溶解,溶液略有顏色 |
過濾,測漂粉精溶液的pH | pH試紙先變藍(約為12),后褪色 |
| i.液面上方出現白霧; ii.稍后,出現渾濁,溶液變為黃綠色;iii.稍后,產生大量白色沉淀,黃綠色褪去 |
(1)Cl2和Ca(OH)2制取漂粉精的化學方程式是 ________________________________。
(2)pH試紙顏色的變化說明漂粉精溶液具有的性質是__________________________。
(3)向水中持續通入SO2,未觀察到白霧。推測現象i的白霧由HCl小液滴形成。進行如下實驗:
a.用濕潤的碘化鉀淀粉試紙檢驗白霧,無變化;
b.用酸化的AgNO3溶液檢驗白霧,產生白色沉淀。
① 實驗a的目的是______________________________________________________。
②由實驗a、b不能判斷白霧中含有HCl,理由是________________________________。
(4)現象ii中溶液變為黃綠色的可能原因:隨溶液酸性的增強,漂粉精的有效成分和Cl-發生反應。通過進一步實驗確認了這種可能性,其實驗方案是_____________________。
(5)將A瓶中混合物過濾、洗滌,得到沉淀X
①向沉淀X中加入稀HCl,無明顯變化。取上層清液,加入BaCl2溶液,產生白色沉淀。則沉淀X中含有的物質是________。
②用離子方程式解釋現象iii中黃綠色褪去的原因:_____________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源:2013年全國普通高等學校招生統一考試理科綜合能力測試化學(北京卷解析版) 題型:實驗題
某學生對SO2與漂粉精的反應進行實驗探究:
|
操作 |
現象 |
|
取4g漂粉精固體,加入100mL水 |
部分固體溶解,溶液略有顏色 |
|
過濾,測漂粉精溶液的pH |
pH試紙先變藍(約為12),后褪色 |
|
|
液面上方出現白霧; 稍后,出現渾濁,溶液變為黃綠色; 稍后,產生大量白色沉淀,黃綠色褪去 |
(1)C12和Ca(OH)2制取漂粉精的化學方程是 。
(2)pH試紙顏色的變化說明漂粉精溶液具有的性質是 。
(3)向水中持續通入SO2,未觀察到白霧。推測現象i的白霧由HC1小液滴形成,進行如下實驗:
a.用濕潤的碘化鉀淀粉試紙檢驗白霧,無變化;
b.用酸化的AgNO3溶液檢驗白霧,產生白色沉淀。
① 實驗a目的是 。
②由實驗a、b不能判斷白霧中含有HC1,理由是 。
(4)現象ii中溶液變為黃綠色的可能原因:隨溶液酸性的增強,漂粉精的有效成分和C1-發生反應。通過進一步實驗確認了這種可能性,其實驗方案是 。
(5)將A瓶中混合物過濾、洗滌,得到沉淀X
①向沉淀X中加入稀HC1,無明顯變化。取上層清液,加入BaC12溶液,產生白色沉淀。則沉淀X中含有的物質是 。
②用離子方程式解釋現象iii中黃綠色褪去的原因: 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com