
【題目】含有a mol FeBr2的溶液中,通入 x mol Cl2。下列各項為通Cl2過程中,溶液內發生反應的離子方程式,其中不正確的是( )
A.x=0.4a,2Fe2++Cl2===2Fe3++2Cl-
B.x=0.6a,2Br-+Cl2===Br2+2Cl-
C.x=a,2Fe2++2Br-+2Cl2===Br2+2Fe3++4Cl-
D.x=1.5a,2Fe2++4Br-+3Cl2===2Br2+2Fe3++6Cl-
科目:高中化學 來源: 題型:
【題目】下列各組離子中,能在溶液中大量共存的一組是
A.Mg2+、Al3+、Cl-、OH-
B.Na+、Ba2+、OH-、SO42—
C.K+、Na+、NO3—、HCO3—
D.K+、NH4+、CO32—、OH-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從結構的角度可以幫助我們更好的理解有機物的化學性質。
(1) 乙炔是一種重要的化工原料,將乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2紅棕色沉淀。Cu+基態核外電子排布式為____________。乙炔與氫氰酸反應可得丙烯腈H2C=CH-C≡N。丙烯腈分子中碳原子軌道雜化類型是____________。[Cu(NH3)2]Cl的氨水溶液在空氣中放置迅速由無色變為深藍色,寫出該過程的離子方程式______________________。
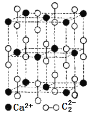
(2)實驗室制乙炔使用的電石主要含有碳化鈣,寫出碳化鈣的電子式______________, CaC2晶體的晶胞結構與NaCl晶體的相似(如圖所示),但CaC2晶體中有啞鈴形![]() 的存在,使晶胞沿一個方向拉長。CaC2晶體中1個Ca2+周圍距離最近的
的存在,使晶胞沿一個方向拉長。CaC2晶體中1個Ca2+周圍距離最近的![]() 數目為____________。已知CaC2晶體的密度為2.22g/cm3,該晶胞的體積為____________cm3
數目為____________。已知CaC2晶體的密度為2.22g/cm3,該晶胞的體積為____________cm3
(3) 甲醇催化氧化可得到甲醛,甲醛分子中的鍵角大約為____________,甲醇的沸點比甲醛的高,其主要原因是_____________________。
(4)已知苯酚具有弱酸性,其Ka=1.1 ×10-10;水楊酸第一級電離形成的離子為![]() 判斷相同溫度下電離平衡常數Ka2(水楊酸)_______Ka(苯酚)(填“>”或“<”),其原因是___。
判斷相同溫度下電離平衡常數Ka2(水楊酸)_______Ka(苯酚)(填“>”或“<”),其原因是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗小組依據反應AsO43-+2I-+2H+![]() AsO33-+I2+H2O設計如圖原電池,探究pH對AsO43-氧化性的影響。測得電壓與pH的關系如圖。下列有關敘述錯誤的是
AsO33-+I2+H2O設計如圖原電池,探究pH對AsO43-氧化性的影響。測得電壓與pH的關系如圖。下列有關敘述錯誤的是
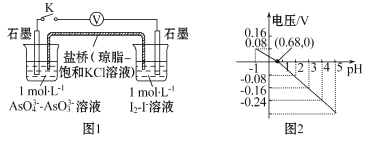
A.調節pH可以改變反應的方向
B.pH=0.68時,反應處于平衡狀態
C.pH=5時, 負極電極反應式為2I--2e -= I2
D.pH>0.68時,氧化性I2>AsO43-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】回答下列問題:
(1)已知下列反應:SO2(g)+2OH (aq) ===SO32 (aq)+H2O(l) ΔH1
ClO (aq)+SO32 (aq) ==SO42 (aq)+Cl (aq) ΔH2 CaSO4(s) ==Ca2+(aq)+SO42(aq) ΔH3
則反應SO2(g)+ Ca2+(aq)+ ClO (aq) +2OH (aq) === CaSO4(s) +H2O(l) +Cl (aq)的ΔH=______。(用ΔH1 ΔH2ΔH3表示)
(2)工業上用H2和Cl2反應制HCl,各鍵能數據為:H﹣H:436kJ/mol,Cl﹣Cl:243kJ/mol,H﹣Cl:431kJ/mol.該反應的熱化學方程式是 。
(3)合成氣(CO和H2為主的混合氣體)不但是重要的燃料也是重要的化工原料,制備合成氣的方法有多種,用甲烷制備合成氣的反應為:
①2CH4(g)+O2(g)═2CO(g)+4H2(g);△H1=﹣72kJ·mol﹣1
②CH4(g)+H2O(g)═CO(g)+3H2(g);△H2=+216kJ·mol﹣1
氫氣與氧氣反應生成水蒸氣的熱化學方程式為 。
現有1mol由H2O(g)與O2組成的混合氣,且O2的體積分數為x,將此混合氣與足量CH4充分反應.若x=0.2時,反應①放出的能量為 kJ;若x= 時,反應①與②放出(或吸收)的總能量為0。
(4) 一定條件,在水溶液中1 mol Cl-和1 mol ClOx-(x=1,2,3,4)的能量(KJ)相對大小如圖所示
。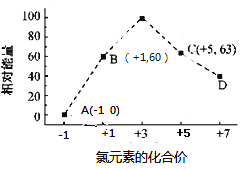
①D是 (填離子符號)。
②B→A+C反應的熱化學方程式為 (用離子符號表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA表示阿伏加德羅常數的值。下列敘述正確的是( )
A.標準狀況下,22.4L CHCl3含氯原子數為3NA
B.100mL 1 mol·L-1醋酸溶液中的氫原子數為0.4NA
C.常溫常壓下,11.2g乙烯中共用電子對數為2.4NA
D.6.4 g CaC2晶體中所含的離子總數為0.3NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】

①配制一定物質的量濃度的硬脂酸的苯溶液;
②測定從膠頭滴管滴出的每滴液體的體積;
③測定在水槽水面上形成硬脂酸單分子膜所需硬脂酸苯溶液的滴數,(如上圖所示)用膠頭滴管
吸取硬脂酸的苯溶液,垂直往水面中滴一滴,待苯在水面上全部揮發,硬脂酸分子在水面擴散至看不到油珠時,再滴第二滴,如此逐滴滴下,直到整個水面形成單個分子厚的硬脂酸分子所形成的膜為止(該單分子膜分子是緊密排列的,此時如再滴入硬脂酸溶液,該溶液在水面上不再擴散);
④測量水槽中水的表面積;
⑤計算求得阿伏加德羅常數。
(1)在第一步實驗中,稱取一定質量的硬脂酸后,配制溶液所需的玻璃儀器主要有 、 、 。
(2)第二步實驗,測定從膠頭滴管滴出的每滴液體的體積,常用方法是
(3)若硬脂酸苯溶液的濃度為c molL-1,測得膠頭滴管滴出的每滴溶液的體積為V mL,水面上形成硬脂酸單分子膜時滴下的硬脂酸溶液的滴數為d,水槽中水的表面積為S cm2,每個硬脂酸分子的截面積為A cm2。求阿伏加德羅常數NA(用c、V、d、S、A的代數式表示): 。
(4)若水中含有少量氫氧化鈉溶液,則會對測定的NA值有何影響? (選填“偏大”、“偏小”或“無影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,飽和NaClO溶液的pH約為11。某消毒液的主要成分為NaClO,潔廁靈主要成分為HCl。下列解釋相關事實的離子方程式中不合理的是
A.該消毒液加白醋生成HClO,可增強消毒能力:H++ClO-=HClO
B.該消毒液可用NaOH溶液吸收Cl2制備:Cl2+2OH-=ClO-+Cl-+H2O
C.常溫下,該消毒液的pH≈11,是因為:ClO-+H2O![]() HClO+OH-
HClO+OH-
D.該消毒液與潔廁靈混用會引起中毒:2H++Cl-+ClO-=Cl2↑+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素A、B、C都是短周期元素,A元素原子的2p軌道上只有兩個未成對電子,B的3p軌道上有空軌道,A、B同主族,B、C同周期,C是本周期中電負性最大的。請回答:
(1)A原子的核外電子排布的軌道表示式________,B原子的核外電子排布式______________________,C原子的價電子排布式________。
(2)A、B、C的氣態氫化物的化學式分別是________,其中最不穩定的是________。
(3)它們的最高價氧化物的水化物中,酸性最強的是________。
(4)AC4的化學式________,電子式________,結構式________,中心原子A的雜化方式________雜化,是________(填“極性”或“非極性”)分子。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com