
用右圖裝置(夾持、加熱裝置已略)進行實驗,有②中現象,不能證實①中反應發生的是( )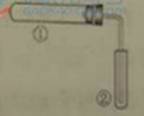
| ①中實驗 | ②中現象 | |
| A | 鐵粉與水蒸氣加熱 | 肥皂水冒泡 |
| B | 加熱NH4Cl和Ca(OH)2混合物 | 酚酞溶液變紅 |
| C | NaHCO3 | 澄清石灰水變渾濁 |
| D | 石蠟油在碎瓷片上受熱分解 | Br2的CCl4溶液褪色 |
科目:高中化學 來源: 題型:
A是一種有機合成中間體,其結構簡式為
A的合成路線如下圖,其中B~H分別代表一種有機物。

請回答下列問題:
(1)A中碳原子的雜化軌道類型有 ① ;A的名稱(系統命名)是 ② ;第⑧步反應的類型是 ③ 。
(2)第①步反應的化學方程式是
(3)C物質與CH2=C(CH3)COOH按物質的量之式1:1反應,其產物經加聚得到 可作隱形眼鏡的鏡片材料I。I的結構簡式是
(4)第⑥步反應的化學方程式是
(5)寫出含有六元環,且一氯代物只有兩種(不考慮立體異構)的A的同分異構體的結構簡式: 。
查看答案和解析>>
科目:高中化學 來源: 題型:
合成氨是人類科學技術上的一項重大突破,其反應原理為:
N2(g)+3H2(g) 2NH3(g) ∆H=—92.4kJ•mol‾1
2NH3(g) ∆H=—92.4kJ•mol‾1
一種工業合成氨的簡易流程圖如下:

(1)天然氣中的H2S雜質常用常用氨水吸收,產物為NH4HS。一定條件下向NH4HS溶液中通入空氣,得到單質硫并使吸收液再生,寫出再生反應的化學方程式: 。
(2)步驟II中制氯氣原理如下:
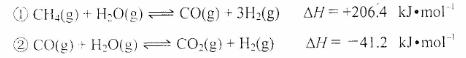
對于反應①,一定可以提高平衡體系中H2百分含量,又能加快反應速率的是 。
a.升高溫度 b.增大水蒸氣濃度 c.加入催化劑 d.降低壓強
利用反應②,將CO進一步轉化,可提高H2產量。若1mol CO和H2的混合氣體(CO的體積分數為20%)與H2O反應,得到1.18mol CO、CO2和H2的混合氣體,則CO轉化率為 。
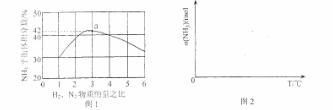
(3)圖1表示500℃、60.0MPa條件下,原料氣投料比與平衡時NH3體積分數的關系。根據圖中a點數據計算N2的平衡體積分數: 。
(4)依據溫度對合成氨反應的影響,在圖2坐標系中,畫出一定條件下的密閉容器內,從通入原料氣開始,隨溫度不斷升高,NH3物質的量變化的曲線示意圖。
(5)上述流程圖中,使合成氨放出的熱量得到充分利用的主要步驟是(填序號) ,簡述本流程中提高合成氨原料總轉化率的方法: 。
查看答案和解析>>
科目:高中化學 來源: 題型:
下列離子方程式錯誤的是
A.向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++ SO42 - =BaS04↓+2H2O
B.酸性介質中KMnO4氧化 H2O2:2MnO4- +5H2O2+6H+ = 2Mn2++5O2↑+ 8H2O
C.等物質的量的MgCl2、Ba(OH)2 和 HC1 溶液混合:Mg2++2OH-= Mg(OH)2↓
D.鉛酸蓄電池充電時的正極反應:PbSO4 + 2H2O-2e- = PbO2+4H++SO42 -
查看答案和解析>>
科目:高中化學 來源: 題型:
用FeCl3酸性溶液脫除H2S后的廢液,通過控制電壓電解得以再生。某同學使用石墨電極,在不同電壓(x)下電解pH=1的0.1mol/LFeCl2溶液,研究廢液再生機理。記錄如下(a、b、c代表電壓值:)

(1)用KSCN溶液檢驗出Fe3+的現象是_______。
(2)I中,Fe2+產生的原因可能是Cl-在陽極放電,生成的Cl2將Fe2+氧化。寫出有關反應的方程式__________________________。
(3)由II推測,Fe3+產生的原因還可能是Fe2+在陽極放電,原因是Fe2+具有_____性。
(4)II中雖未檢測出Cl2,但Cl-在陽極是否放電仍需進一步驗證。電解pH=1的NaCl溶液做對照實驗,記錄如下:
| 序號 | 電壓/V | 陽極現象 | 檢驗陽極產物 |
| IV | a>x≥c | 無明顯變化 | 有Cl2 |
| V | c>x≥b | 無明顯變化 | 無Cl2 |
①NaCl溶液的濃度是________mol/L。
②IV中檢測Cl2的實驗方法:____________________。
③與II對比,得出的結論(寫出兩點):___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
答案 (1)③④⑤⑥⑦⑧⑨ (2)B>A>C
解析 (1)元素原子得電子能力的強弱與元素氫化物的溶解性無關,所以①不符合題意;氫化物的酸性強弱和元素原子得電子能力大小沒有固定的對應關系,所以②也不符合題意,其他均符合題意。(2)由金屬B的最高價氧化物的水化物的堿性比A的最高價氧化物的水化物的堿性強,可判斷失電子能力B>A;又根據A與C形成原電池,C作正極,可判斷失電子能力A>C,故三種金屬元素的原子失電子能力B>A>C。
查看答案和解析>>
科目:高中化學 來源: 題型:
已知33As、35Br位于同一周期。下列關系正確的是 ( )
A.原子半徑:As>Cl>P
B.熱穩定性:HCl>AsH3>HBr
C.還原性:As3->S2->Cl-
D.酸性:H3AsO4>H2SO4>H3PO4
查看答案和解析>>
科目:高中化學 來源: 題型:
(I)X、Y、Z、A、L、E六種短周期主族元素的原子序數依次增大,其中X、E的單質在常溫下呈氣態,E在常溫下是黃綠色氣體;Y的原子的最外層電子數是其電子層數的2倍,Z在同周期的主族元素中原子半徑最大,A是地殼中含量最多的金屬元素,L的單質晶體熔點高、硬度大,是一種重要的半導體材料。
用化學用語回答下列問題:
(1)L的元素符號為 ;A在元素周期表中的位置為
(2)Y、L、E的最高價含氧酸的酸性由弱到強的順序是
(3)Y的最高價氧化物的電子式為 。
(II)下列物質A~F是我們熟悉的單質或化合物,其中A、E均為(I)中元素形成的單質,B是常見的金屬,且B的合金用量最大;在適當的條件下,它們之間可以發生如下圖所示的轉化。
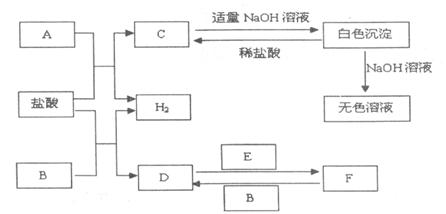
試回答下列問題:
(1)B的化學式是 ;
(2)反應F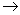 D的化學方程式 。
D的化學方程式 。
(3)檢驗F中金屬陽離子的常用方法是 。
(4)寫出C與過量氨水反應的離子方程式是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com