
【題目】實驗室通常用氧化劑+濃鹽酸![]() 金屬氯化物+水+氯氣的原理制取少量Cl2。現將一定質量的NaClO放入100 mL 10.00 mol·L-1的濃鹽酸中,生成的Cl2在標準狀況下的體積為1.12 L。試計算(反應前后溶液的體積變化忽略不計):
金屬氯化物+水+氯氣的原理制取少量Cl2。現將一定質量的NaClO放入100 mL 10.00 mol·L-1的濃鹽酸中,生成的Cl2在標準狀況下的體積為1.12 L。試計算(反應前后溶液的體積變化忽略不計):
(1)反應過程中,被氧化的HCl的物質的量為____mol。
(2)反應后溶液中HCl的物質的量濃度為____mol·L-1。
科目:高中化學 來源: 題型:
【題目】工業上用鋁土礦(主要成分為Al2O3,含Fe2O3等雜質)為原料冶煉鋁的工藝流程如下:

對上述流程中的判斷正確的是
A. 試劑X為稀硫酸
B. 結合質子( H+)的能力由強到弱的順序是:AlO2—> OH— >CO32—
C. 反應II中生成Al(OH)3的反應為:CO2+AlO2- +2H2O =Al(OH)3↓+HCO3-
D. Al2O3熔點很高,工業上還可采用電解熔融AlCl3冶煉Al
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,兩圓圈相交的陰影部分表示圓圈內物質相互發生的反應。鈉及其氧化物的物質的量 均為0.1 mol,水的質量為100 g。下列說法正確的是

A.甲、乙、丙都屬于氧化還原反應
B.甲反應的離子方程式為Na+2H2O![]() Na++2OH-+H2↑
Na++2OH-+H2↑
C.丙充分反應,能產生0.05 mol O2,轉移電子0.1 mol
D.甲、乙、丙充分反應后所得溶液的質量分數分別為w1、w2、w3,則2w1=w2=w3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】合成氨反應![]() N2(g)+
N2(g)+ ![]() H2(g)
H2(g) ![]() NH3(g) △H 的反應機理如圖所示,圖中“吸”表示各氣態物質在催化劑表面吸附。下列說法錯誤的是
NH3(g) △H 的反應機理如圖所示,圖中“吸”表示各氣態物質在催化劑表面吸附。下列說法錯誤的是
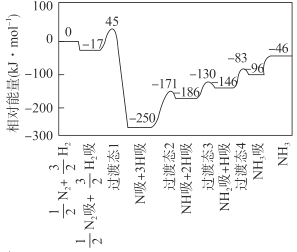
A.該反應的△H = -46 kJ·mol- 1
B.該反應機理中最大活化能為79 kJ·mol- 1
C.升高溫度,該反應過渡態的能量會增大
D.該反應達到平衡后增大壓強反應正向進行
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某酸性廢液中含有Fe3+、Cu2+、Ba2+三種金屬離子,有同學設計了下列方案對該廢液進行處理(所加試劑均稍過量),以回收金屬,保護環境。

請回答:
(1)沉淀a中含有的單質是______________________。
(2)沉淀c的化學式是__________________________。
(3)溶液A與H2O2溶液在酸性條件下反應的離子方程式是________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、W、D、E為短周期元素,且原子序數依次增大,質子數之和為39,A的單質為密度最小的氣體,B、W同周期,A、D同主族,A與W能形成兩種液態化合物A2W和A2W2,E元素的周期序數與主族序數相等。
(1)E元素在周期表中的位置為______________。寫出E的最高價氧化物的水化物與D的最高價氧化物的水化物反應的離子方程式___________________________。
(2)由A、W元素組成的18電子分子的電子式為__________________________。
(3)D的一種氧化物可與B的最高價氧化物反應生成W的單質,試寫出反應的化學方程式____________________________。
(4)向含有Fe2+和淀粉KI的溶液中滴入A2W2,觀察到溶液呈藍色并有紅褐色沉淀生成。當消耗2mol I- 時,共轉移3mol電子,該反應的離子方程式是_______________。
(5)元素D的單質在一定條件下,能與A單質化合生成一種化合物DA,DA能與水反應放氫氣,若將1mol DA和1mol E單質混合加入足量的水,充分反應后生成氣體的體積是_________L(標準狀況下)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】環境監測顯示,某地市的主要氣體污染物為SO2、NOx、CO等,其主要來源為燃煤、機動車尾氣。進行如下研究:
(1)為減少燃煤對SO2的排放,可將煤轉化為清潔燃料水煤氣(CO和H2)。
已知:![]() ΔH=241.8kJ·mol-1,
ΔH=241.8kJ·mol-1,
![]() ΔH=-110.5kJmol-1
ΔH=-110.5kJmol-1
寫出焦炭與1mol水蒸氣反應生成水煤氣的熱化學方程式:________。
(2)汽車尾氣中NO是在發動機汽缸中生成的,反應為N2(g)+O2(g)![]() 2NO(g) ΔH>0。
2NO(g) ΔH>0。
①將含0.8molN2和0.2molO2(近似空氣組成)的混合氣體充入某密閉容器中,保持1300℃反應達到平衡,測得生成8×10-4molNO。計算該溫度下此反應的化學平衡常數K=________(填近似計算結果)。
②汽車啟動后,汽缸內溫度越高,單位時間內NO排放量越大,原因是________.
(3)利用如圖所示裝置(電極均為惰性電極)可吸收SO2,并利用陰極排出的溶液吸收NO2。

①電極A的電極反應式為________;
電極B的電極反應式為________。
②堿性條件下,用陰極排出的溶液吸收NO2,使其轉化為無害氣體,同時生成SO32-。該反應的離子方程式為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,已知Ka1(H2CO3)=4.3×10-7, Ka2(H2CO3)=5.6×10-11。 某二元酸H2R及其鈉鹽的溶液中,H2R、HR-、R2-三者的物質的量分數隨溶液pH變化關系如圖所示,下列敘述錯誤的是( )
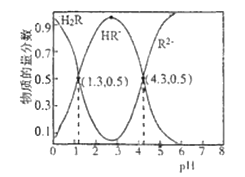
A.H2R的一級電離常數Ka1的數量級為10-2
B.在pH=4.3的溶液中:3c(R2-)=c(Na+ )+c(H+)-c(OH-)
C.等體積、等濃度的NaOH溶液與H2R溶液混合后,溶液中: c(R2- )>c(H2R)
D.向Na2CO3溶液中加入少量H2R溶液,發生的反應是: CO32- +H2R=HCO3-+HR-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子組一定能大量共存的是
A.能使pH試紙顯紅色的溶液中:Na+、NH4+、I-、NO3-
B.含有0.1mol/L Fe3+的溶液中:K+、Mg2+、S2-、SO32-
C.由水電離出來的c(H+)=1×10-13mol/L的溶液中:K+、CO32-、Cl-、NO3-
D.常溫下,![]() 的溶液:Na+、K+、CO32-、NO3-
的溶液:Na+、K+、CO32-、NO3-
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com