
【題目】有關熱化學方程式書寫與對應表述均正確的是
A. 稀硫酸與0.1 mol/L NaOH 溶液反應:H+(aq)+OH-(aq)= H2O(l) △H = +57.3 kJ·mol1
B. 已知 2C(s)+O2(g)=2CO(g)△H= -221 kJ·mol-1, 則可知 C 的熱值為 110.5 kJ·mol1
C. 0℃、30MPa 下,將 0.5mol N2 和 1.5molH2 置于密閉的容器中充分反應生成 NH3(g),放熱 19.3kJ, 其熱化學方程式為:N2(g) + 3H2(g) ![]() 2NH3(g) △H= -38.6kJ·mol1
2NH3(g) △H= -38.6kJ·mol1
D. 密閉容器中,0.3mol 硫粉與 0.2mol 鐵粉混合加熱生成硫化亞鐵 0.2mol 時,放出 19.12 kJ 熱量, 則 Fe(s)+S(s)=FeS(s)△H= - 95.6 kJ·mol1
【答案】D
【解析】
A.酸堿中和是放熱反應,故△H應為負值,故A錯誤;
B.燃燒熱指的是1mol可燃物完全燃燒生成穩定的氧化物時放出的熱量,定義要點:必須完全燃燒生成穩定的氧化物,如C→CO2,H→H2O(液),而2C(s)+O2(g)=2CO(g)△H=-221kJmol-1,是碳的不完全燃燒,故B錯誤;
C.N2(g)+3H2(g)2NH3(g),該反應是可逆反應,所以△H>38.6kJmol-1,故C錯誤;
D.則根據方程式Fe+S=FeS可知,反應中硫是過量的,則1mol參加反應放出的熱量是19.12 kJ×1mol/0.2mol=95.6kJ,因此該反應的熱化學方程式為Fe(s)+S(s)=FeS(s) △H=-95.6kJ/mol,故D正確。
故選D。


科目:高中化學 來源: 題型:
【題目】已知:pKa=-lgKa, 25℃時,H2A的pKa1=1.85,pKa2=7.19。常溫下,用0.1mol·L-1NaOH溶液滴定20 mL0.1mol·L-1H2A溶液的滴定曲線如圖所示。下列說法正確的是( )
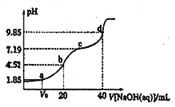
A. a點所得溶液中:c(H2A)>c(HA-) B. b點所得溶液中:c(H2A)+(H+)=c(HA-)+c(OH-)
C. c點所得溶液中:c(A2-)=c(HA-) D. d點所得溶液中A2-水解平衡常數Kh1=10-7.19
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溴、碘主要存在于海水中,有“海洋元素”的美稱。海水中的碘富集在海藻中,我國海帶產量居世界第一,除供食用外,大量用于制碘。提取碘的途徑如下所示:
干海帶![]() 海帶灰
海帶灰![]() 水溶液
水溶液![]()
![]()
![]() ―→碘單質
―→碘單質
下列有關敘述正確的是( )
A. 碘元素在海水中也有游離態存在 B. 在提取的過程中用的氧化劑可以是H2O2
C. 操作A是結晶或重結晶 D. B是提純操作,常用蒸餾或分餾
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. BF3和NH3的空間構型都為平面三角形
B. 晶格能由大到小的順序:NaF>NaCl>NaBr>NaI
C. 熔點:Na-K合金<氯化鈉<鈉<金剛石
D. 空間利用率:體心立方堆積<六方最密堆積<面心立方最密堆積
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】三氯化鐵是合成草酸鐵的重要原料。
利用工業FeCl3制取純凈的草酸鐵晶體[Fe2(C2O4)3·5H2O]的實驗流程如下圖所示:

(1)抑制FeCl3水解,溶液X為___________。
(2)流程中FeCl3能被異丙醚萃取,其原因是__________________________;檢驗萃取、分液后所得水層中是否含有Fe3+的方法是_______________________________________。
(3)得Fe2(C2O4)3·5H2O需用冰水洗滌,其目的是________________________。
(4)為測定所得草酸鐵晶體的純度,實驗室稱取a g樣品,加硫酸酸化,用KMnO4標準溶液滴定生成的H2C2O4,KMnO4標準溶液應置于下圖所示儀器_____(填“甲”或“乙”)中。
![]()
下列情況會造成實驗測得Fe2(C2O4)3·5H2O含量偏低的是_____________。
a.盛放KMnO4的滴定管水洗后未用標準液潤洗
b.滴定管滴定前尖嘴部分有氣泡,滴定后消失
c.滴定前仰視讀數,滴定后俯視讀數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以下是用硫鐵礦燒渣(主要成分為Fe2O3、Fe3O4、FeO、SiO2)為原料制備高純氧化鐵的生產流程示意圖:
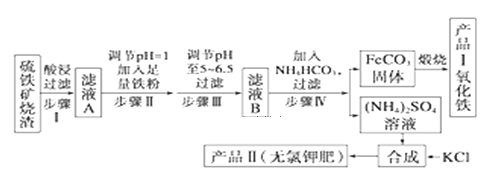
回答下列問題:
(1))古代中國四大發明之一的指南針是由天然磁石制成的,其主要成分是________(填字母) a.Fe b.FeO c.Fe2O3 d.Fe3O4
(2)酸浸、過濾后濾液A中的金屬陽離子是_________,檢驗其中較低價態的陽離子所用試劑為________(填化學式)。煅燒FeCO3生成產品Ⅰ的化學反應方程式為_______________
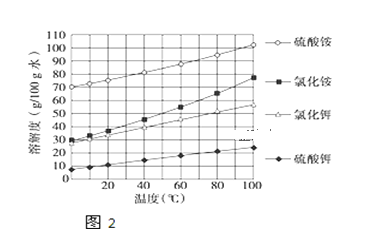
(3)已知幾種鹽的溶解度隨溫度變化的曲線如圖所示,產品Ⅱ的化學式為_______,為了獲得產品Ⅱ,向(NH4)2SO4溶液中加入KCl溶液后,還需要進行的操作是 _____、趁熱過濾、洗滌、干燥.
(4)進一步提純產品Ⅱ的方法是;__________________
(5)步驟IV反應的離子方程式__________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下在容積恒定的密閉容器中發生反應A(s)+2B(g)![]() C(g)+D(g)。下列不能說明反應一定達到化學平衡狀態的是
C(g)+D(g)。下列不能說明反應一定達到化學平衡狀態的是
A. v正(B)=2v逆(C) B. 每消耗1molC,同時生成1molD
C. 氣體的密度保持不變 D. 容器內壓強保持不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以硅孔雀石[主要成分為CuCO3·Cu(OH)2、CuSiO3·2H2O,含SiO2、FeCO3、Fe2O3等雜質]為原料制備CuCl2的工藝流程如下:

已知: SOCl2+H2O![]() SO2↑+2HCl↑,下列說法不正確的是
SO2↑+2HCl↑,下列說法不正確的是
A. “酸浸” 時應該用鹽酸溶解硅孔雀石粉
B. “氧化”時發生反應的離子方程式為:Cl2+2Fe2+![]() 2Fe3++2Cl-
2Fe3++2Cl-
C. “調pH”時,pH需控制在堿性區域,保證鐵元素全部以Fe(OH)3形式除去
D. “加熱脫水”時,加入SOCl2的目的是生成的HCl抑制CuCl2的水解
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列除去雜質(括號中的物質為雜質)的方法中,不正確的是( )
A.FeCl3溶液(FeCl2):通入適量Cl2
B.Fe2O3固體(Al2O3):加入燒堿溶液,過濾
C.CO2氣體(HCl):通過Na2CO3溶液洗氣后干燥
D.Na2CO3固體(NaHCO3):加熱
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com