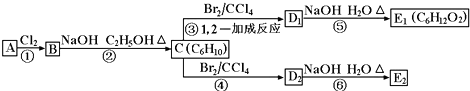
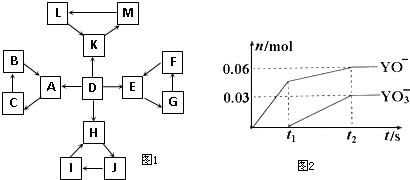
(2012?延邊州模擬)物質A~M有如圖1所示的轉化關系.圖中所有物質均由短周期元素組成,且每個小三角形內的三種物質均至少含有第三周期中的一種相同元素,其他信息見下表:
| 編號 |
信 息 |
| 1 |
D為地殼中含量最高的元素組成的單質 |
| 2 |
E為酸性氧化物,不溶于水,能與某種酸反應 |
| 3 |
F不溶于水,F用于制備干燥劑以及催化劑的載體 |
| 4 |
H為淡黃色固體化合物 |
| 5 |
電解飽和J溶液是工業生產中的重要反應 |
| 6 |
C為離子化合物,陰、陽離子均含有金屬元素 |
| 7 |
K為酸雨的主要成分 |
(1)寫出H的電子式:
.
(2)常溫下測得一定濃度的C溶液的pH=11,用離子方程式表示其原因:
AlO2-+2H2O?Al(OH)3+OH-
AlO2-+2H2O?Al(OH)3+OH-
.
(3)寫出向C溶液中通入過量CO
2的離子方程式:
AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-
AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-
.
(4)金屬銅與L濃溶液反應生成K,該反應的化學方程式是:
Cu+2H
2SO
4(濃)
CuSO
4+SO
2↑+2H
2O
Cu+2H
2SO
4(濃)
CuSO
4+SO
2↑+2H
2O
.
若標準狀況下,生成K的體積為56L,此時轉移的電子數為
5NA
5NA
,為了防止K對環境的污染,實驗室常用
氫氧化鈉溶液
氫氧化鈉溶液
試劑來吸收.
(5)電解飽和J溶液產物之一為Y
2,將一定量的Y
2 通入一定濃度的氫氧化鉀溶液中,兩者恰好完全反應時(已知反應過程放熱),生成物中有三種含Y元素的離子,其中兩種離子的物質的量(n)與反應時間(t)的變化示意圖如圖2所示.寫出該氫氧化鉀溶液中通入Y
2的總化學方程式:
5Cl2+10KOH═7KCl+2KClO+KClO3+5H2O
5Cl2+10KOH═7KCl+2KClO+KClO3+5H2O
.


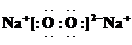
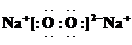
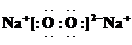 ,
,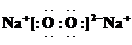 ;
;