
(14分)I.已知:C(s)+H2O(g) CO(g)+H2(g) ΔH
CO(g)+H2(g) ΔH
一定溫度下,在1.0 L密閉容器中放入1 mol C(s)、1 mol H2O(g)進行反應,反應時間(t)與容器內氣體總壓強(p)的數據見下表:
| 時間t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 總壓強p/100 kPa | 4.56 | 5.14 | 5.87 | 6.30 | 7.24 | 8.16 | 8.18 | 8.20 | 8.20 |
(14分,每空2分))
I.(1)AD (2)P/P0 79.82%(或0.80)
II.(1)xCOS(g) =" xCO(g)+" Sx(s) ΔH=0.5(bx-ax)kJ/mol
(2)①HS- c(Na+)=3[c(H2S)+c(HS-)+c(S2-)](由物料守恒得出)
或c(Na+)= c(Cl-)+c(OH-)+c(HS-)+2c(S2-)-c(H+)(由電荷守恒得出)
②M:2S2-+3H+=HS-+H2S
解析試題分析:I.(1)因為該反應中有固體參與,所以氣體的質量一直變化,而容器的體積不變,所以當混合氣體的密度不再發生改變時,證明已達平衡狀態,正確;B、消耗1 mol H2O(g)的同時生成1 mol H2
都是正反應方向,不能證明反應達平衡狀態,錯誤;C、反應方程式固定,則反應的ΔH固定,所以不能判斷化學平衡狀態是否到達,錯誤;D、CO和H2的物質的量之比是1:1,所以v正(CO) = v逆(H2)時符合正逆反應速率相等,說明反應達平衡狀態,正確,答案選AD;
(2)開始時氣體的物質的量為1mol,根據恒溫恒容條件下,氣體的物質的量之比等于氣體的壓強之比得n總=P/P0mol,由表中數據可知平衡時的壓強為8.20(100Kpa),開始的壓強為4.56(100Kpa),設消耗水蒸氣的物質的量為xmol,則平衡時H2O(g)、CO(g)、H2(g)的物質的量(mol)分別為1-x、x、x,根據n總=P/P0mol,得1-x+x+x=8.20/4.56,解得x=0.7982,所以反應物H2O(g)的轉化率α =79.82%;
II.(1)根據蓋斯定律得目標方程式=(②-①)/2,所以所求熱化學方程式為xCOS(g) =" xCO(g)+" Sx(s) ΔH=0.5(bx-ax)kJ/mol;
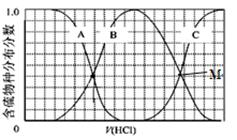
(2)①向等物質的量濃度Na2S、NaOH混合溶液中滴加稀鹽酸至過量,鹽酸先與氫氧化鈉反應生成氯化鈉和水,再與硫化鈉反應生成硫氫化鈉,此時溶液中S2?的含量逐漸減小,HS?的含量逐漸增大,繼續滴加鹽酸,則HS?與氫離子結合生成硫化氫,則溶液中H2S的含量逐漸增大,HS?的含量逐漸減小,所以A、B、C分別代表S2? 、HS?、H2S的分數變化。B曲線代表、HS?的分數變化;根據物料守恒,Na元素的濃度是S元素濃度的3倍,可得滴加過程中,溶液中一定成立的是c(Na+)=3[c(H2S)+c(HS-)+c(S2-)];滴加的過程中溶液中始終存在Na+、Cl-、HS-、S2-、OH-、H+,根據電荷守恒可得c(Na+)= c(Cl-)+c(OH-)+c(HS-)+2c(S2-)-c(H+);
②M點表示HS-與S2-分數相等,所以溶液中發生的總的離子方程式為2S2-+3H+=HS-+H2S
考點:考查化學平衡狀態的判斷及計算,蓋斯定律的應用,混合溶液的離子判斷及計算


科目:高中化學 來源: 題型:填空題
在一固定容積為2L的密閉容器內加入0.2mol的N2和0.6mol的H2,在一定條件下發生如下反應:N2(g)+3H2(g) 2NH3(g) △H<0 。反應中NH3的物質的量濃度的變化情況如下圖所示,請回答下列問題:
2NH3(g) △H<0 。反應中NH3的物質的量濃度的變化情況如下圖所示,請回答下列問題: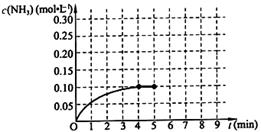
根據圖,計算從反應開始到平衡時,平均反應速率v(NH3)= 。
⑵下列描述中能說明上述反應已達平衡的是 。
| A.3v正(H2)=2v逆(NH3) |
| B.容器中氣體的平均相對分子量不隨時間而變化 |
| C.容器中氣體的密度不隨時間而變化 |
| D.容器中氣體的分子總數不隨時間而變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
用化學反應原理相關知識同答
I.根據下表所示化學反應與數據關系回答下列問題: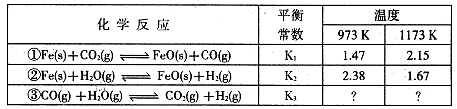
(1)反應①是 (填“吸熱"或“放熱”)反應。
(2)根據反應①與②可推導出同溫下K1、K2與K3之間的關系,則K3= (用K1、K2表示)。
(3)若反應③的逆反應速率與時間的關系如圖所示: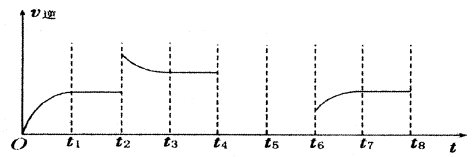
①反應在t1、t3、t7時都達到了平衡,若t2時只改變了一種外界條件j試判斷:改變的條件可能是 。
②若t4時降壓,t6時增大反應物的濃度,請在圖中畫出t4~t6時逆反應速率與時間的關系曲線。
II.請根據醋酸的電離平衡回答下列問題:
(1)常溫下,0.1mol/L 的CH3COOH溶液中有l%的CH3COOH分子發生電離,則溶液的pH= 。
(2)將上述溶液加蒸餾水稀釋,在稀釋過程中,下列各項中增大的是 (填字母編號)。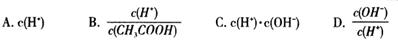
(3)25℃時,CH3COOH的電離平衡常數為1.75×10-5,現將一定量的CH3COOH與NaOH溶液混合,若測得混合液pH=5.6,則混合液中各離子濃度由大到小的順序是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知2A(g)+B(g)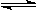 2C(g),向容積為1L的密閉容器中加入0.050 mol A和0.025mol B,在500℃時充分反應,達平衡后測得c(C)="0.040" mol·L-1,放出熱量Q1kJ。
2C(g),向容積為1L的密閉容器中加入0.050 mol A和0.025mol B,在500℃時充分反應,達平衡后測得c(C)="0.040" mol·L-1,放出熱量Q1kJ。
⑴能說明上述反應已經達到化學平衡狀態的是 (填寫序號)
a.v(C)=2v(B) b.容器內壓強保持不變
c.v逆(A)=2v正(B) d.容器內氣體的密度保持不變
⑵若在相同的容器中只加入0.050 mol C,500℃時充分反應達平衡后,吸收熱量Q2kJ,則Q1與Q2之間的關系式可表示為 (用含Q1、Q2的代數式表示);
⑶500℃時,上述反應的化學平衡常數K= ;
⑷已知:K(300℃)>K(350℃),該反應是 (填“放”或“吸”)熱反應;若反應溫度升高,A的轉化率 (填“增大”、“減小”或“不變”);
⑸某溫度下,A的平衡轉化率(a)與體系總壓強(P)的關系如圖所示,平衡狀態由a變到b時,化學平衡常數K(A) K(B)(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某溫度時, 在一個0.5 L的密閉容器中,X、Y、Z三種物質的物質的量隨時間的變化曲線如圖所示。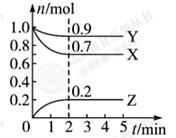
根據圖中數據回答下列問題:
(1)該反應的化學方程式為 。
(2)反應開始至2 min,以氣體Z表示的平均反應速率為 。
(3)用物質X表示的化學反應速率為0.2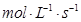 與用物質Y表示的化學反應速率為0.1
與用物質Y表示的化學反應速率為0.1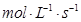 ,哪個快?( )
,哪個快?( )
a.前者 b.后者 c.一樣快 d.無法比較
(4)若X、Y、Z均為氣體,2 min后反應達到平衡,反應達平衡時:
①此時體系的壓強是開始時的 倍;
②達平衡時,容器內混合氣體的平均相對分子質量比起始投料時 (填“增大”“減小”或“相等”)。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(16分)NO和NO2是常見的氮氧化物,研究它們的綜合利用有重要意義。
(1)氮氧化物產生的環境問題有 (填一種)。
(2)氧化—還原法消除氮氧化物的轉化如下: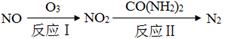
①反應Ⅰ為:NO+O3=NO2+O2,生成11.2 L O2(標準狀況)時,轉移電子的物質的量是 mol。
②反應Ⅱ中,當n(NO2)∶n[CO(NH2)2]=3∶2時,反應的化學方程式是 。
(3)硝化法是一種古老的生產硫酸的方法,同時實現了氮氧化物的循環轉化,主要反應為:
NO2(g)+SO2(g) SO3(g)+NO(g) △H=-41.8 kJ·mol-1
SO3(g)+NO(g) △H=-41.8 kJ·mol-1
①已知:2SO2(g)+O2(g) 2SO3(g) △H=-196.6 kJ·mol-1
2SO3(g) △H=-196.6 kJ·mol-1
寫出NO和O2反應生成NO2的熱化學方程式 。
②一定溫度下,向2 L恒容密閉容器中充入NO2和SO2各1 mol,5min達到平衡,此時容器中NO 和NO2的濃度之比為3∶1,則NO2的平衡轉化率是 。
③上述反應達平衡后,其它條件不變時,再往容器中同時充入
NO2、SO2、SO3、NO各1mol,平衡 (填序號)。
A.向正反應方向移動
B.向逆反應方向移動
C.不移動
(4)某化學興趣小組構想將NO轉化為HNO3,裝置如圖,電極為多孔惰性材料。則負極的電極反應式是 。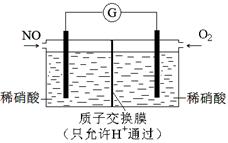
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
在恒溫、恒壓和使用催化劑的條件下,已知:在容積可變的密閉容器中,充入1 L含3 mol H2和1 mol N2的混合氣體,反應達平衡時有a mol NH3生成,N2的轉化率為b%。
(1)若在恒溫、恒壓和使用催化劑的條件下,在體積可變的密閉容器中充入x mol H2和y mol N2,反應達平衡時有3a mol NH3生成,N2的轉化率仍為b%。則x= ;
y= 。
(2)在恒溫、恒壓和使用催化劑的條件下,設在體積可變的密閉容器中充入x mol H2、y mol N2和z mol NH3,若達平衡時N2轉化率仍為b%,則x、y的關系為 ;z的取值范圍為 。
(3)在恒溫[與(1)溫度相同]和使用催化劑的條件下,在容積不可變的密閉容器中,充入1 L含3 mol H2和1 mol N2的混合氣體,反應達平衡時N2的轉化率為c%,則b、c的關系為 (用“<”、“=”或“>”表示),理由是 。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
2012年8月24日,武漢市一家有色金屬制造廠發生氨氣泄露事故。已知在一定溫度下,合成氨工業原料氣H2制備涉及下面的兩個反應:
C(s)+H2O(g) CO(g)+H2(g);
CO(g)+H2(g);
CO(g)+H2O(g) H2(g)+CO2(g)。
H2(g)+CO2(g)。
(1)判斷反應CO(g)+H2O(g) CO2(g)+H2(g)達到化學平衡狀態的依據是________。(多選、漏選、錯選均不得分)
CO2(g)+H2(g)達到化學平衡狀態的依據是________。(多選、漏選、錯選均不得分)
A.容器內壓強不變 B.混合氣體中c(CO)不變
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(2)在2 L定容密閉容器中通入1 mol N2(g)和3 mol H2(g),發生反應:3H2(g)+N2(g)  2NH3(g),ΔH<0,測得壓強-時間圖像如圖甲,測得p2=0.6p1,此時溫度與起始溫度相同,在達到平衡前某一時刻(t1)若僅改變一種條件,得到如乙圖像。
2NH3(g),ΔH<0,測得壓強-時間圖像如圖甲,測得p2=0.6p1,此時溫度與起始溫度相同,在達到平衡前某一時刻(t1)若僅改變一種條件,得到如乙圖像。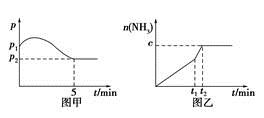
①若圖中c=1.6 mol,則改變的條件是________(填字母);
②若圖中c<1.6 mol,則改變的條件是__________(填字母);此時該反應的平衡常數____________。(填字母)(填“增大”、“減小”、“不變”)
A.升溫 B.降溫 C.加壓 D.減壓 E.加催化劑
(3)如(2)題中圖甲,平衡時氫氣的轉化率為________。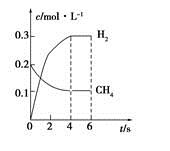
(4)工業上可利用如下反應:H2O (g)+CH4 (g) 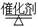 CO(g)+3H2(g)制備CO和H2。在一定條件下1 L的密閉容器中充入0.3 mol H2O和0.2 mol CH4,測得H2(g)和CH4(g)的物質的量濃度隨時間變化曲線如右圖所示:0~4 s內,用CO(g)表示的反應速率為____________。
CO(g)+3H2(g)制備CO和H2。在一定條件下1 L的密閉容器中充入0.3 mol H2O和0.2 mol CH4,測得H2(g)和CH4(g)的物質的量濃度隨時間變化曲線如右圖所示:0~4 s內,用CO(g)表示的反應速率為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
將等物質的量A、B混合于2L的密閉容器中,發生反應:3A(g)+B(g) xC(g)+2D(g),經5min后,測得D的濃度為0.5mol/L,c(A):c(B)=3:5,C的平均反應速率是0.1 mol/(L·min)。求:
xC(g)+2D(g),經5min后,測得D的濃度為0.5mol/L,c(A):c(B)=3:5,C的平均反應速率是0.1 mol/(L·min)。求:
(1)此時A的濃度及反應開始前放入容器中A、B物質的量。
(2)B的平均反應速率。
(3)x值
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com