
【題目】化學反應中的物質變化和能量變化與化學鍵密切相關。依據所學知識回答下列問題:
(1)將裝有二氧化氮和四氧化二氮混合氣體的燒瓶分別侵入冷水和熱水中,觀察到的現象是______________________,由此得出的結論是_______________________________________。
(2)某同學根據原電池原理。將離子反應Cu+2Fe3+=Cu2++2Fe2+設計成原電池,在該原電池中,以FeCl3 為電解質溶液,以石墨為正極材料,負極材料應選用_______________,負極上發生________反應(填寫“氧化“或“還原”)。當反應進行一段時間,測得負極電極質量減輕了6.4g,原電池的電路中轉移電子的物質的量是____________________________。
(3)從能量角度看,斷裂化學鍵吸收能量,形成化學鍵釋放能量。
已知:斷裂1molH-H鍵吸收的能量為436kJ,斷裂氣態ImolI-I鍵吸收的能量為151kJ,形成lmolH-I鍵放出的能量為299kJ。
則由氫氣和碘蒸氣反應生成1molHI需要________(填“放出“或“吸收”)_______kJ的熱量
【答案】 侵入冷水的燒瓶里氣體顏色變淺,侵入熱水的燒瓶里氣體顏色變深 當條件改變時,原來的化學平衡將被破壞,并在新的條件下建立起新的化學平衡,即化學平衡的移動 Cu 氧化 0.2mol 放出 5.5
【解析】(1)二氧化氮轉化成四氧化二氮反應是可逆反應,且正反應是放熱反應.將混合氣體的燒瓶分別侵入冷水和熱水中,觀察到浸入冰水中的燒瓶里的氣體混合物顏色變淺,說明二氧化氮濃度減小,四氧化二氮濃度增加,原平衡狀態被破壞,平衡向正反應方向移動,即向放熱反應方向移動;而浸入熱水中的燒瓶中氣體混合物顏色變深,說明二氧化氮濃度增加,四氧化二氮濃度減小,同樣破壞了原平衡狀態,說明平衡向逆反應方向移動.可見,當條件改變時,原來的化學平衡將被破壞,并在新的條件下建立新的平衡.即發生了化學平衡移動.
(2)根據反應Cu+2Fe3+=Cu2++2Fe2+,Cu失電子是還原劑發生氧化反應,原電池中做負極,故負極材料應選用Cu,發生氧化反應,電極反應式為:Cu—2e-=Cu2+,負極電極質量減輕了6.4g,反應的n(Cu)=0.1mol,故轉移電子的物質的量是0.2mol;
(3)1mol氫氣和1mol碘蒸氣反應生成2molHI,根據鍵能計算(436+151-2![]() ),放出11 kJ的熱量,故生成1molHI放出5.5 kJ的熱量。
),放出11 kJ的熱量,故生成1molHI放出5.5 kJ的熱量。


科目:高中化學 來源: 題型:
【題目】某些有機化合物之間具有如下轉化關系:
其中A是一種五元環狀化合物,其分子中只有一種化學環境的氫原子;F核磁共振氫譜顯示有三種化學環境的氫原子,且峰面積之比為2:2:3.
已知:① 
![]() 2RCOOH(其中R是羥基)
2RCOOH(其中R是羥基)
②R﹣COOH ![]() R﹣CH2OH(其中R是羥基)
R﹣CH2OH(其中R是羥基)
(1)G是合成順丁橡膠的主要原料,G的名稱是 . B中含氧官能團的名稱是
(2)A的結構簡式是
(3)⑥的化學方程式是
(4)E在一定條件下能夠發生縮聚反應,其中主鏈上含“﹣CH2﹣”的高聚物的結構簡式是 . 有機物Y與E互為同分異構體,且具有相同的官能 團種類和數目,則Y的結構可有種.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將4mol SO2與2molO2放入4L的密閉容器中,在一定條件下反應達到平衡:2SO2+O22SO3測得平衡時混合物總的物質的量為5mol,求:
(1)平衡時各物質的濃度;
(2)平衡時SO2的轉化率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素A、B、C、D 原子序數依次增加,X、Y、Z、W是由這四種元素中的兩種元素組成的常見化合物,X為有刺激性氣味的氣體,Y為淡黃色固體,甲是由C元素形成的氣體單質,乙為紅棕色氣體,上述物質之間的轉化關系如下圖所示(部分反應物或生成物省略)。下列說法正確的是

A. 原子半徑大小順序:D>C>B>A B. 最簡單氣態氫化物的穩定性:B>C
C. 圖示轉化關系涉及的反應均為氧化還原反應 D. 元素C、D形成的化合物中一定只含離子鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學學習和研究離不開元素周期表。下表為元素周期表的一部分,表中①-⑩分別代表一種元素。回答下列問題:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
3 | ⑧ | ⑨ | ⑩ |
(1)上述元素中,有一種元素在自然界中形成的物質種類最多,該元素在周期表中的位置是_______。
(2)⑧、⑨、⑩元素的離子半徑由大到小的順序為________________(用離子符號表示)。
(3)寫出由①、⑥、⑧三種元素形成的一種離子化合物的電子式__________________。
(4)上述元素中有一種元素的氧化物和氫氧化物都有兩性,面出該元素的原子結構示意圖______________;高溫條件下,該元素的單質與鐵紅能發生反應,此反應常用于野外焊接鋼軌,則該反應的能量變化可用圖__________________表示。(填“甲“或“乙”)
(5)知W+X→Y+Z,且W、X、Y、Z分別是由①、⑤、⑥三種元素中的兩種形成的10電子粒子,寫出并配平上述反應式___________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,向容積為2 L的密閉容器中通入兩種氣體發生化學反應,反應中各物質的物質的量變化如下圖所示,對該反應的推斷合理的是( )
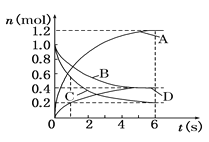
A. 該反應的化學方程式為3B+4D![]() 6A+2C
6A+2C
B. 反應進行到1 s時,v(A)=v(D)
C. 反應進行到6 s時,B的平均反應速率為0.05 mol/(L·s)
D. 反應進行到6 s時,各物質的反應速率相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于2mol二氧化碳的敘述中,正確的是( )
A. 質量為44g B. 含有4mol O C. 分子數為6.02×1023 D. 共有3mol原子
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com