
【題目】能源是現代文明的原動力,通過化學方法開辟新能源和提高能量轉化率。
請回答下列問題:
(1)已知一定條件下白磷轉化為紅磷釋放出能量,故白磷比紅磷穩定性______(填“強”、“弱”)
(2)化學反應的本質是舊的化學鍵斷裂,新的化學鍵形成。已知斷開1molH﹣H鍵、1molN≡N鍵、lmolN﹣H鍵分別需要吸收的能量為436kJ、946kJ、391kJ。那么生成1mo1 NH3需要________(填“放出”或“吸收”)__________kJ 的熱量。
(3)化學電源在生產生活中有著廣泛的應用。
①為了探究化學反應中的能量變化,某同學設計了如下兩個實驗(如下圖)。
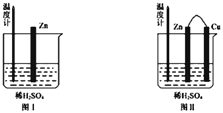
下列說法正確的是___________(填序號)
A.圖Ⅰ和圖Ⅱ的氣泡均產生于鋅棒表面
B.圖Ⅱ中產生氣體的速率比Ⅰ快
C.圖Ⅰ中溫度計的示數高于圖Ⅱ的示數
D.圖Ⅰ和圖Ⅱ中溫度計的示數相等,且均高于室溫
②燃料電池是一種高效、環境友好的供電裝置。以氫氣為燃料的電池中,電解質溶液為氫氧化鉀溶液,負極的反應式為_______________________,當外電路轉移1.2mol電子,消耗的氧氣的體積為_____________ L(標準狀況下)
【答案】弱 放出 46 BC H2-2e-+2OH-=2H2O 6.72
【解析】
(1)物質能量越高越活潑;
(2)化學反應的焓變△H=反應物總鍵能-生成物總鍵能;
(3)①圖Ⅰ鋅和稀硫酸反應生成硫酸鋅和氫氣,離子方程式為Zn+2H+═Zn2++H2↑;;圖Ⅱ該裝置構成原電池,Zn易失電子作負極,Cu作正極,正極上氫離子得電子生成氫氣,據此分析作答;
②原電池中負極發生氧化反應,正極發生還原反應,并考慮電解質溶液參與電極反應來分析;根據電子轉移數與氧氣的關系式求出氧氣消耗量。
(1)已知一定條件下,白磷轉化為紅磷釋放出能量,紅磷能量低,故白磷比紅磷穩定性弱,
故答案為:弱;
(2)在反應N2+3H22NH3中,形成2molNH3,需放出的能量為6×391kJ=2346kJ,斷裂3molHH鍵,1molN≡N鍵共吸收的能量為:3×436kJ+946kJ=2254kJ,該反應為放熱反應,放出的熱量數值為2346kJ2254kJ=92kJ,根據化學反應熱與化學計量數成比例可知,當生成1molNH3時需要放出熱量為46kJ,
故答案為:放出;46;
(3)①A. 圖Ⅰ中氣泡產生在鋅棒表面,Ⅱ中產生在銅棒表面,A項錯誤;
B. 構成原電池加快化學反應速率,則圖Ⅱ中產生氣體的速度比Ⅰ快,B項正確;
C. 圖Ⅱ的溫度計指示的溫度變化不明顯,說明化學能沒有全部轉化為熱能,大多數轉化為電能,則圖Ⅰ中溫度計的示數高于圖Ⅱ的示數,C項正確;
D. 圖Ⅰ稀硫酸和鋅的反應是放熱反應導致溶液溫度逐漸升高,化學能轉化為熱能,溫度高于室溫,而圖Ⅱ化學能沒有全部轉化為熱能,大多數轉化為電能,其溫度計指示的溫度變化不明顯,兩圖示數不相同,D項錯誤;
故答案為:BC;
②燃料電池中,負極氫氣失電子發生氧化反應,在堿性條件下負極反應式為H2-2e-+2OH-=2H2O;正極電極反應為:O2+2H2O+4e=4OH,根據關系式可知,當外電路轉移1.2mol電子,消耗的氧氣的體積為![]() =6.72L,故答案為:H2-2e-+2OH-=2H2O;6.72。
=6.72L,故答案為:H2-2e-+2OH-=2H2O;6.72。


 教學練新同步練習系列答案
教學練新同步練習系列答案 課前課后同步練習系列答案
課前課后同步練習系列答案 課堂小作業系列答案
課堂小作業系列答案 黃岡小狀元口算速算練習冊系列答案
黃岡小狀元口算速算練習冊系列答案科目:高中化學 來源: 題型:
【題目】鈦白粉(TiO2)是重要的白色顏料,LiFePO4是鋰離子電池的正極材料。一種利用鈦鐵礦( 主要成分為FeTiO3 和少量Fe2O3 )進行鈦白粉和LiFePO4 的聯合生產工藝如下圖所示:

回答下列問題:
(1) LiFePO4中Fe的化合價是_______________________。
(2)鈦鐵礦“酸溶”前需要進行粉碎,粉碎的目的是__________________________________。
(3)用離子方程式表示操作I加入鐵粉的目的:__________________________。操作II為一系列操作,名稱是加熱濃縮、冷卻結晶、過濾,其中用到的陶瓷儀器的名稱是___________。
(4)TiO2+易水解,則其水解的離子方程式為______________________;“轉化”利用的是TiO2+的水解過程,需要對溶液加熱,加熱的目的是________________________________。
(5)“沉鐵”的的是使Fe3+生成FePO4,當溶液中c(PO43-)= 1.0×10-17mol/L時可認為Fe3+ 沉淀完全,則溶液中Fe3+沉淀完全時的c(Fe3+)=_______mol/L[已知:該溫度下,Ksp(FePO4)=1.0×10-22]。
(6)由“沉鐵”到制備LiFePO4的過程中,所需17% H2O2溶液與草酸( H2C2O4)的質量比是_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物A的結構為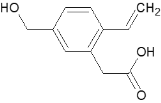 , 下列有關說法正確的是
, 下列有關說法正確的是
A. 1 mol A能跟2 mol NaOH溶液反應
B. 能發生加聚反應
C. 不能發生分子內酯化反應
D. A分子中所有原子在同一平面上
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,某酸H3A水溶液中含A的各種粒子的分布分數(平衡時某種粒子的濃度占各粒子濃度之和的分數)與pH的關系圖如下所示,下列說法正確的是
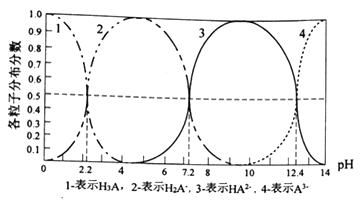
A. NaH2A水溶液呈堿性
B. H3A溶液中存在:c(H+)=c(OH-)+c(H2A-)+1/2c(HA2-)+1/3c(A3-)
C. 向H3A溶液中加入一定量的NaOH溶液至pH=5時,c(HA2-)/c(H3A)=100.6
D. 向H3A溶液中加入氨水使pH從5→9發生的主要離子反應是:H2A-+OH-![]() HA2-+H2O
HA2-+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】通常狀況下,在體積一定的密閉容器中的NH3和Cl2恰好完全反應,若反應產物只有N2和NH4Cl,則反應前后容器中的壓強比應接近于
A.1:11B.11:1C.7:11D.1:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【選做-選修5: 有機化學基礎】PET和PMMA是日常生活常見的兩種高分子材料。下列是合成高分子材料的路線:

已知:①RCOOR1+R2OH![]() RCOOR2+R1OH
RCOOR2+R1OH
② (R1、R2表示烴基或氫原子)
(R1、R2表示烴基或氫原子)
回答下列問題:
(1)物質A的化學名稱_______,物質H中官能團的名稱________。
(2)由C生成D、I生成J的反應類型分別是_______、_______。
(3)由I生成J的反應中產生六元環的副產物,其結構簡式為_______。
(4)寫出D+乙二醇→F+G的化學反應方程式________________。
(5)D存在多種同分異構體,其中只含有一種官能團的三取代芳香族化合物且能與碳酸氫鈉溶液作用產生氣體的同分異構體有____種。
(6)寫出用環己醇為原料制備 的合成路線(其他試劑任選)_________。
的合成路線(其他試劑任選)_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關比較正確的是
A. N、O、F最高價依次升高 B. Al3+、K+、F- 微粒半徑依次增大
C. 單質的熔點:Cl2>Br2>I2 D. 堿性:CsOH>KOH>NaOH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關有機物的說法不正確的是
A. 糖類物質均能發生水解反應
B. 酒精中是否含有水,不能用金屬鈉檢驗
C. 蛋白質在一定條件下能發生水解反應,生成氨基酸
D. 不能用米湯直接檢驗加碘食鹽中是否含有碘元素
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上用鉻鐵礦(FeO、Cr2O3、含SiO2、Al2O3雜質)生產紅礬鈉(Na2Cr2O7)的工藝流程如下:
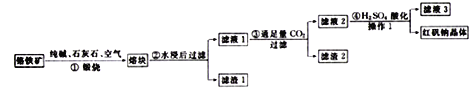
(1)上述四個步驟中,有氧化還原反應發生的是________(填序號),被氧化的元素是______(寫元素符號)。
(2)濾渣1的主要成分是________(寫化學式),寫出步驟③發生反應的離子方程式___________________。
(3)操作1包括______、________、過濾、洗滌、干燥。
(4)向橙紅色的紅釩鈉溶液中滴入氨氧化鈉溶液,變為黃色Na2CrO4溶液,寫出該轉化過程的離子方程式______________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com