
【題目】下列溶液中Cl—濃度最大的是
A.200mL2mol/L氯化鈉溶液B.100mL1mol/L氯化鋁溶液
C.500mL1mol/L氯化鎂溶液D.100g液氯
科目:高中化學 來源: 題型:
【題目】現(xiàn)在污水治理越來越引起人們重視,可以通過 ![]() 膜電池除去廢水中的乙酸鈉和對氯苯酚( ),其原理如圖所示,下列說法正確的是.
膜電池除去廢水中的乙酸鈉和對氯苯酚( ),其原理如圖所示,下列說法正確的是. 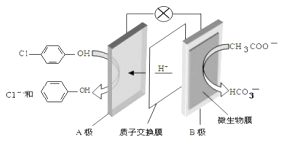
A.電流方向從B極沿導線經(jīng)小燈泡流向A極
B.A極的電極反應式為 ![]() +e﹣═Cl﹣+
+e﹣═Cl﹣+ ![]()
C.當外電路中有0.2mole﹣轉移時,通過質子交換膜的H+的個數(shù)為0.1NA
D.B極為電池的正極,發(fā)生還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某興趣小組設計如下微型實驗裝置.實驗時,先斷開K2 , 閉合K1 , 兩極均有氣泡產(chǎn)生;一段時間后,斷開K1 , 閉合K2 , 發(fā)現(xiàn)電流表指針偏轉,下列有關描述正確的是( ) 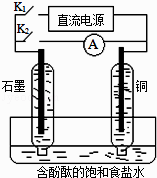
A.斷開K2 , 閉合K1時,總反應的離子方程式為:2H++2Cl﹣ ![]() Cl2↑+H2↑
Cl2↑+H2↑
B.斷開K2 , 閉合K1時,石墨電極附近溶液變紅
C.斷開K1 , 閉合K2時,銅電極上的電極反應為:Cl2+2e﹣=2Cl﹣
D.斷開K1 , 閉合K2時,石墨電極作正極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某校研究性學習小組用一些大部分已經(jīng)銹蝕(成分為 Fe2O3)的廢鐵屑制備綠礬(FeSO4·7H2O),實驗操作過程如下:

已知:雜質不溶于稀硫酸。
請回答下列問題:
(1)步驟①中,稀硫酸與 Fe2O3反應的離子方程式為 ______,廢鐵屑用硫酸處理后,還含有不溶性雜質,為獲取澄清的A溶液,需進行的操作名稱是 _________。
(2)步驟②中溶液A與鐵粉反應的離子方程式為________________。
(3)檢驗溶液 B 中是否還存在雜質金屬陽離子的方法是_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“吃盡百味還點鹽,穿盡綾羅不如棉”。食鹽不僅是調(diào)味品,更在醫(yī)藥、化工等領域有廣泛應用。下列有關敘述中正確的是
A. 食鹽熔化時因離子鍵遭破壞故屬化學變化 B. 電解飽和食鹽水可制備金屬鈉
C. 生理鹽水的濃度越接近飽和藥效越好 D. 加碘食鹽中的碘以 IO3- 形成存在
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】濃度為2mol/L的NaOH溶液的正確含義是 ( )
A. 在2L水中溶有80g NaOH B. 80g NaOH 溶于水配成的溶液
C. 每2L溶液中含有80g NaOH D. 每升溶液中含有80g NaOH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:CO(g)+2H2(g)CH3OH(g)△H=﹣a kJmol﹣1 . ①經(jīng)測定不同溫度下該反應的平衡常數(shù)如下:
溫度(℃) | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
若某時刻、250℃測得該反應的反應物與生成物的濃度為c(CO)=0.4molL﹣1、c(H2)=0.4molL﹣1、c(CH3OH)=0.8molL﹣1 , 則此時v正v逆(填“>”、“<”或“=”).
②某溫度下,在體積固定的2L的密閉容器中將1mol CO和2mol H2混合,測得不同時刻的反應前后壓強關系如下:
時間(min) | 5 | 10 | 15 | 20 | 25 | 30 |
壓強比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
則0~15min,用H2表示的平均反應速率為 , 達到平衡時CO的轉化率為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學在用稀硫酸與鋅制取氫氣的實驗中,發(fā)現(xiàn)反應條件不同,反應速率不同。請回答下列問題:
(1)在用稀硫酸與鋅制氫的實驗中,加入少量下列物質可加快氫氣生成速率的是_____(填序號)
A.Na2SO4 溶液 B.MgSO4 溶液 C.SO3 D.CuSO4 溶液
(2)為了進一步研究硫酸銅的量對氫氣生成速率的影響,該同學設計了如下一系列的實驗:將表中所給的混合溶液分別加入到6個盛有過量Zn粒的容器中,收集產(chǎn)生的氣體,記錄獲得相同體積的氣體所需時間。
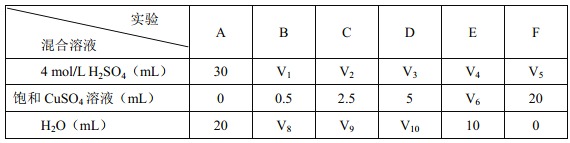
請完成此實驗設計,其中:V1=____ mL, V6=______ mL。
該同學最后得出的結論為:當加入少量CuSO4溶液時,生成氫氣的速率會大大提高,但當加入的CuSO4溶液超過一定量時,生成氫氣的速率反而會下降。請分析速率下降的主要原因__________ 。
(3)該同學為探究其它因素對鋅與稀硫酸反應速率的影響,又做了以下實驗,記錄數(shù)據(jù)如下,回答下列問題:
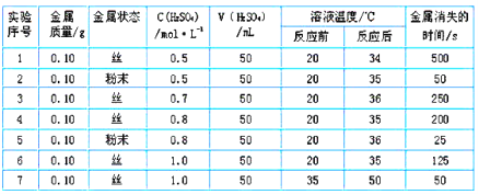
①由實驗可推知,反應物的總能量_______產(chǎn)物的總能量(填“<”、 “>” 或“=”)。
②實驗2和5表明,______對反應速率有影響。
③實驗4和5表明,______對反應速率有影響,能表明同一規(guī)律的實驗還有 _________ (填實驗序號)。
④本實驗中影響反應速率的其他因素還有________。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com