
 .
.分析 在標準狀況下8.5g HxA氣體的體積是5.6L,其物質的量為$\frac{5.6L}{22.4L/mol}$=0.25mol,故HxA的相對分子質量為$\frac{8.5}{0.25}$=34,含5.1g HxA的物質的量為$\frac{5.1g}{34g/mol}$=0.15mol,CuCl2的物質的量為0.2L×0.75mol/L=0.15mol,二者正好完全反應,生成黑色沉淀,則HxA中A表現-2價,故x=2,則A的相對原子質量,34-2=32,若A的質子數等于中子數,可推知A為S元素,據此解答.
解答 解:(1)在標準狀況下8.5g HxA氣體的體積是5.6L,其物質的量為$\frac{5.6L}{22.4L/mol}$=0.25mol,故HxA的相對分子質量為$\frac{8.5}{0.25}$=34,含5.1g HxA的物質的量為$\frac{5.1g}{34g/mol}$=0.15mol,CuCl2的物質的量為0.2L×0.75mol/L=0.15mol,二者正好完全反應,生成黑色沉淀,則HxA中A表現-2價,故x=2,則A的相對原子質量,34-2=32,若A的質子數等于中子數,可推知A為S元素,故答案為:32;S;
(2)硫元素的最高價氧化物是SO3,室溫下呈液態,其分子由共價鍵結合而成,故答案為:SO3;液態;共價;
(3)化合物HxA為H2S,電子式為: ,故答案為:
,故答案為: ;
;
(4)HxA與CuCl2溶液反應的離子方程式為:H2S+Cu2+=CuS↓+2H+,故答案為:H2S+Cu2+=CuS↓+2H+.
點評 本題考查元素化合物推斷,屬于計算型推斷,難度不大,注意三氧化硫的熔沸點.


科目:高中化學 來源: 題型:選擇題
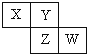
| A. | Z單質的化學活潑性一定比Y單質的強 | |
| B. | W的原子序數可能是Y的原子序數的2倍 | |
| C. | W的氣態氫化物的穩定性一定比Y的強 | |
| D. | X和W兩元素不可能形成共價化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 通過紅外光譜分析可以區分乙醇與乙酸乙酯 | |
| B. | 煎炸食物的花生油和牛油都是可皂化的飽和酯類 | |
| C. | 淀粉可用于制備葡萄糖、釀制食醋,還可作藥片的賦形劑 | |
| D. | 利用太陽能在催化劑參與下分解水制氫是把光能轉化為化學能的綠色化學方法 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 為了加快過濾速度,可用玻璃棒攪拌過濾器中的液體 | |
| B. | 為了防止容量瓶漏液,可在玻璃塞上涂上凡士林 | |
| C. | 為了使制取氫氣的速率加快,可向稀硫酸中加入少量硫酸銅溶液 | |
| D. | 為了使配制的FeCl3溶液不產生混濁,可加入鹽酸和鐵片 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
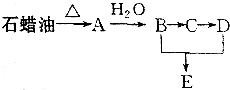 某課外小組以石蠟為原料進行如圖所示轉化關系的實驗探究,其中E具有果香味,且分子中含4個碳原子.試填空:
某課外小組以石蠟為原料進行如圖所示轉化關系的實驗探究,其中E具有果香味,且分子中含4個碳原子.試填空: CH3COOCH2CH3+H2O,反應類型為酯化反應.
CH3COOCH2CH3+H2O,反應類型為酯化反應.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
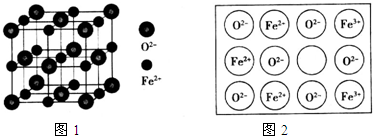
 短周期元素X、Y、Z、W在周期表中相對位置如圖所示,Y元素在地殼中的含量最高.下列說法正確的是( )
短周期元素X、Y、Z、W在周期表中相對位置如圖所示,Y元素在地殼中的含量最高.下列說法正確的是( )| A. | 原子半徑:Z<Y<W | |
| B. | 最簡單氣態氫化物的熱穩定性:Y<W | |
| C. | 含X的化合物形成的溶液一定呈酸性 | |
| D. | Y的最簡單陰離子和Z的最簡單陽離子核外電子數相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| 步驟 | 操作 | 現象 |
| ① | 用pH試紙檢驗 | 溶液的pH大于7 |
| ② | 向溶液中滴加氯水,再加入CCl4震蕩,靜置 | CCl4層呈橙色 |
| ③ | 向②所得溶液中加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀產生 |
| ④ | 過濾,向濾液中加入AgNO3溶液和稀HNO3 | 有白色沉淀產生 |
| A. | 肯定含有的離子是Na+、Br-、SO32- | B. | 肯定沒有的離子是Ba2+、SO32- | ||
| C. | 可能含有的離子是Cl-、Br-、SO42- | D. | 不能確定的離子是Cl-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 向1000mL3mol•L-1NaOH溶液中通入適量CO2氣體,溶液中有關陰離子的物質的量變化曲線圖所示,下列說法中正確的( )
向1000mL3mol•L-1NaOH溶液中通入適量CO2氣體,溶液中有關陰離子的物質的量變化曲線圖所示,下列說法中正確的( )| A. | 水的電離程度一直增大 | |
| B. | 溶液的pH逐漸下降 | |
| C. | M、N兩點對應的溶液中離子種類不同 | |
| D. | CD段反應的離子方程式為OH-+CO2=HCO3- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com