
 某校化學研究性學習小組為了證明銅與稀硝酸反應產生一氧化氮,用如圖所示裝置進行實驗,(加熱裝置和夾持裝置均已略去,氣密性已檢驗,F是用于鼓入空氣的雙連打氣球)
某校化學研究性學習小組為了證明銅與稀硝酸反應產生一氧化氮,用如圖所示裝置進行實驗,(加熱裝置和夾持裝置均已略去,氣密性已檢驗,F是用于鼓入空氣的雙連打氣球)| 操作 | 現象 |
| Ⅰ.將B裝置下移,使碳酸鈣與稀硝酸接觸 | 產生氣體 |
| Ⅱ.當C處產生白色沉淀時,立刻將B裝置上提 | |
| Ⅲ.將A中銅絲放入稀硝酸中,給裝置A微微加熱 | 裝置A中產生無色氣體 裝置E中開始時出現淺紅棕色氣體 |
| Ⅳ.用F向E中鼓入空氣 | 燒瓶E內氣體顏色逐漸加深 |
| Ⅴ.一段時間后 | C中白色沉淀溶解 |
| ||
| ||
| ||
| ||


科目:高中化學 來源: 題型:閱讀理解
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解

| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
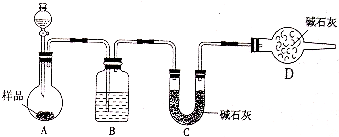
 某校化學研究性學習小組設計如下實驗方案,測定放置己久的小蘇打樣品中純堿的質量分數.
某校化學研究性學習小組設計如下實驗方案,測定放置己久的小蘇打樣品中純堿的質量分數.查看答案和解析>>
科目:高中化學 來源:2011-2012學年黑龍江哈爾濱市第六中學高三上學期期末考試化學試卷 題型:填空題
(14分)某校化學研究性學習小組設計如下實驗方案,測定放置已久的小蘇打樣品中純堿的質量分數。
(1)方案一:稱取一定質量的樣品,置于坩堝中加熱至恒重后,冷卻,稱量剩余固體質量,計算。實驗中加熱至恒重的目的是 。
(2)方案二:稱取一定量樣品,置于小燒杯中,加適量水溶解,向小燒杯中加入足量氯化鋇溶液,過濾洗滌,干燥沉淀,稱量固體質量,計算:
①過濾操作中,除了燒杯、漏斗外還用到的玻璃儀器有______________________;
②試驗中判斷沉淀是否完全的方法是_______________________________________
③若加入試劑改為氫氧化鋇,已知稱得樣品9.5g,干燥的沉淀質量為19.7g,則樣品中碳酸鈉的質量分數為_________________(保留一位小數)。
查看答案和解析>>
科目:高中化學 來源:2012屆黑龍江哈爾濱市高三上學期期末考試化學試卷 題型:填空題
(14分)某校化學研究性學習小組設計如下實驗方案,測定放置已久的小蘇打樣品中純堿的質量分數。
(1)方案一:稱取一定質量的樣品,置于坩堝中加熱至恒重后,冷卻,稱量剩余固體質量,計算。實驗中加熱至恒重的目的是 。
(2)方案二:稱取一定量樣品,置于小燒杯中,加適量水溶解,向小燒杯中加入足量氯化鋇溶液,過濾洗滌,干燥沉淀,稱量固體質量,計算:
①過濾操作中,除了燒杯、漏斗外還用到的玻璃儀器有______________________;
②試驗中判斷沉淀是否完全的方法是_______________________________________
③若加入試劑改為氫氧化鋇,已知稱得樣品9.5g,干燥的沉淀質量為19.7g,則樣品中碳酸鈉的質量分數為_________________(保留一位小數)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com