


科目:高中化學 來源: 題型:閱讀理解
| 實驗編號 | 實驗目的 | T/K | pH | c/10-3mol.L-1 | |
| H2O | Fe2- | ||||
| (1) | 為以下實驗作參照 | 298 | 3 | 6.0 | 0.30 |
| (2) | 探究溫度對降解反應速的影響率 | ||||
| (3) | 298 | 10 | 6.0 | 0.30 | |

查看答案和解析>>
科目:高中化學 來源: 題型:

 Fe(SCN)2+來檢驗反應是否產生鐵離子.已知在一定溫度下該反應達到平衡時c(Fe3+)=0.04mol?L-1,c(SCN-)=0.1mol?L-1,c[Fe(SCN)2+]=0.68mol?L-1.則此溫度下該反應的平衡常數K=
Fe(SCN)2+來檢驗反應是否產生鐵離子.已知在一定溫度下該反應達到平衡時c(Fe3+)=0.04mol?L-1,c(SCN-)=0.1mol?L-1,c[Fe(SCN)2+]=0.68mol?L-1.則此溫度下該反應的平衡常數K=查看答案和解析>>
科目:高中化學 來源: 題型:
| 實驗 編號 |
T/K | pH | c/10-3mol?L-1 | |
| H2O2 | Fe2+ | |||
| Ⅰ | 298 | 3 | 6.0 | 0.30 |
| Ⅱ | 313 | 3 | 6.0 | 0.30 |
| Ⅲ | 298 | 10 | 6.0 | 0.30 |
查看答案和解析>>
科目:高中化學 來源: 題型:
![]() Fenton法常用于處理含難降解有機物的工業廢水,通常是在調節好PH和
Fenton法常用于處理含難降解有機物的工業廢水,通常是在調節好PH和![]() 濃度的廢水中加入H2O2,所產生的羥基自由基能氧化降解污染物。現運用該方法降解有機污染物p-CP,探究有關因素對該降解反應速率的影響。
濃度的廢水中加入H2O2,所產生的羥基自由基能氧化降解污染物。現運用該方法降解有機污染物p-CP,探究有關因素對該降解反應速率的影響。
![]() [實驗設計]控制p-CP的初始濃度相同,恒定實驗溫度在298K或313K(其余實驗條件見下表),設計如下對比試驗。
[實驗設計]控制p-CP的初始濃度相同,恒定實驗溫度在298K或313K(其余實驗條件見下表),設計如下對比試驗。
![]() (1)請完成以下實驗設計表(表中不要留空格)。
(1)請完成以下實驗設計表(表中不要留空格)。
| 實驗
| 實驗目的 | T/K | PH | c/10-3mol·L-1 | |
| H2O2 | Fe2+ | ||||
| ① | 為以下實驗作參考 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究溫度對降解反應速率的影響 | ||||
| ③ |
| 298 | 10 | 6.0 | 0.30 |
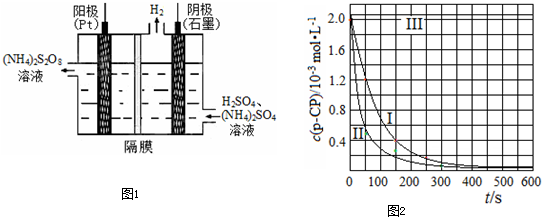
![]() [數據處理]實驗測得p-CP的濃度隨時間變化的關系如右上圖。
[數據處理]實驗測得p-CP的濃度隨時間變化的關系如右上圖。

![]() (2)請根據右上圖實驗①曲線,計算降解反應在50~150s內的反應速率:
(2)請根據右上圖實驗①曲線,計算降解反應在50~150s內的反應速率:
![]()
![]() (p-CP)= mol·L-1·s-1
(p-CP)= mol·L-1·s-1
![]() [解釋與結論]
[解釋與結論]
![]() (3)實驗①、②表明溫度升高,降解反應速率增大。但溫度過高時反而導致降解反應速率減小,請從Fenton法所用試劑H2O2的角度分析原因: 。
(3)實驗①、②表明溫度升高,降解反應速率增大。但溫度過高時反而導致降解反應速率減小,請從Fenton法所用試劑H2O2的角度分析原因: 。
![]() (4)實驗③得出的結論是:PH等于10時, 。
(4)實驗③得出的結論是:PH等于10時, 。
![]() [思考與交流]
[思考與交流]
![]() (5)實驗時需在不同時間從反應器中取樣,并使所取樣品中的反應立即停止下來。根據上圖中的信息,給出一種迅速停止反應的方法:
(5)實驗時需在不同時間從反應器中取樣,并使所取樣品中的反應立即停止下來。根據上圖中的信息,給出一種迅速停止反應的方法: ![]()
查看答案和解析>>
科目:高中化學 來源:2015屆江蘇省泰州市姜堰區高二上學期期中考試化學試卷(解析版) 題型:實驗題
Fenton法常用于處理含難降解有機物的工業廢水,通常是在調節好PH和Fe2+濃度的廢水中加入H2O2,所產生的羥基自由基能氧化降解污染物。現運用該方法降解有機污染物p-CP,探究有關因素對該降解反應速率的影響。
【實驗設計】控制p-CP的初始濃度相同,恒定實驗溫度在298K或313K(其余實驗條件見下表),設計如下對比試驗。
(1)請完成以下實驗設計表(表中不要留空格)。
|
實驗 編號 |
實驗目的 |
T/K |
pH |
c/10-3mol·L-1 |
|
|
H2O2 |
Fe2+ |
||||
|
① |
為以下實驗作參考 |
298 |
3 |
6.0 |
0.30 |
|
② |
探究溫度對降解反應速率的影響 |
|
|
|
|
|
③ |
|
298 |
10 |
6.0 |
0.30 |
【數據處理】實驗測得p-CP的濃度隨時間變化的關系如下圖。

(2)請根據上圖實驗①曲線,計算降解反應在50~150s內的反應速率:
υ(p-CP)= mol·L-1·s-1
(3)實驗①、②表明溫度升高,降解反應速率增大。但溫度過高時反而導致降解反應速率減小,請從Fenton法所用試劑H2O2的角度分析原因:
。
(4)實驗③得出的結論是:pH等于10時, 。
(5)實驗時需在不同時間從反應器中取樣,并使所取樣品中的反應立即停止下來。根據上圖中的信息,給出一種迅速停止反應的方法 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com