
【題目】已知1g氫氣完全燃燒生成水蒸氣時放出熱量121kJ,且氧氣中1mol O=O鍵完全斷裂時吸收熱量496kJ,水蒸氣中1mol H﹣O鍵形成時放出熱量463kJ,則氫氣中1mol H﹣H鍵斷裂時吸收熱量為( )
A.920kJ
B.557kJ
C.436kJ
D.181kJ
 優等生題庫系列答案
優等生題庫系列答案科目:高中化學 來源: 題型:
【題目】現有下列短周期元素的數據(已知Be的原子半徑為0.089 nm):
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半徑 (nm) | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
最高正化合價 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
最低負化合價 | 2 | 3 | 1 | 3 |
(1)⑧號元素的在周期表中的位置是________________;上述元素處于同一主族的有_________________________。(用元素符號表示!)
(2)上表中某兩種元素形成的共價化合物中,每個原子都滿足最外層為8電子的穩定結構,寫出其電子式:__________________________(任寫一種
(3)元素①和⑥能形成兩種化合物,寫出其中較穩定的化合物與水反應的離子方程式_____________________________________________________。
(4)含鋰材料在社會中廣泛應用,如各種儲氫材料(Li2NH等)、便攜式電源材料(LiCoO2等)。根據下列要求回答問題:
①![]() 和
和![]() 作核反應堆最佳熱載體,
作核反應堆最佳熱載體,![]() 和
和![]() 用作高溫堆減速劑。下列說法正確的是________
用作高溫堆減速劑。下列說法正確的是________
A. ![]() 和
和![]() 互為同位素 B.
互為同位素 B. ![]() 和
和![]() 屬于同種核素
屬于同種核素
C. ![]() 和
和![]() 的化學性質不同 D.
的化學性質不同 D. ![]() 和
和![]() 是同種物質
是同種物質
②下列說法不正確的是_________
A. 堿性:Be(OH)2 < LiOH < NaOH < KOH
B. 半徑:K > Na > Li > Li+
C. 氧化性:Li+ < Na+ < K+ < Rb+ < Cs+
D. 金屬性:Cs > Rb > K > Na > Li > Be
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CH4超干重整CO2技術可得到富含CO的氣體,用于生產多種化工產品。該技術中的化學反應為:CH4(g)+3CO2(g) ![]() 2H2O(g)+4CO(g) ΔH=+330kJ/mol
2H2O(g)+4CO(g) ΔH=+330kJ/mol
(1)下圖表示初始投料比n(CH4):n(CO2)為1:3或1:4,CH4的轉化率在不同溫度(T1、T2)下與壓強的關系。[注:投料比用a1、a2表示]

①a2=__________。
②判斷T1的T2的大小關系,并說明理由:__________。
(2)CH4超干重整CO2的催化轉化原理示意圖如下:

①過程Ⅰ,生成1mol H2時吸收123.5kJ熱量,其熱化學方程式是__________。
②過程Ⅱ,實現了含氫物種與含碳物種的分離。生成H2O(g)的化學方程式是__________。
③假設過程Ⅰ和過程Ⅱ中的各步均轉化完全,下列說法正確的是__________。(填序號)
a.過程Ⅰ和過程Ⅱ中發生了氧化還原反應
b.過程Ⅱ中使用的催化劑為Fe3O4和CaCO3
c.若過程Ⅰ投料![]() ,可導致過程Ⅱ中催化劑失效
,可導致過程Ⅱ中催化劑失效
【答案】 1:4 T2>T1 正反應為吸熱反應,溫度升高時甲烷的轉化率增大 CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+247kJ/mol 4H2+Fe3O4![]() 3Fe+4H2O ac
3Fe+4H2O ac
【解析】(1). ①.在相同條件下,投料比越小,甲烷的轉化率越大,據圖可知,a2>a1,故a2表示的是1:4時甲烷的轉化率,故答案為:1:4;
②. 因CH4(g)+3CO2(g)![]() 2H2O(g)+4CO(g)的正反應為吸熱反應,溫度升高時,平衡正向移動,甲烷的轉化率增大,則T2>T1,故答案為:T2>T1,正反應為吸熱反應,溫度升高時甲烷的轉化率增大;
2H2O(g)+4CO(g)的正反應為吸熱反應,溫度升高時,平衡正向移動,甲烷的轉化率增大,則T2>T1,故答案為:T2>T1,正反應為吸熱反應,溫度升高時甲烷的轉化率增大;
(2). ①.在過程I中,生成1mol H2時吸收123.5kJ熱量,據圖可知,其熱化學方程式為:CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+247kJ/mol,故答案為:CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+247kJ/mol;
②. 由過程II的轉化關系來看,混合氣體中的H2將Fe3O4還原為Fe,反應方程式為:4H2+Fe3O4 ![]() 3Fe+4H2O,故答案為:4H2+Fe3O4
3Fe+4H2O,故答案為:4H2+Fe3O4 ![]() 3Fe+4H2O;
3Fe+4H2O;
③. a. 兩個過程都有元素化合價的改變,都發生了氧化還原反應,故a正確;b. 過程II中Fe3O4最終被還原為Fe,Fe3O4不是催化劑,故b錯誤;c. 若初始投料比![]() 時,二者恰好按照題給方程式反應,無CO2生成,導致CaCO3無法參加反應,使催化劑中毒失效,故c正確;答案選ac。
時,二者恰好按照題給方程式反應,無CO2生成,導致CaCO3無法參加反應,使催化劑中毒失效,故c正確;答案選ac。
【題型】綜合題
【結束】
17
【題目】工、農業廢水以及生活污水中濃度較高的![]() 會造成氮污染。工業上處理水體中
會造成氮污染。工業上處理水體中![]() 的一種方法是零價鐵化學還原法。某化學小組用廢鐵屑和硝酸鹽溶液模擬此過程,實驗如下。
的一種方法是零價鐵化學還原法。某化學小組用廢鐵屑和硝酸鹽溶液模擬此過程,實驗如下。
(1)先用稀硫酸洗去廢鐵屑表面的鐵銹,然后用蒸餾水將鐵屑洗凈。
①除銹反應的離子反程式是__________。
②判斷鐵屑洗凈的方法是__________。
(2)將KNO3溶液的pH調至2.5。從氧化還原的角度分析調低溶液pH的原因是__________。
(3)將上述處理過的足量鐵屑投入(2)的溶液中。如圖表示該反應過程中,體系內相關離子濃度、pH隨時間變化的關系。請根據圖中信息回答:

①t1時刻前該反應的離子方程式是__________。
②t2時刻后,該反應仍在進行,溶液中![]() 的濃度在增大,Fe2+的濃度卻沒有增大,可能的原因是__________。
的濃度在增大,Fe2+的濃度卻沒有增大,可能的原因是__________。
(4)鐵屑與KNO3溶液反應過程中向溶液中加入炭粉,可以增大該反應的速率,提高![]() 的去除效果,其原因是__________。
的去除效果,其原因是__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據要求回答下列問題:
I. ①H、D、T ②H2O、D2O ③石墨、金剛石 ④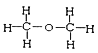 和
和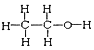
四組微粒或物質中,互為同位素的是_______;(填序號,下同)互為同素異形體的是_____。
II.現有①金剛石 ②干冰 ③Na2SO4 ④NH4Cl 四種物質,按下列要求回答:
(1)晶體熔化時需要破壞共價鍵的是_____(填序號,下同);
(2)熔點最低的是_______
(3)晶體中只存在一種微粒作用力是_______;
(4)屬于離子晶體的是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組中的兩種物質作用時,反應條件或反應物的用量改變時,對生成物沒有影響的是
A. Na與O2 B. Na2O2與CO2 C. C與O2 D. NaOH與CO2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國明代《本草綱目》中收載藥物1892種,其中“燒酒”條目下寫道:“自元時始創其法,用濃酒和糟入甑,燕令氣.上……其清如水,味極濃烈,蓋酒露也。“”這里所用的“法”是指
A. 萃取 B. 滲析 C. 蒸餾 D. 升華
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、U、W是原子序數依次增大的前四周期元素。其中Y的原子核外有7種運動狀態不同的電子;X、Z中未成對電子數均為2;U是第三周期元索形成的簡單離子中半徑最小的元素;W的內層電子全充滿,最外層只有1個電子。請回答下列問題:
(1)X、Y、Z的第一電離能從大到小的順序是_____________ (用元素符號表示,下同)。
(2)寫出W的價電子排布式__________________________,W同周期的元素中,與W原子最外層電子數相等的元素還有_____________。
(3)X、Y、Z的簡單氫化物的鍵角從大到小的順序是__________________________(用化學式表示),原因是__________________________。
(4)由元素Y與U元素組成的化合物A,晶胞結構如圖所示(黑球表示Y原子,白球表示U原子),請寫出化合物A的化學式_____________,該物質硬度大,推測該物質為_____________晶體。其中Y元素的雜化方式是_____________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知五種元素的原子序數大小順序為C>A>B>D>E,A、C同周期,B、C同主族。A與B形成的離子化合物A2B中所有離子的電子數相同,其電子總數為30;D和E可形成4核10個電子的分子。試回答下列問題:
(1)寫出四種元素的名稱:A________B_______C__________D_________
(2)用電子式表示化合物A2B的形成過程:______________________。
(3)寫出D元素形成的單質的結構式:__________________________。
(4)A、B兩種元素組成的化合物A2B2存在的化學鍵是________________。
(5)寫出下列物質的電子式:E與B形成的化合物__________________;A、B、E形成的化合物_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列描述的化學反應狀態,不一定是平衡狀態的是
A.H2(g)+Br2(g)![]() 2HBr(g) 恒溫、恒容下,反應體系中氣體的顏色保持不變
2HBr(g) 恒溫、恒容下,反應體系中氣體的顏色保持不變
B.2NO2(g) ![]() N2O4(g) 恒溫、恒容下,反應體系中氣體的壓強保持不變
N2O4(g) 恒溫、恒容下,反應體系中氣體的壓強保持不變
C.CaCO3(s) ![]() CO2(g)+CaO(s) 恒溫、恒容下,反應體系中氣體的密度保持不變
CO2(g)+CaO(s) 恒溫、恒容下,反應體系中氣體的密度保持不變
D.3H2(g)+N2(g) ![]() 2NH3(g) 反應體系中H2與N2的物質的量之比保持3∶1
2NH3(g) 反應體系中H2與N2的物質的量之比保持3∶1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com