
700℃時,向容積為2L的密閉容器中充入一定量的CO和H2O,發生反應:
CO(g)+H2O(g) CO2(g)+H2(g)。反應過程中測定的部分數據見下表(表中t2>t1):
CO2(g)+H2(g)。反應過程中測定的部分數據見下表(表中t2>t1):

下列說法正確的是
A.反應在t1 min內的平均速率為v(H2)= mol·L-1·min-1
mol·L-1·min-1
B.保持其他條件不變,起始時向容器中充入0.60mol CO和1.20m ol H2O,到達平衡時n(CO2)=0.40mol
ol H2O,到達平衡時n(CO2)=0.40mol
C.保持其他條件不變,向平衡體系中再通入0.20mol H2O(g),△H增大
D.溫度升高至800℃,上述反應平衡常數為0.64,則正反應為吸熱反應
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源:2015-2016學年遼寧沈陽二中高二6月小班成果驗收化學卷(解析版) 題型:填空題
Ⅰ已知NiXO晶體晶胞結構為NaCl型(如圖),由于晶體缺陷,x值小于1。測知NiXO晶體x=0.88,晶胞邊長為4.28×10-10m 求:(已知: =1.4)
=1.4)

(1)晶胞中兩個Ni原子之間的最短距離___________m(精確至0.01)。
(2)與O2-距離最近且等距離的Ni離子圍成的幾何體形狀___ ____。
(3)晶體中的Ni分別為Ni2﹢、Ni3﹢,求此晶體的化學式_________。
(4)已知,NiO晶體熔點大于NaCl,主要原因是______________________________。
Ⅱ金晶體是面心立方最密 堆積,立方體的每個面上5個金原子緊密堆砌(如圖,其余各面省略),金原子半徑為A cm,求:
堆積,立方體的每個面上5個金原子緊密堆砌(如圖,其余各面省略),金原子半徑為A cm,求:

(1)金的密度為___________ 。(用帶A計算式表示)
。(用帶A計算式表示)
(2)金原子空間占有率為___________。(用帶A計算式表示)
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧沈陽二中高二6月小班成果驗收化學卷(解析版) 題型:選擇題
下列各組晶體物質中,化學鍵類型相同,晶體類型也相同的是( )
①SiO2和SO3 ②晶體硼和HCl ③CO2和SO2 ④晶體硅和金剛石 ⑤晶體氖和晶體氮 ⑥硫黃和碘
A.①②③ B.④⑤⑥ C.③④⑥ D.①③⑤
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧師大附中高一下學期6月月考化學試卷(解析版) 題型:填空題
化學平衡原理在工農業生產中發揮著重要的指導作用。
(1) 反應C(s)+CO2(g) 2CO(g)平衡常數K的表達式為 ;
2CO(g)平衡常數K的表達式為 ;
已知C(s) + H2O(g)  CO(g)+H2(g)的平衡常數為K1;H2(g)+CO2(g)
CO(g)+H2(g)的平衡常數為K1;H2(g)+CO2(g)  CO(g)+H2O(g)的平衡常數為K2 ,則K與K1、K2二者的關系為 。
CO(g)+H2O(g)的平衡常數為K2 ,則K與K1、K2二者的關系為 。
(2)已知某溫度下,反應2SO2+O2 2SO3,的平衡常數K=19 mol·L-1。在該溫度下的體積固定的密閉容器中充入c(SO2)=1mol·L-1,c(O2)=1 mol·L-1,當反應在該溫度下SO2轉化率為80%時,該反應是否達到化學平衡狀態?計算過程和結論如下 :
2SO3,的平衡常數K=19 mol·L-1。在該溫度下的體積固定的密閉容器中充入c(SO2)=1mol·L-1,c(O2)=1 mol·L-1,當反應在該溫度下SO2轉化率為80%時,該反應是否達到化學平衡狀態?計算過程和結論如下 :
(3)若未達到,反應向 (填“正反應”或“逆反應”) 方向進行。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧師大附中高一下學期6月月考化學試卷(解析版) 題型:選擇題
下圖表示反應 N2(g) + 3H2 (g) 2NH3(g);△H=- a kJ/mol (a>0)在某一時間段中反應速率與反應過程的曲線圖,則氨的百分含量最高的一段時間是
2NH3(g);△H=- a kJ/mol (a>0)在某一時間段中反應速率與反應過程的曲線圖,則氨的百分含量最高的一段時間是
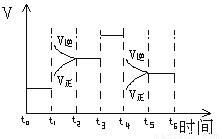
A.t0—t1
B.t2—t3
C.t3—t4
D.t5—t6
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧師大附中高一下學期6月月考化學試卷(解析版) 題型:選擇題
把下列4種X的溶液分別加入4個盛有10mL 2mol/L鹽酸的燒杯中,均加水稀釋到50mL,此時X和鹽酸緩和地進行反應。其中反應速率最大的是
A.20mL 3mol/L的X溶液 B.20mL 2mol/L的X溶液
C.10ml 4mol/L的X溶液 D.10mL 2mol/L的X溶液
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北滄州一中高一上第二次月考化學試卷(解析版) 題型:計算題
有一種白色粉末是無水碳酸鈉和碳酸氫鈉的混合物,稱取4.42g灼燒至恒重,當質量不再變化時稱重質量為3.18g,灼燒后的殘渣能與30mL鹽酸恰好完全反應。試求:原混合物中碳酸氫鈉質量為 ;碳酸鈉質量為 ;所用鹽酸的物質的量濃度 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年貴州貴陽花溪清華中學高一6月月考化學卷(解析版) 題型:選擇題
現有A、B、C、D四種金屬片,①把A、B用導線連接后同時浸入稀硫酸中,A上有氣泡產生;②把C、D用導線連接后同時浸入稀硫酸中,D發生還原反應;③把A、C用導線連接后同時浸入稀硫酸中,電子流動方向為:A→導線→C。根據上述情況判斷四種金屬的活潑性由強到弱的順序為
A.DCAB B.CBAD C.BADC D.BACD
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com