
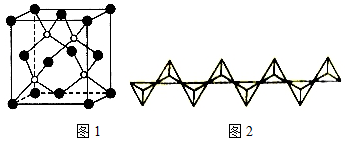
分析 (1)P原子有三個能層;最外層為3s2p3,p軌道的電子云在三維空間中有3個延伸方向,原子軌道為啞鈴形;
(2)同一周期元素自左而右第一電離能呈增大趨勢,但P元素原子3p能級是半滿穩(wěn)定狀態(tài),能量較低,第一電離能高于同周期相鄰元素;
(3)PCl3中P、Cl均滿足8電子穩(wěn)定結構,計算中P的價層電子對數(shù),然后判斷;
(4)先根據(jù)直角三角形計算正四面體的邊長,確定晶胞的邊長,再根據(jù)ρ=$\frac{m}{V}$計算密度;
(5)根據(jù)構造原理寫出基態(tài)鐵原子核外電子排布式;H3[Fe(PO4)3]中PO43-為配體,F(xiàn)e3+為中心離子;
(6)由鏈狀結構可知每個P與3個O形成陰離子,且P的化合價為+5價,以此判斷形成的化合物的化學式.
解答 解:(1)P原子核外有15個電子,分三層排布,即有三個能層,所以電子占據(jù)的最高能層符號為M;最外層為3s2p3,p軌道的電子云在三維空間中沿著x、y、z軸3個方向延伸,p原子軌道為啞鈴形;
故答案為:M;3;啞鈴;
(2)C、N、O元素是同一周期相鄰元素,同一周期元素自左而右第一電離能呈增大趨勢,但P元素原子3p能級是半滿穩(wěn)定狀態(tài),能量較低,第一電離能高于同周期相鄰元素,故第一電離能P>S>Si,
故答案為:P>S>Si;
(3)單質(zhì)磷與Cl2反應,可以生成PCl3和PCl5,PCl3中P、Cl均滿足8電子穩(wěn)定結構,PCl3中P原子的價層電子對數(shù)為3+$\frac{1}{2}$(5-1×3)=4,P原子的雜化軌道類型為sp3,所以分子的空間構型為三角錐型;
故答案為:sp3;三角錐型;
(4)AB、AC、AD、BC、BD、CD的邊長相等,AF、BF的長相等為a,F(xiàn)位于體心上,O位于正三角形BCD的重心上,在正三角形BCD中,BE為三角形BCD的高,則CE為BC的一半,如圖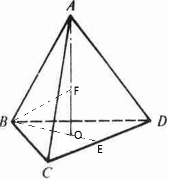 ,
,
設正四面體的邊長為x,CE的長為0.5x,BE=$\sqrt{{x}^{2}-(0.5x)^{2}}$=$\frac{\sqrt{3}}{2}$x,BO與OE的長之比為2:1,則BO的長為=$\frac{\sqrt{3}}{2}x$×$\frac{2}{3}$=$\frac{\sqrt{3}x}{3}$x,在三角形ABO中,AO的長=$\sqrt{{x}^{2}-(\frac{\sqrt{3}}{3}x)^{2}}$=$\frac{\sqrt{6}}{3}x$,在三角形BFO中,OF的長=$\frac{\sqrt{6}}{3}x$-a=$\sqrt{{a}^{2}-(\frac{\sqrt{3}}{3}{x)}^{2}}$,x=$\frac{2}{3}$$\sqrt{6}a$,因正四面體的邊長為x,對角線長2x,晶胞的棱長為2x×$\frac{\sqrt{2}}{2}$=$\sqrt{2}$x=$\frac{4}{3}$$\sqrt{3}a$,
一個晶胞中含有P原子:8×$\frac{1}{8}$+6×$\frac{1}{2}$=4個,B原子在內(nèi)部,共4個,即一個晶胞中含有4個BP,密度的表達式ρ=$\frac{m}{V}$=$\frac{\frac{M}{{N}_{A}}×4}{(\frac{4}{3}\sqrt{3}a)^{3}}$=$\frac{3\sqrt{3}M}{16{N}_{A}{a}^{3}}$;
故答案為:$\frac{3\sqrt{3}M}{16{N}_{A}{a}^{3}}$;
(5)鐵是26號元素,其原子核外有26個電子,根據(jù)構造原理其核外電子排布式為1s22s22p63s23p63d64s2,則基態(tài)Fe3+的核外電子排布式為1s22s22p63s23p63d5;H3[Fe(PO4)3]中PO43-為配體,F(xiàn)e3+為中心離子,中心離子提供空軌道,配體提供孤對電子;
故答案為:1s22s22p63s23p63d5;PO43-;孤對電子;
(6)由鏈狀結構可知每個P與3個O形成陰離子,且P的化合價為+5價,則形成的化合物化學式為NaPO3,故答案為:NaPO3.
點評 本題綜合考查物質(zhì)結構和性質(zhì),為高考常見題型,題目涉及第一電離能的比較、雜化方式的判斷、晶胞的計算、電子排布式、配合物等,側重于基礎知識的綜合應用的考查,題目難度較大,注意把握晶胞的計算方法.


 仁愛英語同步練習冊系列答案
仁愛英語同步練習冊系列答案 學習實踐園地系列答案
學習實踐園地系列答案科目:高中化學 來源: 題型:選擇題
| A. | 反應Z2+2A2+═2A3++2Z-可以進行 | |
| B. | Z元素在反應③中被還原,在反應①中被氧化 | |
| C. | Z2可以置換出X2+溶液中的X | |
| D. | 氧化性由強到弱的順序是XO4-、Z2、B2、A3+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用甘蔗生產(chǎn)的乙醇燃料屬于可再生能源,利用乙醇燃料不會產(chǎn)生溫室氣體 | |
| B. | 低碳生活注重節(jié)能減排,盡量使用太陽能等代替化石燃料,可減少霧霾的發(fā)生 | |
| C. | 太陽能、風能和生物能源屬于新能源 | |
| D. | 太陽能電池可將太陽能直接轉(zhuǎn)化為電能 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 花的種類 | 花汁在酒精中的顏色 | 花汁在稀酸中的顏色 | 花汁在稀堿中的顏色 |
| 玫瑰 | 粉色 | 粉色 | 綠色 |
| 萬壽菊 | 黃色 | 黃色 | 黃色 |
| 大紅花 | 粉色 | 橙色 | 綠色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:1 | B. | 5:1 | C. | 3:13 | D. | 4:15 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 內(nèi)容 | 結論 | |
| A | 一個反應的△H<0△S<0 | 該反應在高溫條件下有利于自發(fā)進行 |
| B | 硝酸銨溶于水可自發(fā)進行(△H>0) | 因為該過程的△S>0 |
| C | H2O(g)變成H2O(l) | △S<0 |
| D | H2(g)+F2(g)═2HF(g)的△H=-271kJ•mol-1,△S=+8J•mol-1•K-1 | 反應在任意溫度下都能自發(fā)進行 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
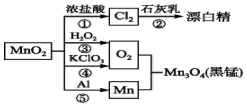
| A. | 反應①②③④⑤均屬于氧化還原反應,反應③還屬于置換反應 | |
| B. | 反應⑤說明該條件下鋁可用于制熔點較高的金屬 | |
| C. | 相同條件下生成等量的O2,反應③和④轉(zhuǎn)移的電子數(shù)之比為1:1 | |
| D. | 反應①中氧化劑與還原劑的物質(zhì)的量之比為1:4 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 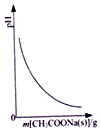 圖表示向CH3COOH溶液中逐步加入CH3COONa固體后,溶液pH的變化 | |
| B. | 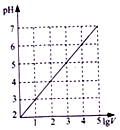 圖表示0.1LpH=2的HC1溶液加水稀釋至VL,pH隨lgV的變化 | |
| C. | 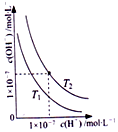 圖表示不同溫度下水溶液中H+和OH-濃度變化的曲線,圖中溫度T2>T1 | |
| D. | 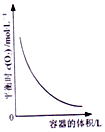 圖表示同一溫度下,再不同容積的容器中進行反應2BaO2(s)?2BaO(S)+O2(g),O2的平衡濃度與容器容積的關系 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com