
| A. | ①② | B. | ②③ | C. | ①③④ | D. | ①②④ |
分析 不用其它試劑即可鑒別,則相互之間反應的現象不同;反之,現象相同時不能鑒別,以此來解答.
解答 解:①均不能與其它兩種物質反應生成沉淀的為Na2SO4,相互滴定,先有沉淀后沉淀消失則所加的是KOH溶液,被滴定的為AlCl3,不用其它試劑即可鑒別,故選;
②藍色溶液為CuSO4,與CuSO4反應生成白色沉淀的為Ba(OH)2,剩余一種為碳酸氫鈉,可鑒別,故選;
③HCl與氫氧化鋇反應無明顯現象,NaCl與其它兩種物質不反應,不用其它試劑不能鑒別,故不選;
④Ba(OH)2與Na2CO3反應生成沉淀,Ba(OH)2與H2SO4反應生成沉淀,且Na2CO3、H2SO4反應生成氣體,則不加其它試劑能鑒別,故選;
故選D.
點評 本題考查物質鑒別和檢驗,為高頻考點,把握物質的性質與發生的反應和現象為解答的關鍵,側重分析與應用能力考查,注意元素化合物知識的綜合應用,題目難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 現代化學元素分析測試中,可用元素分析儀確定物質中是否含有C、H、O、N、S、Cl、Br等元素,用紅外光譜儀確定物質中是否存在某些有機原子團,用原子吸收光譜確定物質中含有哪些金屬元素等 | |
| B. | 鈉鉀合金在常溫下是液體,可用于快中子反應堆作劑;鎂合金大量用于制造火箭、導彈和飛機的部件等 | |
| C. | 2015年浙江省多地遭遇霧霾天氣,有報道稱霧霾顆粒中汽車尾氣占20%以上,一致汽車尾氣中的主要污染物為NOx、CO、燃燒源超細顆粒(PM2.5)等有害物質,其中PM2.5(OM單位為百萬分之一米)顆粒大小約等于膠體粒子 | |
| D. | 如圖所示為四大基本反應及其關系,則反應4NH3+5O2$\frac{\underline{催化劑}}{△}$4NO+6H2O屬于區域3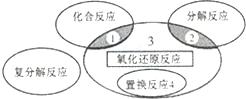 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
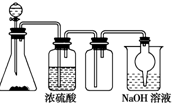 如圖是一套實驗室制取氣體的裝置,用于發生、干燥、收集和吸收有害氣體,下列各組物質能利用這套裝置進行實驗的是
如圖是一套實驗室制取氣體的裝置,用于發生、干燥、收集和吸收有害氣體,下列各組物質能利用這套裝置進行實驗的是| A. | MnO2和濃鹽酸 | B. | Na2SO3(s)和較濃H2SO4 | ||
| C. | Cu片和濃HNO3 | D. | 濃氨水和生石灰 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+、Ca2+、Cl-、SO42- | B. | Fe2+、H+、AlO2-、ClO- | ||
| C. | Fe2+、Na+、Cl-、NO3- | D. | K+、Fe3+、NO3-、SCN- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 粒子半徑:F-<Mg2+<Al3+ | B. | 熱穩定性:HI>HBr>HCl>HF | ||
| C. | 酸性:H2SiO3<H3PO4<H2SO4<HClO4 | D. | 堿性:Al(OH)3>Mg(OH)2>NaOH |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 氫氣是一種清潔能源,氫氣的制取與儲存是氫能源利用領域的研究熱點.
氫氣是一種清潔能源,氫氣的制取與儲存是氫能源利用領域的研究熱點.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 金屬離子 | 開始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com