
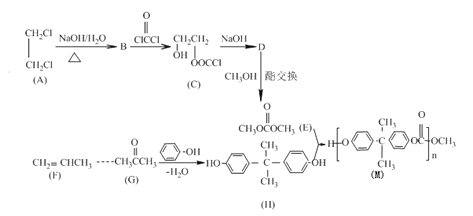
【題目】聚碳酸酯的透光率良好,可制作擋風玻璃、眼鏡片等。某聚碳酸酯(M)的合成路線如下:
已知:
Ⅰ.D的分子式為C3H4O3,核磁共振氫譜只有一組峰
Ⅱ.R1COOR2+R3OH![]() R1COOR3+ R2OH
R1COOR3+ R2OH
(1)A的名稱是 _______,D的結構簡式為_____;
(2)B→C的反應類型______;
(3)關于H的說法正確的是(_______)
A.分子式為C15H16O2
B.呈弱酸性,是苯酚的同系物
C.分子中碳原子可能共面
D.1mol H與濃溴水取代所得有機物最多消耗NaOH10mol
(4)寫出A→B化學方程式________;
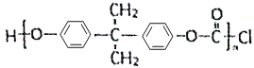
(5)最常見的聚碳酸酯是用H與光氣(![]() )聚合得到,請寫出該聚碳酸酯的結構簡式________;
)聚合得到,請寫出該聚碳酸酯的結構簡式________;
(6)H的同分異構體中滿足下列條件的有___種;
①有萘環(![]() )結構 ②能發生水解和銀鏡反應 ③兩個乙基且在一個環上
)結構 ②能發生水解和銀鏡反應 ③兩個乙基且在一個環上
(7)F→G需三步合成
CH2=CHCH3![]() K
K![]() L
L
若試劑1為HBr,則L的結構簡式為_______,③的反應條件是_____。
【答案】1,2-二氯乙烷 ![]() 取代反應 AD
取代反應 AD 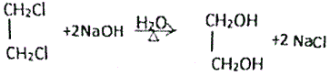
 18
18 ![]() Cu/Ag,O2,△
Cu/Ag,O2,△
【解析】
根據流程圖,鹵代烴A(![]() )在氫氧化鈉溶液中水解生成B,B為
)在氫氧化鈉溶液中水解生成B,B為![]() ,C(
,C(![]() )在氫氧化鈉條件下反應生成D,D與甲醇發生酯交換生成E(
)在氫氧化鈉條件下反應生成D,D與甲醇發生酯交換生成E(![]() ),D的分子式為C3H4O3,核磁共振氫譜只有一組峰,因此D為
),D的分子式為C3H4O3,核磁共振氫譜只有一組峰,因此D為![]() ,據此分析解答(1)~(6);
,據此分析解答(1)~(6);
(7)CH2=CHCH3與HBr發生加成反應生成CH3CHBrCH3,CH3CHBrCH3水解生成CH3CHOHCH3,最后將CH3CHOHCH3氧化即可得到丙酮,據此分析解答。
(1)A的結構簡式為![]() ,名稱為1,2-二氯乙烷,D的結構簡式為
,名稱為1,2-二氯乙烷,D的結構簡式為![]() ,故答案為:1,2-二氯乙烷;
,故答案為:1,2-二氯乙烷;![]() ;
;
(2)B為![]() ,C為
,C為![]() ,B與
,B與![]() 發生取代反應生成,故答案為:取代反應;
發生取代反應生成,故答案為:取代反應;
(3)H為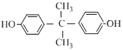 。A.根據H的結構簡式,H的分子式為C15H16O2,故A正確;B.H中含有酚羥基,具有弱酸性,但含有2個苯環,不屬于苯酚的同系物,故B錯誤;C.結構中含有
。A.根據H的結構簡式,H的分子式為C15H16O2,故A正確;B.H中含有酚羥基,具有弱酸性,但含有2個苯環,不屬于苯酚的同系物,故B錯誤;C.結構中含有![]() ,是四面體結構,因此分子中碳原子一定不共面,故C錯誤;D.酚羥基的鄰位和對位氫原子能夠發生取代反應,1mol H與濃溴水取代所得有機物中最多含有4個溴原子,酚羥基和溴原子均能消耗NaOH,且溴原子水解生成的酚羥基也能與氫氧化鈉反應,因此1mol
,是四面體結構,因此分子中碳原子一定不共面,故C錯誤;D.酚羥基的鄰位和對位氫原子能夠發生取代反應,1mol H與濃溴水取代所得有機物中最多含有4個溴原子,酚羥基和溴原子均能消耗NaOH,且溴原子水解生成的酚羥基也能與氫氧化鈉反應,因此1mol 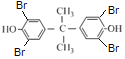 最多消耗10mol氫氧化鈉,故D正確,故答案為:AD;
最多消耗10mol氫氧化鈉,故D正確,故答案為:AD;
(4)A→B是鹵代烴的水解反應,反應的化學方程式為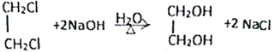 ,故答案為:
,故答案為: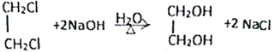 ;
;
(5)最常見的聚碳酸酯是用H與光氣(![]() )聚合得到,
)聚合得到, 與
與![]() 發生縮聚反應生成
發生縮聚反應生成 ,故答案為:
,故答案為: ;
;
(6)H(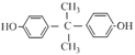 )的不飽和度=8,H的同分異構體中滿足下列條件:①有萘環(
)的不飽和度=8,H的同分異構體中滿足下列條件:①有萘環(![]() )結構,不飽和度=7,②能發生水解和銀鏡反應,說明結構中含有酯基和醛基,因此屬于甲酸酯類物質,酯基的不飽和度=1,因此其余均為飽和結構,③兩個乙基且在一個環上,兩個乙基在一個環上有
)結構,不飽和度=7,②能發生水解和銀鏡反應,說明結構中含有酯基和醛基,因此屬于甲酸酯類物質,酯基的不飽和度=1,因此其余均為飽和結構,③兩個乙基且在一個環上,兩個乙基在一個環上有![]() 、
、![]() 、
、![]() 、
、![]() 4種情況,HCOO-的位置分別為6、6、3、3,共18種結構,故答案為:18;
4種情況,HCOO-的位置分別為6、6、3、3,共18種結構,故答案為:18;
(7)CH2=CHCH3與HBr發生加成反應生成CH3CHBrCH3,CH3CHBrCH3水解生成CH3CHOHCH3,最后將CH3CHOHCH3氧化即可得到丙酮,因此L為CH3CHOHCH3,反應③的條件為Cu/Ag,O2,△,故答案為:CH3CHOHCH3;Cu/Ag,O2,△。


科目:高中化學 來源: 題型:
【題目】丁子香酚可用于制備殺蟲劑和防腐劑,結構簡式如右下圖所示。下列說法中,不正確的是

A. 丁子香酚可通過加聚反應生成高聚物
B. 丁子香酚分子中的含氧官能團是羥基和醚鍵
C. 1 mol丁子香酚與足量氫氣加成時,最多能消耗4 mol H2
D. 丁子香酚能使酸性KMnO4溶液褪色,可證明其分子中含有碳碳雙鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了探究原電池和電解池的工作原理,某研究性學習小組分別用下圖所示的裝置進行實驗。據圖回答問題。
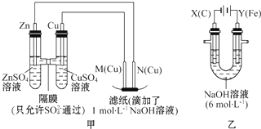
I.用圖甲所示裝置進行第一組實驗時:
(1)在保證電極反應不變的情況下,不能替代Cu作電極的是_____ (填字母)。
A石墨 B. 鎂 C.銀 D.鉑
(2)實驗過程中,SO42-____(填“從左向右”“從右向左”或“不”)移動;濾紙上能觀察到的現象是________________。
II.該小組同學用圖乙所示裝置進行第二組實驗時發現,兩極均有氣體產生,且Y極處溶液逐漸變成紫紅色;停止實驗觀察到鐵電極明顯變細,電解液仍然澄清。查閱資料知,高鐵酸根(FeO42-)在溶液中呈紫紅色。請根據實驗現象及所查信息,回答下列問題:
(3)電解過程中,X極處溶液的OH-濃度____(填“增大”“減小”或“不變)。
(4)電解過程中,Y極發生的電極反應為___________________,_________________。
(5)電解進行一段時間后,若在X極收集到672mL氣體,Y電板(鐵電極)質量減小0.28g,則在Y極收集到氣體為____mL(均己折算為標準狀況時氣體體積)。
(6)K2FeO4-Zn也可以組成堿性電池,K2FeO4在電池中作為正極材料,其電池反應總反應式為2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,該電池正極發生的電極反應式為_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種用于驅動潛艇的液氨![]() 液氧燃料電池原理示意如圖,下列有關該電池說法正確的是
液氧燃料電池原理示意如圖,下列有關該電池說法正確的是

A.該電池工作時,每消耗![]()
![]() 轉移3mol電子
轉移3mol電子
B.電子由電極A經外電路流向電極B
C.電池工作時,![]() 向電極B移動
向電極B移動
D.電極B上發生的電極反應為:![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】人們對含硼(元素符號為“B”)物質結構的研究,極大地推動了結構化學的發展。回答下列問題:
(1)基態B原子價層電子的電子排布式為_____,核外電子占據最高能層的符號是____,占據該能層未成對電子的電子云輪廓圖形狀為____。
(2)1923年化學家Lewis提出了酸堿電子理論。酸堿電子理論認為:凡是可以接受電子對的物質稱為酸,凡是可以給出電子對的物質稱為堿。已知BF3與F-反應可生成BF4-,則該反應中BF3屬于____(填“酸”或“堿”),原因是____。
(3)NaBH4是有機合成中常用的還原劑,NaBH4中的陰離子空間構型是_____,中心原子的雜化形式為____,NaBH4中存在____(填標號)
a.離子鍵 b.金屬鍵 c.σ鍵 d.π鍵 e.氫鍵
(4)請比較第一電離能:IB____IBe(填“>”或“<”),原因是_______。
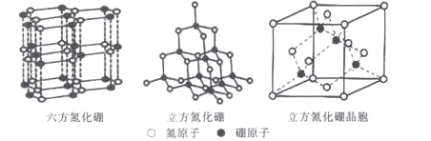
(5)六方氮化硼的結構與石墨類似,B—N共價單鍵的鍵長理論值為158pm,而六方氮化硼層內B、N原子間距的實測值為145 pm,造成這一差值的原因是____。高溫高壓下,六方氮化硼可轉化為立方氮化硼,立方氮化硼的結構與金剛石類似,已知晶胞參數中邊長為a=362 pm,則立方氮化硼的密度是____g/cm3。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關電解質溶液的說法正確的是
A. 向0.1mol/LCH3COOH溶液中加入少量水,溶液中c(H+)/c(CH3COOH)減小
B. 將CH3COONa溶液從20℃升溫至30℃,溶液中c(CH3COO-)/c(CH3COOH)·c(OH-)增大
C. 向鹽酸中加入氨水至中性,溶液中c(NH4+)/c(Cl-)>1
D. 向AgCl、AgBr的飽和溶液中加入少量硝酸銀,溶液中c(Cl-)/c(Br-)不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】三硫化磷(P4S3)是黃綠色針狀晶體,易燃、有毒,分子結構之一如圖所示,已知其燃燒時P被氧化為P4010,下列有關P4S3的說法中不正確的是

A. P4S3中磷元素為+3價
B. P4S3屬于共價化合物
C. P4S3充分燃燒的化學方程式為P4S3+8O2=P4O10+3SO2
D. 1mol P4S3分子中含有9mol共價鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物的元素定量分析最早是由德國人李比希提出的,某實驗室模擬李比希法測定某種氨基酸(CxHyOzNp)的分子組成。取一定量的該氨基酸放在純氧氣中燃燒,燃燒后生成的水用裝置D(無水氯化鈣)吸收,二氧化碳用裝置C(KOH濃溶液)吸收,N2的體積用E裝置進行測量,所需裝置如下圖(夾持儀器的裝置及部分加熱裝置已略去):

(1)該實驗裝置的合理連接順序為:A、__、E。(部分裝置可以重復選用)
(2)實驗開始時,首先打開止水夾a,關閉止水夾b,通一段時間的純氧,這樣做的目的是_____。
(3)A中放入CuO的作用是_______,裝置B的作用是_____。
(4)為了確定此氨基酸的分子式,除了準確測量N2的體積、生成二氧化碳和水的質量外,還需得到的數據有___。
(5)在讀取E裝置中所排水的體積時,液面左低右高,則所測氣體的體積____(填“偏大”、“偏小”或“無影響”)。
(6)已知分子式為C2H4O2的有機物也含有氨基酸中的某個官能團,請設計實驗證明該官能團(試劑任選):____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對下列物質進行分類(均填序號)。互為同素異形體的是_______;互為同分異構體的是_______;互為同系物的是________.
①16O 和18O ②12C60與13C70③O2和O3 ④CH3CH2OH和CH3OCH3⑤正戊烷和異戊烷⑥ CH4和CH3CH2CH2CH3⑦ 和
和 ;⑧H2O與H2O2⑨金剛石與水晶
;⑧H2O與H2O2⑨金剛石與水晶
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com