
四種元素X、Y、Z、W位于元素周期表的前四周期,已知它們的核電荷數
依次增加,且核電荷數之和為51;Y原子的L層p軌道中有2個電子;Z與Y原子的價層電子數相同;W原子的L層電子數與最外層電子數之比為4:1,其d軌道中的電子數與最外層電子數之比為5:1。
(1)Y、Z可分別與X形成只含一個中心原子的共價化合物a、b,它們的分子式分別是_____、_______; 雜化軌道分別是________、_________;a分子的立體結構是____________。
(2)Y的最高價氧化物和Z的最高價氧化物的晶體類型分別是_______晶體、_______晶體:
(3)X的氧化物與Y的氧化物中,分子極性較小的是(填分子式)__________;
(4)Y與Z比較,電負性較大的____________, 其+2價離子的核外電子排布式是_________
(1)CH4 SiH4 sp3 sp3 正四面體![]()
![]()
![]()
![]()
![]()
![]()
![]()
(2)分子 原子
(3)CO2
(4)C 1s22s2
由“Y原子的L層p軌道中有2個電子”可知Y原子的電子排布式是1s22s22p2,
為碳元素;由“Z與Y原子的價層電子數相同”可知Z與碳元素同主族,又因Z位于元素周期表的前四周期且核電荷數大于Y,所以Z可能為硅元素(14號)或鍺元素(32號),若Z為鍺元素,則四種元素的核電荷數之和大于51(因W的核電荷數比Z的還要大),即Z只能為硅元素;由“W原子的L層電子數與最外層電子數之比為4︰1”可知W的最外層電子數為2,由“d軌道中的電子數與最外層電子數之比為5︰1”可知d軌道中的電子數為10,所以W原子的電子排布式是1s22s22p63s23p63d104s2,即W為鋅元素;又因四種元素的核電荷數之和為51,所以X元素的核電荷數為1,是氫元素。


科目:高中化學 來源: 題型:
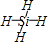
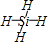
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
四種元素X、Y、Z、W位于元素周期表的前四周期,已知它們的核電荷數依次增加,且核電荷數之和為51;Y原子的L層p軌道中有2個電子;Z與Y原子的價層電子數相同;W原子的L層電子數與最外層電子數之比為4:1,其d軌道中的電子數與最外層電子數之比為5:1。
(1)Y、Z可分別與X形成只含一個中心原子的共價化合物a、b,它們的分子式分別是__________________、_____________________;雜化軌道分別是_________________、_________________;a分子的立體結構是_________________;
(2)Y的最高價氧化物和Z的最高價氧化物的晶體類型分別是______________晶體、_______________晶體;
(3)X的氧化物與Y的氧化物中,分子極性較小的是(填分子式)_________________;
(4)Y與Z比較,電負性較大的是(填元素符號)_________________;
(5)W的元素符號是____________,其+2價離子的核外電子排布式是_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
四種元素X、Y、Z、W位于元素周期表的前四周期,已知它們的核電荷數依次增加,且核電荷數之和為51;Y原子的L層p軌道中有2個電子;Z與Y原子的價層電子數相同;W原子的L層電子數與最外層電子數之比為4:1,其d軌道中的電子數與最外層電子數之比為5:1。
(1)Y、Z可分別與X形成只含一個中心原子的共價化合物a、b,它們的分子式分別是__________________、_____________________;雜化軌道分別是_________________、_________________;a分子的立體結構是_________________;
(2)Y的最高價氧化物和Z的最高價氧化物的晶體類型分別是______________晶體、_______________晶體;
(3)X的氧化物與Y的氧化物中,分子極性較小的是(填分子式)_________________;
(4)Y與Z比較,電負性較大的是(填元素符號)_________________;
(5)W的元素符號是____________,其+2價離子的核外電子排布式是_________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com