
【題目】下列屬于物理變化的是
A.焰色反應B.煤的液化C.烴的裂解D.氫氧化鈉溶液導電的過程
 備戰中考寒假系列答案
備戰中考寒假系列答案科目:高中化學 來源: 題型:
【題目】含等物質的量NaOH的溶液分別用pH為2和3的CH2COOH溶液中和,設消耗CH2COOH溶液的體積依次為Va、Vb,兩者的關系正確的是
A. Va>10Vb B. Va=10Vb C. Va<10Vb D. Va>10Vb
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲乙兩燒杯中分別裝有相同體積、相同pH的氨水和NaOH溶液,各加入10mL0.1mol/LA1C13 溶液,兩燒杯中都有沉淀生成。下列判斷正確的是( )
A. 甲中沉淀一定比乙中多 B. 乙中沉淀可能比甲中的多
C. 甲中沉淀一定比乙中的少 D. 甲中和乙中的沉淀可能一樣多
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金屬鋁在生產生活中有廣泛用途。
(1)鋁元素在元素周期表中位于______________。
(2)用化學方程式表示工業制備鋁單質______________。 鋁熱反應可用于焊接鋼軌,下圖為鋁熱反應的實驗裝置圖。

(3) 該鋁熱反應的化學方程式是______________。鋁熱反應的反應現象說明反應物的總能量___________生成物的總能量(填“<”、“>”或“=”)。
(4)鋁熱反應在工業上用于冶煉______________金屬(填編號)。
A. 強還原性 B. 難熔性 C. 易導電 D. 活潑
(5)反應結束后,從沙中取出生成的固體物質,有同學推測該固體是鐵鋁合金,他設計了如下實驗證明此 固體中含有金屬鋁:取少量固體于試管中,滴加______________,當觀察到______________現象時,證明固體中含有金屬鋁。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫化堿法是工業上制備Na2S2O3的方法之一,反應原理為:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2(該反應△>0)某研究小組在實驗室用硫化堿法制備Na2S2O3·5H2O流程如下。

(1)吸硫裝置如圖所示。

①裝置B的作用是檢驗裝置中SO2的吸收效率,B中試劑是________,表明SO2吸收效率低的實驗現象是B中溶液________________。
②為了使SO2盡可能吸收完全,在不改變A中溶液濃度、體積的條件下,除了及時攪拌反應物外,還可采取的合理措施是_______、_______。(寫出兩條)
(2)假設本實驗所用的Na2CO3含少量NaCl、NaOH,設計實驗方案進行檢驗。(室溫時CaCO3飽和溶液的pH=12), 限用試劑及儀器:稀硝酸、AgNO3溶液、CaCl2溶液、Ca(NO3)2溶液、酚酞溶液、蒸餾水、pH計、燒杯、試管、滴管、
序號 | 實驗操作 | 預期現象 | 結論 |
① | 取少量樣品于試管中,加入適量蒸餾水,充分振蕩溶解,_________。 | 有白色沉淀生成 | 樣品含NaCl |
② | 另取少量樣品于燒杯中,加入適量蒸餾水,充分振蕩溶解,_________。 | 有白色沉淀生成,上層清液pH>10.2 | 樣品含NaOH |
(3)Na2S2O3溶液是定量實驗中的常用試劑,測定其濃度的過程如下:
第一步:準確稱取ag KIO3(相對分子質量:214)固體配成溶液,
第二步:加入過量KI固體和H2SO4溶液,滴加指示劑,
第三步:用Na2S2O3溶液滴定至終點,消耗Na2S2O3溶液溶液的體積為vmL 則c(Na2S2O3溶液)=_______mol·L-1。(只列出算式,不作運算)
已知:IO3-+I-+6H+=3I2+3H2O ,2S2O32-+I2=S4O62-+2I- 某同學第一步和第二步的操作都很規范,第三步滴速太慢,這樣測得的Na2S2O3的濃度可能_____(填“不受影響”、“偏低”或“偏高”) ,原因是________(用離子方程式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知X、Y、Z、W四種短周期元素的原子序數依次增大,其中X與Y、Z、W所形成的常見化合物(10e或18e)在常溫下均為氣態,在元素周期表中Z與W相鄰,Y的最高價氧化物的水化物與其氫化物反應生成鹽,且Y的核電荷數與W的外成層電子數相同。
(1)Z離子的結構示意圖是_____________________________。
(2)X、Y、W可組成一種化合物,原子個數比為4:1:1,該化合物的化學式是_______,其中含有的化學鍵有__________________。
(3)X與Y所形成的分子的電子式為__________,它比同主族其他元素的氫化物沸點高的原因是__________________。
(4)請從Z、W的結構上說明Z、W兩種元素非金屬性的強弱_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在密閉容器中充入4 mol A,在一定溫度和體積可變的密閉容器中發生如下反應:4A(g) ![]() 3B(g)+C(g);ΔH<0,達到平衡時有30%的A發生反應,下列判斷正確的是
3B(g)+C(g);ΔH<0,達到平衡時有30%的A發生反應,下列判斷正確的是
A. 若向密閉體系內再加入3molB、2molC,達平衡時C的百分含量與原平衡相同
B. 達到平衡時氣體的總物質的量、密度都不發生變化
C. 反應達平衡的過程中,釋放出的熱量不發生變化
D. 升高溫度A的轉化率大于30%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物M(C16H14O2)是一種香料,工業上利用烴A和甲苯為主要原料,按下列路線合成:

已知:①氣態烴A在標準狀況下的密度是1.25 g/L;
②醛在堿性溶液中能發生羥醛縮合反應,再脫水生成不飽和醛:
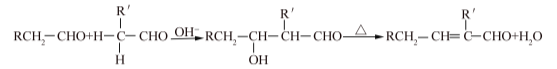 。
。
請回答下列問題:
(1)F的名稱是_____________;G中含有的官能團名稱是_________________。
(2)寫出D→E的化學方程式_______________________________________。
(3)A→B的反應類型是________________;M的結構簡式是____________________。
(4)同時滿足下列條件的K的同分異構體有_____種(不考慮立體異構)。
①遇FeCl3溶液發生顯色反應
②能發生銀鏡反應
③除苯環以外不再含有其他環狀結構
其中核磁共振氫譜為五組峰的結構簡式為_______________。
(5)以乙醇為起始原料,選用必要的無機試劑合成1-丁烯,寫出合成路線(用結構簡式表示有機物),用箭頭表示轉化關系,箭頭上注明試劑和反應條件)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】當光線通過下列分散系:①有塵埃的空氣 ②稀硫酸 ③NaCl溶液 ④墨水 ⑤稀豆漿 ⑥Fe(OH)3膠體。能觀察到丁達爾現象的是
A. ②③ B. ④⑤ C. ①②⑤ D. ①④⑤⑥
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com