
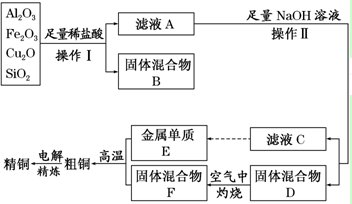
分析 某礦渣(含有Cu2O、Al2O3,Fe2O3、SiO2)加足量的稀鹽酸,過濾,濾液A含有Cu2+、Al3+、Fe2+;固體混合物B為二氧化硅和Cu;濾液A中加足量的NaOH溶液,生成偏鋁酸鈉、氫氧化鐵沉淀和氫氧化銅沉淀,過濾,濾液C為偏鋁酸鈉,偏鋁酸鈉經過一系列操作可以制得E(Al),固體混合物D為氫氧化鐵沉淀和氫氧化銅沉淀,灼燒氫氧化鐵沉淀和氫氧化銅沉淀得到固體混合物F(氧化鐵和氧化銅),氧化鐵和氧化銅混合物發生鋁熱反應生成Cu和Fe,電解得到純銅.
(1)根據分離溶液和沉淀;根據灼燒過程所需要用到的儀器分析即可;
(2)依據提取流程圖可知,加入過量鹽酸,氧化鐵和氧化鋁全部溶解為氯化鐵和氯化鋁溶液,Cu2O與鹽酸反應生成氯化銅、銅和水,生成的銅能與氯化鐵反應生成氯化亞鐵和氯化銅,二氧化硅不溶于鹽酸為沉淀;三價鐵離子與KSCN溶液發生反應生成紅色物質來檢驗三價鐵離子;
(3)根據鋁熱反應的原理來書寫;
(4)設溶液的PH為X,然后求出由水電離出的c(OH-),利用由水電離出的c(OH-)前者為后者的108倍求出X;
(5)a.電能轉化為化學能、熱能;
b.粗銅接電源正極,失去電子,發生氧化反應
c.精銅作陰極,電解后電解液中Cu2+濃度減小
d.粗銅精煉時通過的電量與陰極析出銅的量存在關系;
(6)設計方案的主要步驟是將濃硫酸用蒸餾水稀釋,將樣品與稀硫酸充分反應后,過濾,干燥,稱量剩余固體銅的質量即可.
解答 解:某礦渣(含有Cu2O、Al2O3,Fe2O3、SiO2)加足量的稀鹽酸,過濾,濾液A含有Cu2+、Al3+、Fe2+;固體混合物B為二氧化硅和Cu;濾液A中加足量的NaOH溶液,生成偏鋁酸鈉、氫氧化鐵沉淀和氫氧化銅沉淀,過濾,濾液C為偏鋁酸鈉,偏鋁酸鈉經過一系列操作可以制得E(Al),固體混合物D為氫氧化鐵沉淀和氫氧化銅沉淀,灼燒氫氧化鐵沉淀和氫氧化銅沉淀得到固體混合物F(氧化鐵和氧化銅),氧化鐵和氧化銅混合物發生鋁熱反應生成Cu和Fe,電解得到純銅.
(1)實驗操作I步驟中分離溶液和沉淀的操作名稱為過濾,在空氣中灼燒固體混合物D時,所用到的儀器有坩堝、泥三角、三角架、酒精燈,玻璃棒,
故答案為:過濾;坩堝;
(2)依據提取流程圖可知,加入過量鹽酸,氧化鐵和氧化鋁全部溶解為氯化鐵和氯化鋁溶液,Cu2O與鹽酸反應生成氯化銅、銅和水,生成的銅能與氯化鐵反應生成氯化亞鐵和氯化銅,方程式為:2FeCl3+Cu═2FeCl2+CuCl2,二氧化硅不溶于鹽酸為沉淀,所以濾液A中鐵元素的存在形式為亞鐵離子,可用氯水將其氧化成三價鐵離子,三價鐵離子與KSCN溶液發生反應生成紅色物質來檢驗三價鐵離子,
故答案為:Fe2+;2Fe3++Cu═2Fe2++Cu2+;硫氰化鉀溶液和新制氯水;
(3)鋁與氧化鐵發生鋁熱反應的化學方程式為:2Al+Fe2O3$\frac{\underline{\;高溫\;}}{\;}$2Fe+Al2O3,故答案為:2Al+Fe2O3$\frac{\underline{\;高溫\;}}{\;}$2Fe+Al2O3;
(4)設溶液的PH為X,NaAlO2溶液中由水電離出的c(OH-)=10X-14mol/L,NaOH溶液中由水電離出的c(OH-)=10-Xmol/L,$\frac{1{0}^{X-14}}{1{0}^{-X}}$=108,解得X=11,
則溶液中氫離子濃度:c(H+)=10-11mol/L,即pH=11;
故答案為:11;
(5)a.電能部分轉化為化學能,故a錯誤;
b.粗銅接電源正極,失去電子,發生氧化反應,故b正確;
c.精銅作陰極,電解后電解液中Cu2+濃度減小,故c正確;
d.粗銅精煉時通過的電量與陰極析出銅的量存在關系:電路中通過3.01×1023個電子,得到精銅的質量為16g,故d錯誤;
故選:b.c;
(6)設計方案的主要步驟是將濃硫酸用蒸餾水稀釋,將樣品與稀硫酸充分反應后,過濾,干燥,稱量剩余固體銅的質量即可;
故答案為:將濃硫酸用蒸餾水稀釋,將樣品與稀硫酸充分反應.
點評 本題以礦渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取銅為背景,考查考查物質的制備以及分離和提純等知識,側重于考查學生綜合運用化學知識的能力,為高考常見題型,難度中等.


科目:高中化學 來源: 題型:選擇題
 常溫下,0.2mol•L-1NaHA 與等濃度等體積的 NaOH 溶液混合,所得溶液中部分微粒組分及濃度如圖所示,下列說法正確的是( )
常溫下,0.2mol•L-1NaHA 與等濃度等體積的 NaOH 溶液混合,所得溶液中部分微粒組分及濃度如圖所示,下列說法正確的是( )| A. | NaHA 溶液顯酸性 | B. | 混合溶液中 c(OH-)、c(H+)相等 | ||
| C. | 圖中 X、Y、Z 分別代表 OH-、HA-、H+ | D. | 混合溶液中:c(Na+)═c(H2A)+c(HA-)+c(A2-) |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 鐵和稀硫酸反應:2Fe+6H+=2Fe3++3H2↑ | |
| B. | 少量NaHCO3溶液與Ca(OH)2溶液反應:OHˉ+HCO3ˉ+Ca2+=CaCO3↓+H2O | |
| C. | 鈉和冷水反應:2Na+2H2O=2 Na++2OHˉ+H2↑ | |
| D. | 過量的CO2和氫氧化鈣溶液的反應 OHˉ+CO32-=HCO3ˉ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH3、P4、C10H8 | B. | PCl3、CO2、H2SO4 | C. | SO2、SiO2、P2O5 | D. | CCl4、H2O、Na2O2 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
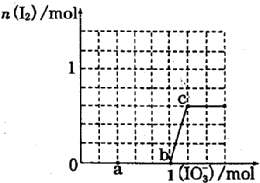 已知:還原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入NaIO3溶液.加入NaIO3的物質的量和和析出的I2的物質的量的關系曲線如圖.下列說法正確的是( )
已知:還原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入NaIO3溶液.加入NaIO3的物質的量和和析出的I2的物質的量的關系曲線如圖.下列說法正確的是( )| A. | 反應過程中的氧化產物均為Na2SO4 | |
| B. | a 點時消耗NaHSO3的物質的量為1.0mol | |
| C. | 0~b間的反應可用如下離子方程式表示:3HSO3-+IO3-=3SO42-+I-+3H+ | |
| D. | 當溶液中I-與I2的物質的量之比為5:3時,加入的NaIO3為1.1mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
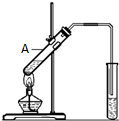 乙酸是食醋的主要成分,它具有以下化學性質:
乙酸是食醋的主要成分,它具有以下化學性質:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
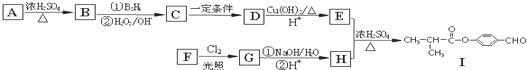
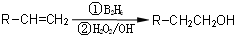
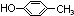 .
. .
.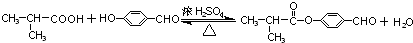 .
.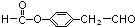 (鄰、間、對任寫一種即可).
(鄰、間、對任寫一種即可).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 僅有實驗①可推出肯定含有SO42-,不含Cl- | |
| B. | 該無色溶液肯定含有NH4+、K+、Al3+、SO42- | |
| C. | 該無色溶液中肯定不含K+、Mg2+、HCO3-、Cl-、MnO4-、I- | |
| D. | 不能確定該無色溶液是否含有K+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 32g O2 | B. | 0.2mol N2 | ||
| C. | 3.01×1023個CO2分子 | D. | 標準狀況下11.2L H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com