
【題目】最近中央電視二臺報道,市場抽查吸管合格率較低,存在較大的安全隱患,其中塑化劑超標是一個主要方面,塑化劑種類繁多,其中鄰苯二甲酸二酯是主要的一大類,![]() (代號DMP)是一種常用的酯類化劑,其蒸氣對氫氣的相對密度為97。工業上生產DMP的流程如圖所示:
(代號DMP)是一種常用的酯類化劑,其蒸氣對氫氣的相對密度為97。工業上生產DMP的流程如圖所示:

已知:R-X+NaOH![]() R-OH+NaX
R-OH+NaX
(1)上述反應⑤的反應類型為___________________。
(2)D中官能團的名稱為___________________。
(3)DMP的結構簡式為___________________。
(4)B→C的化學方程式為_____________________________。
【答案】 取代反應(酯化反應) 羧基 
【解析】鄰二甲苯和氯氣在一定條件下發生取代反應生成氯代烴A,A和氫氧化鈉的水溶液發生取代反應生成醇B,B被氧氣氧化生成生成醛C,C被氧氣氧化生成羧酸D,D和醇發生酯化(取代)反應生成DMP,根據DMP的結構知鄰二甲苯中甲基上1個氫原子被氯原子取代,所以A的結構簡式為:![]() ,B是
,B是![]() ,C是
,C是![]() ,D是
,D是![]() ,鄰二苯甲酸和醇發生酯化反應生成DMP,DMP蒸氣對氫氣的相對密度為97,則DMP的相對分子質量為194,則該醇是甲醇,故DMP的結構簡式為:
,鄰二苯甲酸和醇發生酯化反應生成DMP,DMP蒸氣對氫氣的相對密度為97,則DMP的相對分子質量為194,則該醇是甲醇,故DMP的結構簡式為:![]() ,據此答題。
,據此答題。
(1)根據上面的分析可知,上述轉化中⑤屬于取代反應;故答案為:取代反應(酯化反應);
![]() 中官能團的名稱為羧基;
中官能團的名稱為羧基;
DMP的結構簡式為:![]() ,
,
故答案為:![]() ;
;
B→C的反應是醇的催化氧化化反應,化學方程式為![]() .
.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】用1~18號元素及其形成的化合物的化學式填空。
(1)原子半徑最小的元素是________。
(2)除稀有氣體元素外,原子半徑最大的元素是________,它的原子結構示意圖是________。
(3)與水反應最劇烈的金屬是________。
(4)最高價氧化物對應的水化物堿性最強的是________。
(5)最高價氧化物對應的水化物為兩性氫氧化物的是________。
(6)氣態氫化物的水溶液呈堿性的元素是________。
(7)最穩定的氣態氫化物是________。
(8)金屬性最強的元素是________,非金屬性最強的元素是________。
(9)最高價氧化物對應的水化物酸性最強的是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,分別取未知濃度的MOH和HA溶液,加水稀釋至原體積的n倍。稀釋過程中,兩溶液pH的變化如下圖所示。下列敘述正確的是

A. MOH為弱堿,HA為強酸
B. 水的電離程度:X=Z>Y
C. 若升高溫度,Y、Z點對應溶液的pH均不變
D. 將X點溶液與Z點溶液等體積混合,所得溶液呈堿性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】三氯化硼(BCl3)是一種重要的化工原料,可用于制取乙硎烷(B2H6),也可做有機合成的催化劑。某興趣小組選用下列裝置制備BCl3。

查閱資料:
①BCl3的沸點為12.5℃,熔點為-107.3℃,易水解;
②2B+6HCl![]() 2BCl3+3H2
2BCl3+3H2
請回答下列問題:
(1)裝置A中盛濃鹽酸的儀器名稱為_________;裝置A中發生反應的離子方程為___________。
(2)按氣流方向連接各裝置的接口,順序為a→___→___→___→___→b→c→f→g→h,連接好裝置后的第一步實驗操作為_________。
(3)裝置C中盛放的試劑為_________,實驗中若不用裝置C,可能產生的危險為_________。
(4)裝置E的作用為__________________。
(5)常溫下, KSP[Mn(OH)2]=1.0×10-13,向制取Cl2后的殘余液中加入氫氧化鈉溶液至Mn2+沉淀完全[c(Mn2+)≤1.0×10-5mol·L-1]溶液的PH最小為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎂、鋅等金屬與H2O2可形成“金屬-H2O2”電池,能為潛水器提供動力,可用食鹽水作為電解質溶液,如下圖所示。下列有關Zn-H2O2電池的說法正確的是

A. 電流從Zn電極沿導線流向Pt電極
B. Pt為正極,電極反應為:H2O2+2e-=2OH-
C. 每消耗6.5gZn,將反應0.05molH2O2
D. 食鹽水中Cl-向Pt電極移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“低碳生活,綠色出行”已經成為很多人的生活理念。CO2的捕捉和利用也成為了科學家們積極探索的熱門領域。回答下列問題:
(1)用CO2催化加氫可制取乙烯,其能量關系如圖1,寫出該反應的熱化學方程式____________。

(2)以硫酸作電解質溶液,利用太陽能電池將CO2轉化為乙烯的工作原理如圖2。則A為電池的___極,N極的電極反應式為_________________________。
(3)用CO2催化加氫制取二甲醚的反應為:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)
在恒容密閉容器中,均充入2mol.CO2和6molH2,分別以Ir和Ce作催化劑,反應進行相同的時間后測得的CO2的轉化率a(CO2)隨反應溫度的變化情況如圖3。

①用Ir和Ce作催化劑時,反應的活化能更低的是_______。
②a、b、c、d和e五種狀態,反應一定達到平衡狀態的是__________,反應的△H ___0(填“>”、“=”或“<”)。
③從狀態a到c,CO2轉化率不斷增大的原因是________________________________。
④狀態e時,a(CO2)= 50%,若保持容器容積為10L,則此時的平衡常數K=____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】亞硝酸鈉是一種重要的工業用鹽,某同學針對亞硝酸鈉設計了如下實驗:(已知:Na2O2+2NO=2NaNO2;Na2O2+2NO2=2NaNO3)

(1)該同學用以上儀器制備NaNO2,則裝置的連接順序為A→___→___→___→___→E。_________(填序號,可重復)
(2)儀器a的名稱為______________。
(3)NO在E中可被氧化成NO3-,寫出反應的離子方程式_________________________。
(4)比色法測定樣品中的NaNO2含量:
①在5個有編號的帶刻度試管中分別加入不同量的NaNO2溶液,各加入1mL的M溶液(M遇NaNO2呈紫紅色,NaNO2的濃度越大顏色越深),再加蒸餾水至總體積均為10 mL并振蕩,制成標準色階:
試管編號 | a | b | c | d | e |
NaNO2含量/(mg.L-1) | 0 | 20 | 40 | 60 | 80 |
②稱量0.10g制得的樣品,溶于水配成500mL溶液,取5mL 待測液,加入1mLM溶液,再加蒸餾水至10mL 并振蕩,與標準比色階比較;
③比色的結果是: 待測液的顏色與d 組標準色階相同,則樣品中NaNO2的質量分數為_______。
(5)滴定法測定樣品中的NaNO2含量:
①稱量0.5000g制得的樣品,溶于水配成500mL溶液,取25.00mL待測液于錐形瓶中,加入s mL KI 酸性溶液(足量),發生反應2NO2-+2I-+4H+=2NO↑+I2+2H2O;
②滴入2~3 滴_____作指示劑,用0.0100mol/LNa2S2O3溶液進行滴定,當看到______現象時,即為痛定終點(已知,2 Na2S2O3+ I2=Na2S4O6+2NaI);
③重復實驗后,平均消耗Na2S2O3溶液的體積為20.50mL,則樣品中NaNO2的質量分數為____(保留3 位有效數字)。
④下列操作會導致測定結果偏高的是______(填序號)。
A.滴定過程中向錐形瓶中加少量水
B.滴定前滴定管尖嘴部分有氣泡,滴定后氣泡消失
C.觀察讀數時,滴定前仰視,滴定后俯視
D.滴定時搖瓶幅度過大標準溶液滴到瓶外
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素R、X、Y、Z的原子序數依次遞增,R的無氧酸溶液能在玻璃容器上刻標記;R和X能形成XR3型化合物,X在化合物中只顯一種化合價;R和Z位于同主族,Y原子最外層電子數等于電子層數的2倍。下列有關推斷正確的是
A. R單質和Z單質均可與水發生反應置換出O2
B. 上述元素形成的簡單離子都能促進水的電離平衡
C. YR6能在氧氣中劇烈燃燒
D. 元素對應的簡單離子的半徑:Y>Z>R>X
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分子式均為C5H10O2的兩種有機物的結構簡式如右圖所示:
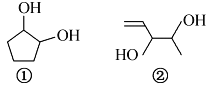
下列說法正確的是
A. 二者都能使Br2的CCl4溶液褪色
B. ①②分子中所有原子均可能處于同一平面
C. 等質量的①和②分別與足量鈉反應生成等質量的H2
D. 與其互為同分異構體的酯有8種(不考慮立體異構)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com