
在2 L密閉容器內,800 ℃時反應2NO(g)+O2(g)  2NO2(g)體系中,n(NO)隨時間的變化如表:
2NO2(g)體系中,n(NO)隨時間的變化如表:
時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)下圖表示NO2的變化的曲線是________。用O2表示從0~2 s內該反應的平均速率v=________。
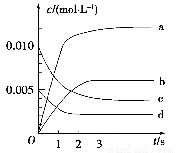
(2)能說明該反應已達到平衡狀態的是________。
a.v(NO2)=2v(O2) b.容器內壓強保持不變
c.v逆(NO)=2v正(O2) d.容器內密度保持不變
(3)為使該反應的反應速率增大,下列措施正確的是________。
a.及時分離出NO2氣體 b.適當升高溫度
c.增大O2的濃度 d.選擇高效催化劑
(1)b 1.5×10-3 mol·(L·s)-1 (2)bc (3)bcd
【解析】(1)NO2的起始濃度為c(NO2)=0,2 s時c(NO2)可根據圖表中n(NO)的變化量求解,c(NO2)=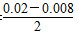 mol·L-1=0.006 mol·L-1,故答案選b。由圖表可求0~2 s內v(NO)=
mol·L-1=0.006 mol·L-1,故答案選b。由圖表可求0~2 s內v(NO)= mol·(L·s)-1=0.003 mol·(L·s)-1,故v(O2)=1.5×10-3mol·(L·s)-1。
mol·(L·s)-1=0.003 mol·(L·s)-1,故v(O2)=1.5×10-3mol·(L·s)-1。
(2)a:在任意狀態下,都存在v(NO2)=2v(O2)這樣的速率關系,不能作為平衡狀態的標志,故a錯。
b:因該反應為氣體體積不等的反應,故壓強不變可作為平衡狀態的標志。
c:由v逆(NO)=2v正(O2),可推出v逆(NO)=v正(NO),說明已達到平衡狀態。
d:由于平衡體系中全是氣體,容器體積固定,故任意狀態下密度不變,故d錯。
(3)及時分離出NO2氣體,只能使平衡向正反應方向移動,不能增大反應速率,故a錯;因該反應為放熱反應,適當升高溫度,雖使反應速率增大,但平衡向逆反應方向移動,故b錯;增大O2的濃度既能增大反應速率,又能使平衡向正反應方向移動,故c正確;催化劑只能增大反應速率,不能影響化學平衡的移動,故d錯。


 一線名師提優試卷系列答案
一線名師提優試卷系列答案科目:高中化學 來源:2014年化學高考復習演練4-5海水資源利用環境保護綠色化學練習卷(解析版) 題型:實驗題
海帶中含有豐富的碘。為了從海帶中提取碘,某研究性學習小組設計并進行了以下實驗:
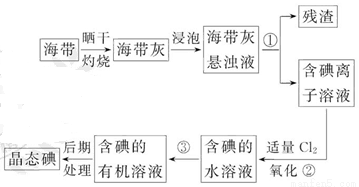
(1)步驟①的實驗操作名稱是_________;
(2)現有燒杯、玻璃棒、集氣瓶、酒精燈、導管、圓底燒瓶、石棉網以及必要的夾持儀器、物品。完成該實驗尚缺少的玻璃儀器是_________;
(3)步驟③中能選用CCl4從碘水中萃取碘的原因是_________;
A.CCl4與水不互溶
B.CCl4可與I2發生取代反應
C.CCl4的密度比水大
D.CCl4不易燃燒,可作滅火劑
E.碘在CCl4中的溶解度比在水中大很多
(4)步驟③中還可選擇_________作萃取劑;
(5)步驟②中反應的離子方程式是__________________________________;
(6)請設計一種簡單的實驗方法,檢驗提取碘后的水溶液中是否還含有單質碘:_________。
查看答案和解析>>
科目:高中化學 來源:2014學年高二魯科版選修3化學規范訓練 1章原子結構練習卷(解析版) 題型:選擇題
若短周期的兩元素可形成原子個數比為2∶3的化合物,則這兩種元素原子序數之差不可能是( )。
A.1 B.3 C.5 D.6
查看答案和解析>>
科目:高中化學 來源:2014學年高一化學人教版必修2 2章化學反應與能量練習卷(解析版) 題型:選擇題
一定溫度下,反應2SO2(g)+O2(g)  2SO3(g),達到平衡時,n(SO2)∶n(O2)∶n(SO3)=2∶3∶4。縮小體積,反應再次達到平衡時,n(O2)=0.8 mol,n(SO3)=1.4 mol,此時SO2的物質的量應是( )。
2SO3(g),達到平衡時,n(SO2)∶n(O2)∶n(SO3)=2∶3∶4。縮小體積,反應再次達到平衡時,n(O2)=0.8 mol,n(SO3)=1.4 mol,此時SO2的物質的量應是( )。
A.0.4 mol B.0.6 mol C.0.8 mol D.1.2 mol
查看答案和解析>>
科目:高中化學 來源:2014學年高一化學人教版必修2 2章化學反應與能量練習卷(解析版) 題型:選擇題
在可逆反應CO(g)+H2O(g)  CO2(g)+H2(g)(正反應為放熱反應)中,改變下列條件,不能使v正增大的是( )。
CO2(g)+H2(g)(正反應為放熱反應)中,改變下列條件,不能使v正增大的是( )。
A.升高溫度 B.降低溫度 C.使用催化劑 D.增大CO濃度
查看答案和解析>>
科目:高中化學 來源:2014學年高一化學人教版必修2 2.3.2反應限度條件的控制練習卷(解析版) 題型:選擇題
在合成氨反應中,下列說法可以確定反應達到化學平衡狀態的是( )。
A.當有1 mol N≡N鍵斷裂的同時,有3 mol H—H鍵斷裂
B.當有1 mol N≡N鍵斷裂的同時,有6 mol N—H鍵形成
C.當有1 mol N≡N鍵斷裂的同時,有6 mol H—H鍵形成
D.當有1 mol N≡N鍵斷裂的同時,有6 mol N—H鍵斷裂
查看答案和解析>>
科目:高中化學 來源:2014學年高一化學人教版必修2 2.3.2反應限度條件的控制練習卷(解析版) 題型:選擇題
可逆反應達到最大反應限度的本質特征是( )。
A.反應停止了 B.正逆反應的速率均為零
C.正逆反應都還在繼續進行 D.正逆反應的速率相等
查看答案和解析>>
科目:高中化學 來源:2014學年高一化學人教版必修2 2.2.2發展中的化學電源練習卷(解析版) 題型:填空題
鉛蓄電池是典型的可充電電池,它的正負極格板是惰性材料,電池總反應式為:
Pb+PbO2+4H++2SO42— 2PbSO4+2H2O
2PbSO4+2H2O
請回答下列問題(不考慮氫、氧的氧化還原):
放電時:正極的電極反應式是______________________________;電解液中H2SO4的濃度將變________;當外電路通過1 mol電子時,理論上負極板的質量增加________g。
查看答案和解析>>
科目:高中化學 來源:2014學年高一化學人教版必修2 1章物質結構 元素周期律練習卷(解析版) 題型:填空題
科學家發現:具有2、8、20、28、50、82、114、126等數目的質子或中子的原子核具有特別的穩定性,并將這些偶數稱為“幻數”,而具有雙幻數的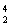 He、
He、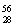 Ni、
Ni、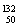 Sn、Pb等尤為穩定。根據此信息回答下列問題:
Sn、Pb等尤為穩定。根據此信息回答下列問題:
(1)寫出前三種質子數為“幻數”的元素原子的結構示意圖,并標明元素符號__________________。
(2)已知氧有三種同位素 O、
O、 O、
O、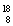 O,根據上述“幻數”規律,氧的同位素中原子核最穩定的是________。
O,根據上述“幻數”規律,氧的同位素中原子核最穩定的是________。
(3)根據現有元素周期律推算, R位于元素周期表的第________周期第________族,核穩定性
R位于元素周期表的第________周期第________族,核穩定性 R__________
R__________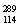 R(填“>”、“<”或“=”)。
R(填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com