
【題目】熱化學碘硫循環可用于大規模制氫氣,SO2水溶液還原I2和HI分解均是其中的主要反應。回答下列問題:
(1)以太陽能為熱源,熱化學硫碘循環分解水是一種高效、無污染的制氫方法。其反應過程如圖所示。
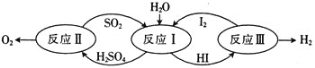
反應II包含兩步反應:
①H2SO4(l)=SO3(g)+H2O(g) △H1=+177kJ/mol
②2SO3(g)=2SO2(g)+O2(g) △H2=+196kJ/mol
①寫出反應①自發進行的條件是:________。
②寫出反應Ⅱ的熱化學方程式:________。
(2)起始時 HI的物質的量為1mo1,總壓強為0.1MPa下,發生反應HI(g)![]()
![]() H2(g)+
H2(g)+![]() I2(g) 平衡時各物質的物質的量隨溫度變化如圖所示:
I2(g) 平衡時各物質的物質的量隨溫度變化如圖所示:
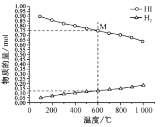
①該反應的△H ________ (“>”或“<”)0。
②600℃時,平衡分壓p(I2)= ___MPa,反應的平衡常數Kp=______ (Kp為以分壓表示的平衡常數)。
(3)反應 H2(g)+I2(g) ![]() 2HI(g)的反應機理如下:
2HI(g)的反應機理如下:
第一步:I2![]() 2I(快速平衡)
2I(快速平衡)
第二步:I+H2![]() H2I(快速平衡)
H2I(快速平衡)
第三步:H2I+I ![]() 2HI (慢反應)
2HI (慢反應)
①第一步反應_____ (填 “放出”或“吸收”)能量。
②只需一步完成的反應稱為基元反應,基元反應如aA+dD = gG+hH 的速率方程,v= kca(A)cd(D),k為常數;非基元反應由多個基元反應組成,非基元反應的速率方程可由反應機理推定。H2(g)與I2(g)反應生成 HI(g)的速率方程為v= ____(用含k1、k-1、k2…的代數式表示)。
【答案】高溫 2H2SO4(1)=2SO2(g)+O2(g)+2H2O(g)△H=+550kJ/mol > 0.0125 ![]() (或0.167) 吸收
(或0.167) 吸收 ![]() c(H2)·c(I2)
c(H2)·c(I2)
【解析】
(1)由反應式①+②可得熱化學方程式;
(2)①隨著溫度的不斷升高,HI的物質的量不斷減小,H2的物質的量不斷增大,則平衡正向移動,所以正反應為吸熱反應;
②從圖中采集數據,600℃時,n(HI)=0.75mol,n(H2)=0.125mol,反應前后氣體分子數不變,從而得出平衡分壓![]() ,計算出各組分氣體的分壓,從而求得平衡常數;
,計算出各組分氣體的分壓,從而求得平衡常數;
(3)①第一步反應斷裂共價鍵,吸收能量;
②反應速率由慢反應決定,即v=k3c(H2I)c(I),用第一步反應k1c(I2)=k-1c2(I),求出c(I)的表達式,用第二步的反應k2c(I)c(H2)=k-2c(H2I),求出c(H2I)的表達式,代入即可求得v。
(1)①反應①是氣體物質的量增大的吸熱反應,由![]() ,能自發進行的條件是高溫,故答案為:高溫;
,能自發進行的條件是高溫,故答案為:高溫;
②由反應式①+②可得出反應Ⅱ的熱化學方程式:2H2SO4(1)=2SO2(g)+O2(g)+2H2O(g)△H=+550kJ/mol;故答案為:2H2SO4(1)=2SO2(g)+O2(g)+2H2O(g)△H=+550kJ/mol;
(2)①隨著溫度的不斷升高,HI的物質的量不斷減小,H2的物質的量不斷增大,則平衡正向移動,所以正反應為吸熱反應,該反應的△H>0,故答案為:>;
②從圖中采集數據,600℃時,n(HI)=0.75mol,n(H2)=0.125mol,反應前后氣體分子數不變,從而得出平衡分壓![]() p,各氣體的平衡分壓:
p,各氣體的平衡分壓:![]() ,
,![]() ,反應HI(g)
,反應HI(g)![]()
![]() H2(g)+
H2(g)+![]() I2(g)的平衡常數
I2(g)的平衡常數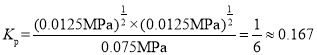 ,故答案為:0.0125;
,故答案為:0.0125;![]() (或0.167);
(或0.167);
(3)①第一步反應斷裂共價鍵,吸收能量,故答案為:吸收;
②反應速率由慢反應決定,即v=k3c(H2I)c(I),
第一步是快速平衡,k1c(I2)=k-1c2(I),可得![]() ,第二步也是快速平衡,k2c(I)c(H2)=k-2c(H2I),可得
,第二步也是快速平衡,k2c(I)c(H2)=k-2c(H2I),可得![]() ,則速率方程為:
,則速率方程為:![]() ,故答案為:img src="http://thumb.zyjl.cn/questionBank/Upload/2020/07/22/00/8fe3223f/SYS202007220000202798657132_DA/SYS202007220000202798657132_DA.002.png" width="49" height="45" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />c(H2)·c(I2)。
,故答案為:img src="http://thumb.zyjl.cn/questionBank/Upload/2020/07/22/00/8fe3223f/SYS202007220000202798657132_DA/SYS202007220000202798657132_DA.002.png" width="49" height="45" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />c(H2)·c(I2)。


科目:高中化學 來源: 題型:
【題目】如圖所示每一方框表示一種反應物或生成物,其中A、C、D、E、F在通常情況下均為氣體,且加熱X生成的A與C的物質的量之比為1∶1,B為常見液體。
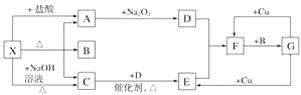
試回答下列問題:
(1)X是________(填化學式,下同),F是__________。
(2)A―→D反應的化學方程式為_______。
(3)G與Cu的反應中,G表現的性質為______。
(4)X與過量NaOH溶液反應生成C的離子方程式為_____________。
(5)以C、B、D為原料可生產G,若使amol C完全轉化為G,理論上至少需要D___ mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H是合成某藥物的中間體,一種合成H的路線如下(部分條件和產物省略):
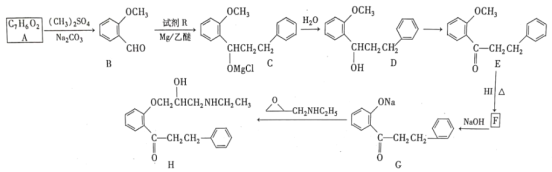
已知:①RCHO![]()
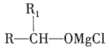
②A能發生銀鏡反應,遇FeCl3溶液發生顯色反應。
請回答下列問題:
(1)A所含官能團的名稱是___________。1個H分子含___________個手性碳原子。
(2)D→E的反應條件和試劑為___________。G→H的反應類型是___________。
(3)設計A→B、E→F步驟的目的是__________。
(4)寫出B→C的化學方程式:______。
(5)在B的同分異構體中,能發生水解反應的結構有___________種(不考慮立體異構)。其中,在核磁共振氫譜上有4組峰且峰的面積比為1:2:2:3的結構簡式可能為____________。
(6)參照上述流程,以乙醇為有機物原料合成2-丁醇(其他試劑自選),設計合成路線:________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2016 年諾貝爾化學獎授予在“分子機器設計和合成”領域有突出成就的三位科學家,其研究對象之一“分子開關”即與大環主體分子苯芳烴、硫或氮雜環杯芳烴等有關。回答下列問題:
(1)對叔丁基杯[4]芳烴(如圖Ⅰ所示)可用于ⅢB 族元素對應離子的萃取,如La3+、Sc2+。寫出基態二價 鈧離子(Sc2+)的核外電子排布式:____,其中電子占據的軌道數為_____個。
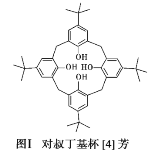
(2)對叔丁基杯[4]芳烴由4個羥基構成杯底,其中羥基氧原子的雜化方式為_____,羥基間的相互作用力為_____。
(3)不同大小苯芳烴能識別某些離子,如:N3-、SCN等。一定條件下,SCN與 MnO2反應可得到(SCN)2,試寫出(SCN)2的結構式_______。
(4)NH3分子在獨立存在時 H-N-H 鍵角為 106.7°。 [Zn(NH3)6]2+離子中 H-N-H 鍵角變為 109.5°,其原因是:_________________________。
(5)已知 C60 分子結構和 C60 晶胞示意圖(如圖Ⅱ、圖Ⅲ所示):則一個 C60 分子中含有σ鍵的個數為______,C60 晶體密度的計算式為____gcm3。(NA 為阿伏伽德羅常數 的值)
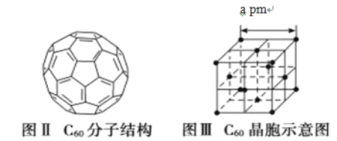
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙醇催化氧化制取乙醛(沸點為20.8℃,能與水混溶)的裝置(夾持裝置已略)如圖所示:
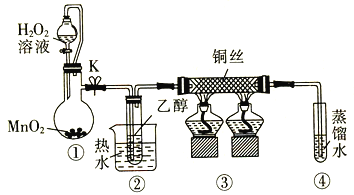
下列說法錯誤的是
A.向圓底燒瓶中滴入H2O2溶液前需打開K
B.實驗開始時需先加熱②,再通O2,然后加熱③
C.裝置③中發生的反應為2CH3CH2OH +O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
D.實驗結束時需先將④中的導管移出。再停止加熱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機化合物G是4-羥基香豆素,是重要的醫藥中間體,可用來制備抗凝血藥,可通過下列路線合成。
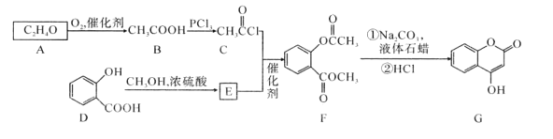
請回答:
(1)D→E的反應類型是___。
(2)G中含有的官能團名稱為____。
(3)寫出G和過量NaOH溶液共熱時反應的化學方程式___。
(4)化合物E的同分異構體很多,符合下列條件的結構共___種。
①能與氯化鐵溶液發生顯色反應;②能發生銀鏡反應;③能發生水解反應
其中,核磁共振氫譜為5組峰,且峰面積比為2:2:2:1:1的結構簡式為____。
(5)E的同分異構體很多,所有同分異構體在下列某種表征儀器中顯示的信號(或數據)完全相同,該儀器是___(填標號)。
a.質譜儀 b.元素分析儀 c.紅外光譜儀 d.核磁共振儀
(6)已知酚羥基一般不易直接與羧酸酯化。苯甲酸苯酚酯(![]() )是一種重要的有機合成中間體。請根據已有知識并結合相關信息,試寫出以苯酚、甲苯為原料制取該化合物的合成路線流程圖(無機原料任選):___。
)是一種重要的有機合成中間體。請根據已有知識并結合相關信息,試寫出以苯酚、甲苯為原料制取該化合物的合成路線流程圖(無機原料任選):___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組用下列裝置完成了探究濃硫酸和 SO2性質的實驗(部分夾持裝置已省略),下列“ 現象預測” 與“ 解釋或結論” 均正確的是
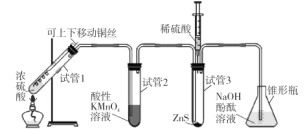
選項 | 儀器 | 現象預測 | 解釋或結論 |
A | 試管1 | 有氣泡、酸霧,溶液中有白色固體出現 | 酸霧是SO2所形成,白色固體是硫酸銅晶體 |
B | 試管2 | 紫紅色溶液由深變淺,直至褪色 | SO2具有還原性 |
C | 試管3 | 注入稀硫酸后,沒有現象 | 由于Ksp(ZnS)太小,SO2與ZnS在注入稀硫酸后仍不反應 |
D | 錐形瓶 | 溶液紅色變淺 | NaOH溶液完全轉化為NaHSO3溶液,NaHSO3溶液堿性小于NaOH |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:pAg=![]() lg[c(Ag+)],Ksp(AgCl)=1×10-12。如圖是向10mLAgNO3溶液中逐漸加入0.1mol·L-1的NaCl溶液時,溶液的pAg隨著加入NaCl溶液的體積(單位:mL)變化的圖像(實線)。根據圖像所得下列結論不正確的是[提示:Ksp(AgCl)>Ksp(AgI)]
lg[c(Ag+)],Ksp(AgCl)=1×10-12。如圖是向10mLAgNO3溶液中逐漸加入0.1mol·L-1的NaCl溶液時,溶液的pAg隨著加入NaCl溶液的體積(單位:mL)變化的圖像(實線)。根據圖像所得下列結論不正確的是[提示:Ksp(AgCl)>Ksp(AgI)]
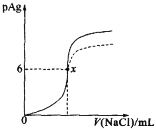
A.原AgNO3溶液的物質的量濃度為1mol·L-1
B.圖中x點的坐標為(100,6)
C.圖中x點可認為溶液中Ag+被沉淀完全
D.把0.1mol·L-1的NaCl換成0.1mol·L-1NaI,則圖像在終點后變為虛線部分
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】微型實驗具有裝置小巧、節約藥品、操作簡便、現象明顯、安全可靠、減少污染等優點,下圖是某同學設計的實驗室制取Cl2并探究其化學性質的微型裝置(圖中夾持裝置均略去)。
查閱資料:氯氣的氧化性大于HIO3。
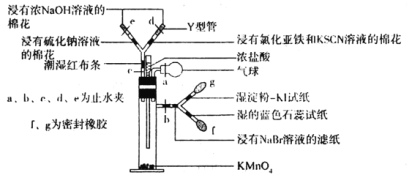
回答下列問題:
(1)實驗室中可代替圖中添加濃鹽酸的儀器名稱是___________。
(2)加入濃鹽酸后試管內發生反應的化學方程式是__________________________________。
(3)探究氯氣的化學性質,將實驗現象填寫在下表對應的空格里:___________
操作步驟 | 實驗現象 |
緩慢加入濃鹽酸,打開c、d、e,使產生的氯氣緩慢充入Y試管 | |
關閉c打開b,使氯氣緩慢進入Y管中 |
(4)實驗中發現若氯氣的通入量過多,淀粉碘化鉀試紙會逐漸變為無色,可能的原因是__________________________________________________。
(5)此裝置___________(填“能”或“不能”)證明氧化性順序Cl2>Br2>I2,原因是___________,實驗完畢后,關閉止水夾b,打開a、c,擠壓氣球,目的是__________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com