
【題目】如圖所示為實驗室模擬工業上催化裂化的裝置示意圖,根據圖示回答下列問題。

(1)工業上石油裂化的主要目的是_______________________。
(2)A中氧化鋁的作用是_____________,B中冷水的作用是___________________。
(3)C中得到的液體具有汽油的氣味,該液體________________(填“能”或“不能”,下同)通過化學反應使溴水褪色,而通過石油分餾得到的汽油_______________通過化學反應使溴水褪色。
(4)D中酸性高錳酸鉀溶液褪色,說明石蠟裂化時除有液態不飽和烴生成外,還有__________生成。
科目:高中化學 來源: 題型:
【題目】某溫度下,![]() 和
和![]() 的電離常數分別為
的電離常數分別為![]() 和
和![]() 。將
。將![]() 和體積均相同的兩種酸溶液分別稀釋,其
和體積均相同的兩種酸溶液分別稀釋,其![]() 隨加水體積的變化如圖所示。下列敘述正確的是( )
隨加水體積的變化如圖所示。下列敘述正確的是( )

A. 曲線Ⅰ代表![]() 溶液
溶液
B. 溶液中水的電離程度:b點>c點
C. 從c點到d點,溶液中 保持不變(其中
保持不變(其中![]() 、
、![]() 分別代表相應的酸和酸根離子)
分別代表相應的酸和酸根離子)
D. 相同體積a點的兩溶液分別與![]() 恰好中和后,溶液中
恰好中和后,溶液中![]() 相同
相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國科學家在某雜志上發表研究報告稱,利用鉻同位素的系統分析發現,“古代大氣氧含量高于現代水平的1%”。鉻的同位素有![]() 、
、![]() 、
、![]() 、
、![]() 。鉻及其化合物在生活、生產中有廣泛應用。回答下列問題:
。鉻及其化合物在生活、生產中有廣泛應用。回答下列問題:
(1)基態![]() 的價層電子排布圖為_________
的價層電子排布圖為_________
(2)交警用“酒精儀”查酒駕,其化學反應原理如下:
2K2Cr2O7+3CH3CH2OH+8H2SO4→3CH3COOH+2Cr2(SO4)3+2K2SO4+11H2O
①CH3CH2OH、CH3COOH的沸點高于對應的CH3OCH3(二甲醚)、HCOOCH3(甲酸甲酯),其主要原因是___________。
②CH3COOH分子中碳原子的雜化類型是______;CH3COOH分子中σ鍵和π鍵數目之比為_________。
③K2SO4晶體中陰離子的空間構型是________。上述反應中,只含極性鍵的極性分子有________(填分子式)。
(3)晶體鉻的晶胞結構如圖1所示,其堆積模型為___________;鉻原子的配位數為___________。

(4)鉻的一種氧化物晶胞結構如圖2所示。六棱柱邊長為a nm,高為b nm,NA代表阿伏加德羅常數的值。該晶體的化學式為______;該晶體的密度ρ=_______g·cm-3。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金屬鈦呈銀白色,因它堅硬、強度大、耐熱、密度小,被稱為高技術金屬。目前生產鈦采用氯化法,主要步驟如下:
Ⅰ.即將金紅石或鈦鐵礦與焦炭混合,通入氯氣并加熱制得TiCl4:
2FeTiO3+7Cl2+6C![]() 2TiCl4+2FeCl3+6CO
2TiCl4+2FeCl3+6CO
TiO2+2Cl2+2C![]() TiCl4+2CO
TiCl4+2CO
Ⅱ.將TiCl4蒸餾并提純,在氬氣保護下與鎂共熱得到鈦:
TiCl4+2Mg![]() Ti+2MgCl2
Ti+2MgCl2
Ⅲ.用稀鹽酸溶解MgCl2和過量Mg后得海綿狀鈦,再在真空熔化鑄成鈦錠。
請回答下列問題:
(1)基態鈦原子的價電子排布式為___。
(2)與CO互為等電子體的離子為___(填化學式)。
(3)在CH2Cl2、HCHO、CO2、C2H4中,碳原子采取sp2雜化的分子有___。
(4)TiCl4在常溫下是無色液體,在水或潮濕空氣中易水解而冒白煙。則TiCl4屬于___(填“原子”“分子”或“離子”)晶體。
(5)與鈦同周期的另一種元素鈷(Co)可形成分子式均為Co(NH3)5BrSO4的兩種配合物,其中一種化學式為[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液時,現象是___;往另一種配合物的溶液中加入BaCl2溶液時,無明顯現象,若加入AgNO3溶液時,產生淡黃色沉淀,則第二種配合物的化學式為___。
(6)在自然界中TiO2有金紅石、板鈦礦、銳鈦礦三種晶型,其中金紅石的晶胞如圖所示,則其中Ti4+的配位數為___。
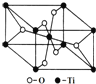
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是
A.分子的中心原子通過sp3雜化軌道成鍵時,該分子一定為正四面體結構
B.1,2-二氯丙烷( )分子中含有兩個手性碳原子
)分子中含有兩個手性碳原子
C.熔、沸點:Na<Mg<Al
D.配合物的穩定性與配位鍵的強弱有關,與配位體的性質無關
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,用0.1000mol·L-1的NaOH溶液分別滴定20.00mL均為0.1000mol·L-1的三種酸HX、HY、HZ ,滴定曲線如圖所示。下列說法錯誤的是
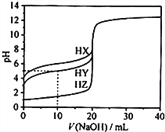
A. HZ是強酸,HX、HY是弱酸
B. 根據滴定曲線,可得Ka(HY)≈10-5
C. 將上述HX、HY溶液等體積混合后,用NaOH溶液滴定至HX恰好完全反應時:c(X-)>c(Y-)>c(OH-)>c(H+)
D. 將上述HY與HZ溶液等體積混合達到平衡時:C(H+)=c(OH-)+c(Z-)+c(Y-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵是地殼中含量較豐富的元素,僅次于氧、硅、鋁元素,其單質及合金是在生產生活中應用廣泛的金屬材料。化學上常用KSCN溶液等來檢驗溶液中是否存在Fe3+。
(1)Fe3+離子基態的電子排布式可表示為___。
(2)一種鐵晶體的晶胞屬于體心立方堆積,則該晶胞中所包括的鐵原子的個數是___。
(3)C、N兩種元素的簡單氣態氫化物的熱穩定性由強到弱的順序為___。(填化學式)
(4)C、N、O三種元素的第一電離能由大到小的順序為___(填元素符號)。
(5)離子化合物Fe2O3的熔點高于KC1的熔點的原因是___。
(6)據報道:由Q、X、Z三種元素形成的一種晶體具有超導性,其晶體結構如圖所示。晶體中距每個X原子周圍距離最近的Q的原子的個數是___。
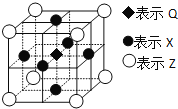
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 時,將濃度均為
時,將濃度均為![]() 、體積分別為
、體積分別為![]() 和
和![]() 的
的![]() 溶液與
溶液與![]() 溶液按不同體積比混合,保持
溶液按不同體積比混合,保持![]() ,
,![]() 、
、![]() 與混合液的
與混合液的![]() 的關系如圖所示,下列說法不正確的是( )
的關系如圖所示,下列說法不正確的是( )
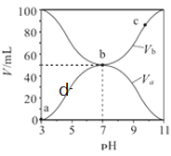
A.![]() 的數量級約為
的數量級約為![]()
B.b點時![]()
C.a、b、d幾點中,水的電離程度![]()
D.![]() 點過程中,可能存在
點過程中,可能存在![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯堿工業以電解精制飽和食鹽水的方法制取氯氣、氫氣、燒堿和氯的含氧酸鹽等系列化工產品。如圖是離子交換膜法電解食鹽水的示意圖,圖中的離子交換膜只允許陽離子通過。
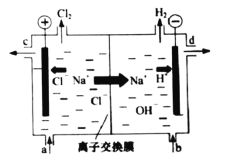
完成下列填空:
(1)寫出電解飽和食鹽水的離子方程式_______。
(2)離子交換膜的作用為:______、______。
(3)精制飽和食鹽水從圖中_____位置補充,氫氧化鈉溶液從圖中_____位置流出(選填“a”、“b”、“c”或“d”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com