
【題目】將如圖所示實驗裝置的K閉合,下列判斷正確的是( )
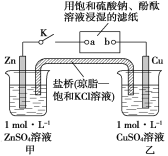
A.電子沿Zn→a→b→Cu路徑流動
B.Cu電極上發生還原反應
C.片刻后甲池中c(SO![]() )增大
)增大
D.片刻后可觀察到濾紙b點變紅色
【答案】B
【解析】
試題分析:A、閉合K構成原電池,鋅比銅活潑,鋅作負極,銅作正極,根據原電池工作原理,電子從Zn流出,達到a,在濾紙上沒有電子的通過,只有陰陽離子的定向移動,電子從b流向Cu,故錯誤;B、根據選項A的分析,Cu作正極,根據原電池的工作原理,正極上發生還原反應,故正確;C、鹽橋的作用是形成閉合回路,平衡兩燒杯的電荷守恒,因此Cl-流向甲池,溶液中c(SO42-)不變,故錯誤;D、濾紙相當于電解池,b接電源的正極,b作陽極,發生電極反應式為4OH-4e-=2H2O+O2↑,a接電源的負極,作陰極,電極反應式為2H2O-2e-=H2↑+2OH-,因此a極變紅,故錯誤。


科目:高中化學 來源: 題型:
【題目】幾種物質的化學式及其名稱分別是:Na2S2O3硫代硫酸鈉;CaSx多硫化鈣;BaO2過氧化鋇。根據上述命名規律K2CS3的名稱應為( )
A.三硫代碳酸鉀 B.多硫碳化鈣肥 C.過硫碳酸鉀 D.超硫碳酸鉀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于生物體的組成元素的說法,正確的是( )
A. 脂肪、磷脂和蛋白質都可以供能
B. 糖類、脂質和蛋白質都含有C、H、O元素
C. 小麥體內的化學元素與自然界中的化學元素在種類和含量上基本相同
D. 小麥體內的化學元素與玉米體內的化學元素在種類和含量上基本相同
查看答案和解析>>
科目:高中化學 來源: 題型:
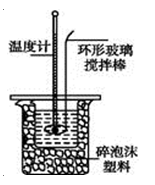
【題目】用100mL 1.00mol·L-1鹽酸與100mL 1.10mol·L-1NaOH溶液在如下圖所示的裝置中進行中和熱測定實驗。以下是四次實驗所得數據。回答下列問題:
實驗 數據 | 鹽酸起始溫度t1/℃ | 氫氧化鈉起始溫度t2/℃ | 兩溶液混合后 溫度t3/℃ |
1 | 21.0 | 21.1 | 26.9 |
2 | 21.5 | 21.7 | 28.2 |
3 | 21.9 | 22.1 | 28.7 |
4 | 22.3 | 22.5 | 29.2 |
(1)上表中的溫度差平均值為 ℃
(2)近似認為上述兩種溶液的密度都是1 g·cm-3,中和后生成溶液的比熱容c=4.18J·(g·℃)-1。則計算得到中和熱ΔH= (取小數點后一位)。
(3)上述實驗數值結果與57.3 kJ·mol-1有偏差,產生偏差的原因可能是(填字母) 。
a.實驗裝置保溫、隔熱效果差
b.用環形銅質攪拌棒代替環形玻璃攪拌棒
c.分多次把NaOH溶液倒入盛有鹽酸的小燒杯中
d.用溫度計測定鹽酸溶液起始溫度后直接測定NaOH溶液的溫度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室在加熱條件下H2還原CuO所得的紅色固體可能是Cu與Cu2O的混合物,已知Cu2O在酸性溶液中可發生自身氧化還原反應,生成Cu2+和單質銅。現有8g CuO被H2還原后,得到紅色固體6.8g。
(1)寫出H2還原CuO生成Cu2O的化學方程式 ;
(2)6.8 g上述混合物中含Cu與Cu2O的物質的量之比是 ;
(3)若將6.8 g上述混合物與足量的稀硫酸充分反應后過濾,可得到固體 g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)制備氫氧化鐵膠體,向沸水中逐滴滴加 溶液,繼續加熱至 為止,寫出有關反應的化學方程式 。
(2)若向該分散系逐滴加入鹽酸溶液至過量,會出現一系列變化的現象為 (填序號)
A.無明顯變化 B.出現紅褐色沉淀 C.紅褐色沉淀溶解
寫出有關的離子方程式 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某地甲、乙兩廠排放的污水中各含有下列8種離子中的4種(兩廠廢水所含離子不同):Ag+、Ba2+、Fe3+、Na+、Cl-、SO![]() 、NO
、NO![]() 、OH-。若兩廠單獨排放污水都會造成嚴重的水污染,如將兩廠的污水按一定比例混合,沉淀后污水便能變得無色澄清,溶質主要含硝酸鈉,污染程度大大降低。根據所給信息有以下幾種說法,你認為正確的是( )
、OH-。若兩廠單獨排放污水都會造成嚴重的水污染,如將兩廠的污水按一定比例混合,沉淀后污水便能變得無色澄清,溶質主要含硝酸鈉,污染程度大大降低。根據所給信息有以下幾種說法,你認為正確的是( )
A.Na+和NO![]() 可能來自同一工廠 B.Cl-和NO
可能來自同一工廠 B.Cl-和NO![]() 一定來自同一工廠
一定來自同一工廠
C.Ag+和Na+可能來自同一工廠 D.SO![]() 和OH-一定來自同一工廠
和OH-一定來自同一工廠
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com