

| A.二氧化硫的接觸氧化在接觸室中發生 |
| B.吸收塔用濃度為98.3%濃硫酸吸收三氧化硫 |
| C.煅燒含硫48%的黃鐵礦時,若FeS2損失了2%,則S損失2% |
| D.B裝置中反應的條件之一為較高溫度是為了提高SO2的轉化率 |
 2Fe2O3 + 8SO2 (2)D、E
2Fe2O3 + 8SO2 (2)D、E Na2CO3 + CO2↑+ H2O
Na2CO3 + CO2↑+ H2O  2Fe2O3 + 8SO2。(2)A.在接觸室中發生反應:2SO2+O2
2Fe2O3 + 8SO2。(2)A.在接觸室中發生反應:2SO2+O2 2SO3因此該選項正確。B.如果用水吸收SO3,容易形成酸霧,不利于SO3的吸收。所以在吸收塔中一般是用98.3%濃硫酸吸收三氧化硫形成發煙硫酸,然后再稀釋成所需要的濃度。正確。C.C.煅燒含硫48%的黃鐵礦時,若FeS2損失了2%,則其中各組分的損失也都是2%.這與物質的組成無關。正確。D.在設備B中發生的反應2SO2+O2
2SO3因此該選項正確。B.如果用水吸收SO3,容易形成酸霧,不利于SO3的吸收。所以在吸收塔中一般是用98.3%濃硫酸吸收三氧化硫形成發煙硫酸,然后再稀釋成所需要的濃度。正確。C.C.煅燒含硫48%的黃鐵礦時,若FeS2損失了2%,則其中各組分的損失也都是2%.這與物質的組成無關。正確。D.在設備B中發生的反應2SO2+O2 2SO3為放熱反應,如果升高溫度,根據平衡移動原理,升高溫度,化學平衡會向吸熱反應方向移動,對該反應來說就是向逆反應方向移動。這對于提高SO2的轉化率不利。之所以采用較高的溫度,是為了加快化學反應速率,縮短達到平衡所需要的時間。提高生產效率。錯誤。E.硫酸工業中在接觸室安裝熱交換器是為了利用SO2氧化為SO3時的熱量。錯誤。Ⅱ.(3)“聯合制堿法”中CO2的來源于合成氨廠;“氨堿法”中CO2來源于煅燒石灰石。(4)氨堿法的化學反應原理為:NH3+CO2+H2O==NH4HCO3;NaCl+NH4HCO3==NaHCO3↓+NH4Cl 2NaHCO3
2SO3為放熱反應,如果升高溫度,根據平衡移動原理,升高溫度,化學平衡會向吸熱反應方向移動,對該反應來說就是向逆反應方向移動。這對于提高SO2的轉化率不利。之所以采用較高的溫度,是為了加快化學反應速率,縮短達到平衡所需要的時間。提高生產效率。錯誤。E.硫酸工業中在接觸室安裝熱交換器是為了利用SO2氧化為SO3時的熱量。錯誤。Ⅱ.(3)“聯合制堿法”中CO2的來源于合成氨廠;“氨堿法”中CO2來源于煅燒石灰石。(4)氨堿法的化學反應原理為:NH3+CO2+H2O==NH4HCO3;NaCl+NH4HCO3==NaHCO3↓+NH4Cl 2NaHCO3 Na2CO3 + CO2↑+ H2O ;2NH4Cl+Ca(OH)2
Na2CO3 + CO2↑+ H2O ;2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O。CO2、NH3循環利用。在該方法中,目標產物為Na2CO3;實際產物為Na2CO3和CaCl2。所以原子利用率為[106÷(106+111)]×100%=49%(或106/217)。(5) “聯合制堿法”有關反應的化學方程式為NH3 + H2O + CO2 + NaCl(飽和)= NaHCO3 ↓+ NH4Cl; 2NaHCO3
CaCl2+2NH3↑+2H2O。CO2、NH3循環利用。在該方法中,目標產物為Na2CO3;實際產物為Na2CO3和CaCl2。所以原子利用率為[106÷(106+111)]×100%=49%(或106/217)。(5) “聯合制堿法”有關反應的化學方程式為NH3 + H2O + CO2 + NaCl(飽和)= NaHCO3 ↓+ NH4Cl; 2NaHCO3 Na2CO3 + CO2↑+ H2O。
Na2CO3 + CO2↑+ H2O。

科目:高中化學 來源:不詳 題型:問答題

查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 CO2(g)+H2(g) ΔH<0。欲提高CO轉化率可采用的方法可能有:①降低溫度;②增大壓強 ③使用催化劑 ④增大CO的濃度;⑤增大水蒸氣的濃度,其中正確的組合是( )。
CO2(g)+H2(g) ΔH<0。欲提高CO轉化率可采用的方法可能有:①降低溫度;②增大壓強 ③使用催化劑 ④增大CO的濃度;⑤增大水蒸氣的濃度,其中正確的組合是( )。| A.①②③ | B.④⑤ | C.①⑤ | D.⑤ |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.制普通玻璃的主要原料是純堿、石灰石、石英砂 |
| B.工業上電解熔融的氯化鈉來制取鈉 |
| C.將二氧化硫催化成三氧化硫后,在吸收塔內用水吸收制得濃硫酸 |
| D.制造普通水泥的主要原料是黏土、石灰石 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
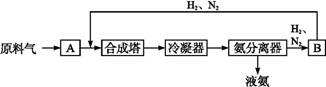
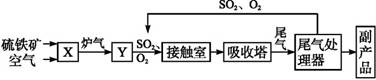
 2NH3(g) ΔH<0; 2SO2(g)+O2(g)
2NH3(g) ΔH<0; 2SO2(g)+O2(g) 2SO3(g) ΔH<0
2SO3(g) ΔH<0查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 NH2COONH4;NH2COONH4
NH2COONH4;NH2COONH4 CO(NH2)2+H2O
CO(NH2)2+H2O| A.NO2與H2O的反應生成HNO3和NO | B.NO與O2反應生成NO2 |
| C.NH3經催化氧化生成NO | D.N2 蛋白質 蛋白質 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.神七宇航員所穿航天服是由我國自行研制的新型“連續纖維增韌”航空材料做成,其主要成分是由碳化硅、陶瓷和碳纖維復合而成的,它是一種新型無機非金屬材料 |
| B.食品包裝袋、食物保鮮膜等材料的主要成份是聚氯乙烯 |
| C.人體內沒有能使纖維素水解成葡萄糖的酶,因此纖維素不能作為人類的營養食物 |
| D.針對病毒性流感的擴散情況,要加強環境、個人等的消毒預防,其中消毒劑常選用含氯消毒劑、酒精、雙氧水等適宜的物質 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
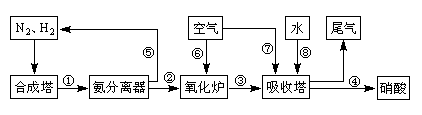
 CO2+H2。t℃時,往1L密閉容器中充入0.2mol CO和0.3mol水蒸氣。反應建立平衡后,體系中c(H2)=0.12mol·L-1。該溫度下此反應的平衡常數K=_____(填計算結果)。
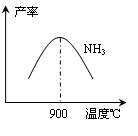
CO2+H2。t℃時,往1L密閉容器中充入0.2mol CO和0.3mol水蒸氣。反應建立平衡后,體系中c(H2)=0.12mol·L-1。該溫度下此反應的平衡常數K=_____(填計算結果)。 2NH3(g) △H<0。下表為不同溫度下該反應的平衡常數。由此可推知,表中T1____300℃(填“>”、“<”或“=”)。
2NH3(g) △H<0。下表為不同溫度下該反應的平衡常數。由此可推知,表中T1____300℃(填“>”、“<”或“=”)。| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.土壤膠體吸附的H+、Al3+被其他陽離子交換 |
| B.微生物、細菌在利用土壤中的有機物時,會產生二氧化碳和多種有機酸 |
| C.微生物、細菌在利用土壤中物質時,將土壤中的NH3轉化為亞硝酸和硝酸,將硫化物轉化為硫酸 |
| D.土壤有機物中的氮被微生物分解生成氨的氨化過程,會使土壤的pH升高 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com