
【題目】向NaOH和Na2CO3混合溶液中滴加0.1mol·L-1稀鹽酸,CO2的生成量與加入鹽酸的體積(V)的關系如圖所示。下列判斷正確的是( )
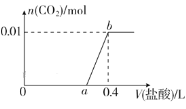
A.在0~a范圍內,只發生中和反應
B.a=0.3
C.ab段發生反應的離子方程式為CO32-+2H+=CO2↑+H2O
D.原混合溶液中NaOH與Na2CO3的物質的量之比為1∶2
【答案】B
【解析】
向NaOH和Na2CO3混合配成的溶液中滴加鹽酸時,先發生氫氧化鈉與鹽酸的中和反應:NaOH+HCl=NaCl+H2O,氫氧化鈉反應完畢后再發生碳酸鈉與鹽酸的反應:HCl+Na2CO3=NaHCO3+NaCl,最后發生反應:NaHCO3+HCl=NaCl+H2O+CO2↑,利用物質的量的關系并結合圖象分析解答。
A.向NaOH和Na2CO3混合溶液中滴加鹽酸時,首先和NaOH反應生成水和氯化鈉:NaOH+HCl=NaCl+H2O,繼續滴加時,鹽酸與Na2CO3首先發生反應:HCl+Na2CO3=NaHCO3+NaCl,不放出氣體,繼續滴加時發生反應:NaHCO3+HCl=NaCl+H2O+CO2↑,則在0-a范圍內發生反應為:NaOH+HCl=NaCl+H2O、HCl+Na2CO3=NaHCO3+NaCl,故A錯誤;
B.根據圖像可知,從a點開始發生反應NaHCO3+HCl=NaCl+H2O+CO2↑,該過程中消耗氯化氫的物質的量與生成二氧化碳的物質的量相等為0.01mol,則消耗0.1molL-1稀鹽酸的體積分別為![]() =0.1L,所以a=0.4-0.1=0.3,故B正確;
=0.1L,所以a=0.4-0.1=0.3,故B正確;
C.根據分析可知,ab段發生反應為:NaHCO3+HCl=NaCl+H2O+CO2↑,反應的離子方程式為:HCO3-+H+=H2O+CO2↑,故C錯誤;
D.根據碳元素守恒,混合物中碳酸鈉的物質的量是0.01mol,b點消耗鹽酸的物質的量為0.1mol/L×0.4L=0.04mol,則a點氯化氫的物質的量為:0.04mol-0.01=0.03mol,根據反應HCl+Na2CO3=NaHCO3+NaCl可知,0.01mol碳酸鈉消耗0.01mol氯化氫生成碳酸氫鈉,則氫氧化鈉的物質的量為0.03mol-0.01mol=0.02mol,所以原混合溶液中NaOH與Na2CO3的物質的量之比為0.02mol∶0.01mol=2∶1,故D錯誤;
故選B。


科目:高中化學 來源: 題型:
【題目】電化學在日常生活中用途廣泛,如圖①是鎂、次氯酸鈉燃料電池的示意圖,電池總反應式為:Mg+ClO-+H2O=Cl-+Mg(OH)2↓。如圖②是電解法除去工業廢水中的Cr2O72-,下列說法正確的是( )
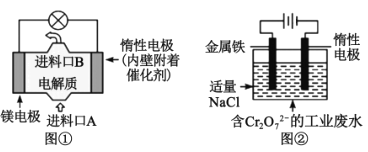
A.圖①中鎂電極發生的反應是:ClO-+H2O+2e-=Cl-+2OH-
B.圖②最終得到Fe(OH)3和Cr(OH)3,則陽極上的電極反應式為:Fe-3e-=Fe3+
C.圖②中每轉移0.2mol電子,陰極逸出2.24LH2
D.若圖①中7.2gMg溶解產生的電量用于圖②廢水處理,理論得到Fe(OH)3的物質的量為0.3mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:①H2(g)+![]() O2(g)=H2O(g) ΔH1=akJ·mol1
O2(g)=H2O(g) ΔH1=akJ·mol1
②2H2(g)+O2(g)=2H2O(g) ΔH2=bkJ·mol1
③H2(g)+![]() O2(g)=H2O(l) ΔH3=ckJ·mol1
O2(g)=H2O(l) ΔH3=ckJ·mol1
④2H2(g)+O2(g)=2H2O(l) ΔH4=d kJ·mol1
下列關系式中正確的是
A.a<c<0B.b>d>0C.2a=b<0D.2c=d>0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將4 mol A氣體和2 mol B氣體在2 L的容器中混合并在一定條件下發生如下反應:2A(g) +B(g)![]() 2C(g),2 s后測得C的濃度為0.6 mol·L-1,下列說法正確的是( )
2C(g),2 s后測得C的濃度為0.6 mol·L-1,下列說法正確的是( )
A. 用物質A表示的反應平均速率為0.6 mol·L-1·s-1
B. 用物質B表示的反應的平均速率為0.3 mol·L-1·s-1
C. 2s時物質A的轉化率為30%
D. 2s時物質B的濃度為0.8mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知熱化學方程式:SO2(g)+ 1/2O2(g) ![]() SO3(g) ΔH=―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反應,最終放出的熱量為( )
SO3(g) ΔH=―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反應,最終放出的熱量為( )
A. 196.64kJB. 小于98.32kJ
C. 小于196.64kJD. 大于196.64kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知下列反應的熱化學方程式為
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
②C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g)+![]() O2(g)=H2O(l) ΔH3=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH3=-285.8 kJ·mol-1
則反應2C(s)+2H2(g)+O2(g)=CH3COOH(l)的ΔH為( )
A. -488.3 kJ·mol-1 B. -191 kJ·mol-1
C. -476.8 kJ·mol-1 D. -1 549.6 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】釔鋇銅氧、汞鋇銅氧、汞鋇鈣銅氧等都是常見的高溫超導體。回答下列問題:
(1)釔(39Y)是一種重要的稀土金屬,基態Y原子的價電子排布式為______。下列科學家中,在稀土化學領域做出重要貢獻的是_________(填標號)。
a.侯德榜 b.屠呦呦 c.徐光憲
(2)BaCO3可用于制備上述高溫超導體,其3種組成元素中,第一電離能最大的是______(填元素符號),CO32-的空間構型為________,其中碳原子的雜化方式為________________。
(3)汞鋇銅氧晶體的晶胞如下圖A所示,通過摻雜Ca2+獲得的具有更高臨界溫度的超導材料如圖B所示。
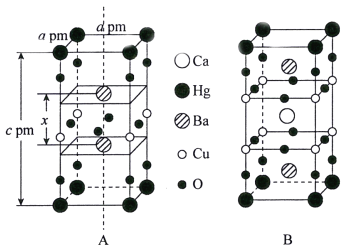
汞鋇銅氧晶體的密度為______g·cm-3(設NA為阿伏加德羅常數的值)。圖A晶胞中鋇離子的分數坐標為(![]() )和_________。摻雜Ca2+所得超導材料的化學式為_________。
)和_________。摻雜Ca2+所得超導材料的化學式為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,用0.100 mol·L-1 NaOH溶液滴定10 mL 0.100 mol·L-1 H3PO4溶液,曲線如圖所示。下列說法正確的是
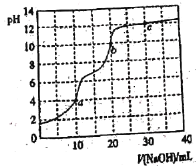
A.滴定終點a可選擇酚酞作指示劑
B.c點溶液中c(Na+)>3c(PO43-)+2c(HPO42-)+c(H2PO4-)
C.b點溶液中c(HPO42-)>c(PO43-)>c(H2PO4-)
D.a、b、c三點中水的電離程度最小的是c
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】把0.6molX氣體和0.4molY氣體混合于容積為2L的容器中,使其發生如下反應:3X(g)+Y(g)![]() nZ(g)+2W(g)。5min末生成0.2molW,若測知以Z濃度變化表示的平均反應速率為0.01mol/( L· min),則n的值為
nZ(g)+2W(g)。5min末生成0.2molW,若測知以Z濃度變化表示的平均反應速率為0.01mol/( L· min),則n的值為
A. 1B. 2C. 3D. 4
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com