
【題目】下列有關物質結構和性質的說法不正確的是( )
A. 分子式為C5H9O2Cl且能與飽和NaHCO3溶液反應產生氣體的有機物有12種(不含立體結構)
B. 已知引發某疫情的病毒對化學藥品很敏感,乙醇、漂白粉溶液均可將病毒氧化而達到消毒的目的
C. 一定條件下,完全燃燒14g含氧質量分數為a的乙烯、乙醛混合氣體,則生成水的質量為18(1-a)g
D. 按系統命名法,化合物![]() 的名稱為3-甲基-5,7-二乙基癸烷
的名稱為3-甲基-5,7-二乙基癸烷
【答案】B
【解析】
A.分子式為C5H9O2Cl且能與飽和NaHCO3溶液反應產生氣體說明該有機物為飽和一元羧酸的一氯代物,分子組成為C4H9—COOH的結構有四種,分別是①CH3CH2CH2CH2—COOH、②(CH3)2CHCH2—COOH、③(CH3)3C—COOH、④CH3CH2CH(CH3)—COOH,其中①分子中烴基上有四種不同化學環境的氫原子,則其一氯代物有四種;②分子中烴基上有3種不同化學環境的氫原子,則其一氯代物有3種;③分子中烴基上有1種不同化學環境的氫原子,則其一氯代物有1種;④分子中烴基上有四種不同化學環境的氫原子,則其一氯代物有四種;則其同分異構體的總數為:4+3+1+4=12,故A說法正確;
B.乙醇、漂白粉溶液可以消毒是因為它們能使蛋白質發生變性,并不是氧化,故B說法錯誤;
C.乙烯的分子式為C2H4,甲醛的分子式為CH2O,兩物質中C、H原子數目之比都是1:2,故混合物中C、H元素質量之比=12:2=6:1,含氧的質量分數為a,則C、H元素質量分數之和=1-a,故H元素質量分數=(1-a)×1÷(1+6)= (1-a)/7,生成水的質量為14g×![]() ×9=18(1-a)g,故C說法正確;
×9=18(1-a)g,故C說法正確;
D. A.主鏈含10個C,3號C上有甲基,5、7號C上有乙基,名稱為3-甲基-5,7-二乙基癸烷,故D說法正確;
答案選B。


科目:高中化學 來源: 題型:
【題目】常用的激光打印機、復印機使用的墨粉主要成分之一就是Fe3O4,氧化沉淀法是工業生產Fe3O4的主要方法,其工藝流程如下圖所示。已知:①工業綠礬主要成分是FeSO4·7H2O,②Fe(OH)2+2Fe(OH) 3=Fe3O4+4H2O
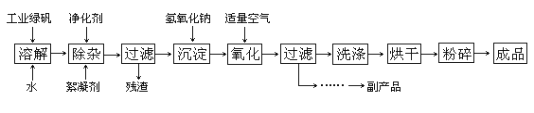
請回答下列問題:
(1)實驗室中檢驗FeSO4溶液因氧化而變質的實驗操作是__________
(2)寫出沉淀和氧化過程的化學方程式____________、_____________
(3)氧化過程中,若通入過量空氣會使成品含大量________雜質
(4)若原料中有278kg綠礬,則理論上可制得Fe3O4______kg
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面有關發泡塑料飯盒的敘述,不正確的是
A. 主要材質是高分子材料 B. 價廉、質輕、保溫性能好
C. 適用于微波爐加熱食品 D. 不適于盛放含油較多的食品
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與社會生產生活等密切相關,下列說法不正確的是
A.PM2.5屬于膠體,能產生丁達爾現象
B.中國芯的主要成分為單晶硅
C.人體缺乏鐵元素,可以適當補充硫酸亞鐵
D.節假日燃放煙花利用了焰色反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖為相關物質間的轉化關系,其中甲、丙為生活中常見的金屬單質,乙、丁為非金屬單質且丁為氣態,E為白色沉淀,D為淺綠色溶液。請回答:

(1)組成甲的元素在元素周期表中的位置為____________,請列舉乙單質的一種用途__________,用電子式表示丁的形成過程________________________
(2)在C溶液中滴入2滴酚酞,再逐滴加入稀鹽酸至紅色消失,可得到一種膠體,該膠體的膠粒成分是________________(化學式)
(3)反應①的離子方程式為____________________________
(4)將B的稀溶液加水稀釋,在圖中畫出溶液的pH隨加水體積的變化趨勢曲線。__________

(5)將等物質的量的A和NaOH混合溶于水,該溶液中離子的物質的量濃度由大到小的順序為:________________________
(6)若反應②中鹽酸過量,向D溶液中滴加84消毒液,溶液的顏色發生了變化,該反應的離子方程式為________________________________________,小輝同學欲設計實驗,驗證D溶液中的陽離子尚未完全被氧化,請你將實驗過程補充完整:取反應液少許于試管中,滴加______________________,則證明D中的陽離子未完全被氧化。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA表示阿伏加德羅常數,下列敘述中不正確的是
A.標準狀況,11.2L氧氣所含的原子數為NA
B.1.8g的NH4+離子中含有的電子數為NA
C.常溫常壓下,48gO3和O2的混合氣體含有的氧原子數為3NA
D.2.4g金屬鎂變為鎂離子時失去的電子數為0.1NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分。表中所列的字母分別代表一種化學元素。
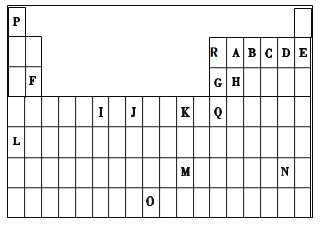
試回答下列問題:
(1)I的最高化合價為__________,J價電子排布圖__________。
(2)寫出基態時G元素原子中,電子占據的最高能層符號為__________,該能層具有的原子軌道數為____________ 。
(3)第一電離能介于R、B之間的第二周期元素有_____________種。
(4)下列關于元素在元素周期表中的位置以及元素原子的外圍電子排布特點的有關敘述不正確的是__________。
a.L位于元素周期表第五周期ⅠA族,屬于s區元素
b.O位于元素周期表第七周期Ⅷ族,屬于ds區元素
c.M的外圍電子排布式為6s1,屬于ds區元素
d.H所在族的外圍電子排布式為ns2np2,屬于p區元素
(5)配合物甲的焰色反應呈紫色,其內界由中心離子J3+與配位體AB-構成,配位數為6,甲的水溶液可用于實驗室J2+的定性檢驗,此方法檢驗J2+的離子方程式為_____________________。
(6)寫出Q元素的簡寫電子排布式___________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于SO2的說法中,不正確的是
A.SO2能使品紅溶液褪色,是因為SO2具有漂白性
B.SO2在空氣中極易被氧化為SO3
C.SO2通入Na2SO3或NaHCO3溶液中均能發生反應
D.SO2是形成酸雨的大氣污染物之一,主要來自于化石燃料的燃燒和工廠排放的廢氣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA為阿伏加德羅常數的數值,下列敘述錯誤的是( )
A. 18gH2O中含有的質子數為10NA
B. 1.0L1.0mo1·L-1的NaAlO2水溶液中含有的氧原子數為2NA
C. 46gNO2和N2O4混合氣體中含有原子總數為3NA
D. 1molNa與足量O2反應,生成Na2O和Na2O2的混合物,鈉失去NA個電子
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com