
| A. | 0.27 s | B. | 0.44 s | C. | 1.33 s | D. | 2 s |
分析 在N2+3H2?2NH3的反應中,經過一段時間后,NH3的濃度增加0.6mol/L,根據方程式知,氫氣濃度減少$\frac{3}{2}$×0.6mol/L=0.9mol/L,在此時間內用H2表示的平均反應速率為0.45mol/(L•s),則所經歷的時間=$\frac{△c}{v}$,據此分析解答.
解答 解:在N2+3H2?2NH3的反應中,經過一段時間后,NH3的濃度增加0.6mol/L,根據方程式知,氫氣濃度減少$\frac{3}{2}$×0.6mol/L=0.9mol/L,在此時間內用H2表示的平均反應速率為0.45mol/(L•s),則所經歷的時間=$\frac{△c}{v}$=$\frac{0.9mol/L}{0.45mol/(L.s)}$=2s,故選D.
點評 本題考查化學反應速率有關計算,側重考查學生分析計算能力,明確同一時間段內各物質濃度變化量與計量數關系是解本題關鍵,題目難度不大.


 狀元及第系列答案
狀元及第系列答案 同步奧數系列答案
同步奧數系列答案科目:高中化學 來源: 題型:解答題
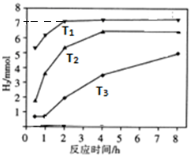 天然氣(主要成分甲烷)含有少量含硫化合物[硫化氫、羰基硫(COS)、乙硫醇(C2H5SH)],可以用氫氧化鈉溶液洗滌除去.
天然氣(主要成分甲烷)含有少量含硫化合物[硫化氫、羰基硫(COS)、乙硫醇(C2H5SH)],可以用氫氧化鈉溶液洗滌除去.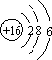 ;羰基硫分子的電子式為
;羰基硫分子的電子式為 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 得到2.54 g沉淀時,加入NaOH溶液的體積是700 mL | |
| B. | 該合金中銅與鎂的物質的量之比是2:1 | |
| C. | 該濃硝酸中HNO3的物質的量濃度是14.0 mol/L | |
| D. | NO2和N2O4的混合氣體中,NO2的體積分數是80% |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 元素編號 | 元素性質或原子結構 |
| A | 有三個電子層,K、M層電子數之和等于L層電子數 |
| B | 短周期中金屬性最強 |
| C | 常溫下單質為雙原子分子,氫化物的水溶液呈堿性 |
| D | 元素高正價是+7價 |
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2S2O3與硫酸反應的實驗中,實驗室沒有硫酸,臨時用硝酸進行實驗 | |
| B. | 滴定管洗凈后經蒸餾水潤洗,即可注入標準液進行滴定 | |
| C. | 制取氯氣時,用二氧化錳與濃鹽酸在加熱下反應,并用排水集氣法收集 | |
| D. | 配制FeCl3溶液時,將FeCl3溶解在較濃的鹽酸中,用水稀釋到所需濃度 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 四氯化碳分子的比例模型 | B. | 次氯酸的結構式為H-Cl-O | ||
| C. | CO2的電子式是: | D. | ${\;}_{8}^{18}$O2-離子結構示意圖: |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com