

分析 裝置A制備氯氣,裝置B吸收氯氣的中HCl,裝置C干燥氯氣,D裝置生成SCl2,E裝置收集SCl2,F裝置吸收多余的氯氣,吸收空氣中水蒸氣,防止進入E中.
(1)根據裝置的氣體的壓強差檢驗裝置的氣密性;加熱硫粉時,空氣中的氧氣能與硫粉反應;
(2)根據裝置圖可知裝置D中玻璃儀器的名稱為蒸餾燒瓶;將硫粉加熱使之融化,輕輕搖動使硫附著在容器的內壁,可以增大硫的表面積;
(3)二氯化硫(SCl2)的沸點低,易揮發,可以用冰水冷卻;防止空氣中水蒸氣進入;
(4)根據方程式判斷硫黃、液氯和液體三氧化硫的物質的量之比;
由SOCl2與氫氧化鈉溶液反應可知,SOCl2水解后分解得到SO2、HCl,利用品紅溶液檢驗有二氧化硫生成,用硝酸銀溶液檢驗氯離子.
解答 解:裝置A制備氯氣,裝置B吸收氯氣的中HCl,裝置C干燥氯氣,D裝置生成SCl2,E裝置收集SCl2,F裝置吸收多余的氯氣,吸收空氣中水蒸氣,防止進入E中.
(1)儀器組裝完成后,檢查裝置氣密性的操作是:(關閉分液漏斗活塞) 在干燥管末端連接一個排盡空氣的氣球,對A中燒瓶微熱,若氣球膨大,停止加熱,氣球恢復原狀,說明裝置氣密性良好;加熱硫粉時,空氣中的氧氣與硫粉反應,應先排盡系統中空氣,
故答案為:(關閉分液漏斗活塞) 在干燥管末端連接一個排盡空氣的氣球,對A中燒瓶微熱,若氣球膨大,停止加熱,氣球恢復原狀,說明裝置氣密性良好;防止加熱硫粉時,空氣中的氧氣與硫粉反應;
(2)根據裝置圖可知裝置D中玻璃儀器的名稱為蒸餾燒瓶,熱使之融化,輕輕搖動使硫附著在容器的內壁,形成一薄層膜,可以增大反應物接觸面積,使反應更加充分,
故答案為:蒸餾燒瓶;增大反應物接觸面積,使反應更加充分;
(3)二氯化硫(SCl2)的沸點低,為防止SCl2中液體揮發,可采取將錐形瓶放入冰水中冷卻等措施,裝置F(盛放堿石灰)有兩個作用:一是防止空氣中水蒸氣進入;二是吸收多余的氯氣,
故答案為:將錐形瓶放入冰水中冷卻;一是防止空氣中水蒸氣進入;二是吸收多余的氯氣;
(4)由S(s)+Cl2(g)$\frac{\underline{\;\;△\;\;}}{\;}$SCl2(l)、SCl2(l)+SO3(l)═SOCl2(l)+SO2(g)可知硫黃、液氯和液體三氧化硫的物質的量之比為1:1:1;
由SOCl2與氫氧化鈉溶液反應可知,SOCl2水解后分解得到SO2、HCl,利用品紅溶液檢驗有二氧化硫生成,用硝酸銀溶液檢驗氯離子,具體實驗操作為:分別取兩份水解后的溶液于試管中,向其中一支試管中加入品紅溶液,品紅褪色,說明有二氧化硫生成;向另一支試管中加入硝酸銀溶液,生成白色沉淀,說明有HCl生成,
故答案為:1:1:1;分別取兩份水解后的溶液于試管中,向其中一支試管中加入品紅溶液,品紅褪色,說明有二氧化硫生成;向另一支試管中加入硝酸銀溶液,生成白色沉淀,說明有HCl生成.
點評 本題考查化學實驗制備方案,涉及基本操作、對操作與裝置的分析評價、物質檢驗等,較好的考查學生對知識的遷移運用能力,難度中等.


科目:高中化學 來源: 題型:解答題
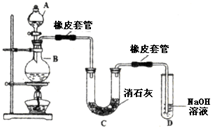 瑞典化學家舍勒在研究軟錳礦(主要成分是MnO2)的過程中,將它與濃鹽酸混合加熱,產生了一種黃綠色、刺激性氣味的氣體--氯氣.某學生使用這一原理設計如圖所示的實驗裝置,并且利用制得的氯氣與潮濕的消石灰反應制取少量漂白粉(這是一個放熱反應),據此回答下列問題:
瑞典化學家舍勒在研究軟錳礦(主要成分是MnO2)的過程中,將它與濃鹽酸混合加熱,產生了一種黃綠色、刺激性氣味的氣體--氯氣.某學生使用這一原理設計如圖所示的實驗裝置,并且利用制得的氯氣與潮濕的消石灰反應制取少量漂白粉(這是一個放熱反應),據此回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
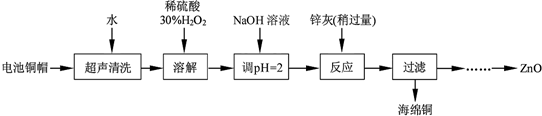
| 開始沉淀的pH | 完全沉淀的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 11.2g | B. | 5.6g | C. | 2.8g | D. | 無法計算 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Al3+、Na+、NO3-、Cl- | B. | K+、Na+、Cl-、NO3- | ||
| C. | K+、Na+、Cl-、AlO2- | D. | K+、NH4+、SO42-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在0.01mol•L-1Ba(OH)2溶液中:Na+、NH4+、NO3-、HCO3- | |
| B. | 使甲基橙變紅色的溶液中:Mg2+、Fe2+、NO-3、Cl- | |
| C. | 含有苯酚的溶液中:K+、Cl-、Br-、Fe3+ | |
| D. | 水電離的c(H+)=1×10-13mol•L-1的溶液中:K+、Na+、I-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
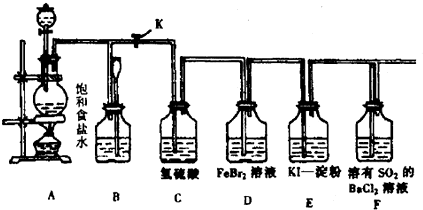
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com