
| 離子 | Ca2+ | Fe3+ |
| 完全沉淀時的pH | 13 | 3.7 |
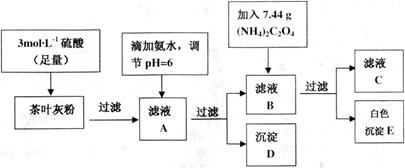
分析 (1)高溫灼燒物質通常在坩堝內進行,據此選擇;
(2)濾液A中含有鐵離子,鐵離子與氨水反應生成氫氧化鐵沉淀,注意一水合氨為弱電解質,需要保留分子式;
(3)若氫氧化鐵沉淀沒有洗滌干凈,氫氧化鐵中會混有鈣離子,可以使用碳酸鈉溶液檢驗;
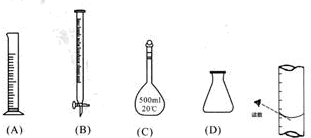
(4)①根據配制一定物質的量濃度的溶液方法及滴定操作方法選擇使用的儀器;
②根據滴定結束前溶液為為無色,滴定結束時高錳酸鉀溶液溶液過量進行解答;
③俯視液面導致滴定管中讀數偏小,讀出的高錳酸鉀溶液體積偏小,計算出的鈣離子消耗的草酸根離子物質的量偏大,測定結果偏高;
(5)根據檢驗鐵離子遇到硫氰根離子溶液顯示紅色進行解答;
(6)根據滴定消耗高錳酸鉀的物質的量計算出與鈣離子反應剩余的草酸根離子的物質的量,再根據醋酸銨的總的質量及樣品質量計算出鈣離子的質量分數,注意滴定體積與樣品體積的關系.
解答 解:(1)高溫灼燒物質通常在坩堝內進行,要用到酒精燈、坩堝、泥三角、三腳架等,故答案為:①③④⑤;
(2)濾液中含有鐵離子,鐵離子與氨水反應生成紅褐色的氫氧化鐵沉淀,反應的離子方程式為Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+,
故答案為:Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+;
(3)檢驗氫氧化鐵沉淀中是否洗滌干凈,可以通過檢驗氫氧化鐵中是否混有鈣離子進行判斷,方法為:向最后一次洗滌少許與試管中,滴加碳酸鈉溶液,若無沉淀產生,說明洗滌干凈,
故答案為:向最后一次洗滌少許與試管中,滴加碳酸鈉溶液,若無沉淀產生,說明洗凈;
(4)①將濾液C稀釋至500mL時需要使用到容量瓶,滴定操作中需要使用滴定管和錐形瓶,即B、C、D正確,
故答案為:B、C、D;
②滴定結束之前溶液為無色,滴定結束時高錳酸鉀溶液過量,溶液變為紫色,所以滴定終點顏色變化為:無色變為紫色或高錳酸鉀溶液不褪色,
故答案為:無色變為紫色或高錳酸鉀溶液不褪色;
③滴定到終點,靜置后,如圖3讀取KMnO4標準溶液的刻度數據,導致讀數偏小,計算出的消耗的高錳酸鉀溶液體積偏高,計算出的鈣離子消耗的草酸根離子物質的量偏高,則測定的鈣元素含量將偏高,
故答案為:偏高;
(5)濾液A中含有鐵離子,可以通過檢驗濾液A來驗證該品牌茶葉中是否含有鐵元素,方法為:取少量的濾液A,滴入硫氰化鉀溶液,溶液變成紅色,證明溶液中存在鐵離子,也證明離子茶葉中含有鐵元素,
故答案為:KSCN溶液,溶液呈紅色;
(6)7.44g草酸銨的物質的量為:$\frac{7.44g}{124g/mol}$=0.06mol,根據反應5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O可知與鈣離子反應的草酸根離子的物質的量為:0.06mol-$\frac{5}{2}$×(0.10mol•L-1×0.01L)×$\frac{500mL}{25mL}$=0.01mol,根據化學式CaC2O4可知鈣離子的物質的量為0.01mol,所以樣品中鈣離子的質量分數為:$\frac{40g/mol×0.01mol}{200g}$×100%=0.2%,
故答案為:0.2%.
點評 本題考查了探究茶葉中鐵元素、鈣元素的含量的方法及性質實驗方案的設計,題目難度較大,注意掌握性質實驗方案的設計方法,明確探究物質組成及含量的方法,試題培養了學生靈活應用所學知識解決實際問題的能力.


科目:高中化學 來源: 題型:選擇題
| A. | $\frac{64m}{n}$ | B. | $\frac{32m}{n}$ | C. | $\frac{n}{32m}$ | D. | $\frac{n}{64m}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 如圖是我校實驗室化學試劑濃硫酸標簽上的部分內容.現需要480mL 1mol•L-1的稀硫酸.用該濃硫酸和蒸餾水配制,可供選用的儀器有:①膠頭滴管;②玻璃棒;③燒杯;④量筒.
如圖是我校實驗室化學試劑濃硫酸標簽上的部分內容.現需要480mL 1mol•L-1的稀硫酸.用該濃硫酸和蒸餾水配制,可供選用的儀器有:①膠頭滴管;②玻璃棒;③燒杯;④量筒.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
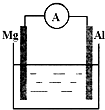 如圖所示裝置:
如圖所示裝置:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4個 | B. | 5個 | C. | 6個 | D. | 全部 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Mg2+ | B. | Na+ | C. | CO32- | D. | Ba2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 表示五氧化二磷分子是由磷元素與氧元素組成的 | |
| B. | 表示4個磷原子和10個氧原子 | |
| C. | 表示2個五氧化二磷分子,有4個磷原子和10個氧原子 | |
| D. | 表示2個五氧化二磷分子,每個五氧化二磷分子中含有2個磷原子和5個氧原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com