
【題目】科學家開發出了多種太陽能電池,除晶體硅太陽能電池外,還有GaAs太陽能電池、銅銦鎵硒薄膜太陽能電池等。
(1)基態Ga原子的電子排布式為___。
(2)高溫下CuO容易轉化為Cu2O,試從原子結構角度解釋原因___。
(3)與SeO3互為等電子體的兩種陰離子___(寫化學式)。
(4)AsF3是極性分子,理由是___。
(5)金剛砂(SiC)晶胞如圖所示:
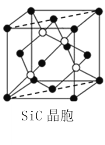
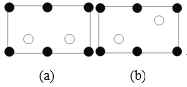
①金剛砂中硅原子的雜化軌道類型為___,沿晶胞圖中虛線方向的切面圖為___(填標號)。
②若晶胞參數為apm,阿伏加德羅常數為NA,則金剛砂的密度為___g·cm-3(列出表達式)。
【答案】[Ar]3d104s24p1 Cu2+的價電子排布為3d9,而Cu+為3d10的全充滿穩定結構 CO32-、NO3- 分子中正、負電荷中心不重合 sp3 a ![]()
【解析】
(1)Ga為31號元素,基態Ga原子核外有31個電子,基態Ga原子的電子排布式為:1s22s22p63s23p63d104s24p1或[Ar]3d104s24p1;
(2)Cu2+的價電子排布為3d9,而Cu+為3d10的全充滿穩定結構,所以在高溫下CuO能分解生成Cu2O;
(3)等電子體原子個數相同,價電子數相同,SeO3原子個數為4,價電子個數為24,與之互為等電子體的陰離子有CO32-、NO3-等;
(4)AsF3中新原子價層電子對數為3+![]() =4,含1對孤對電子,為三角錐形結構,分子中正負電荷重心不重合,屬于極性分子;
=4,含1對孤對電子,為三角錐形結構,分子中正負電荷重心不重合,屬于極性分子;
(5)①金剛砂中硅原子形成4個Si-C鍵,Si原子雜化軌道數目為4,Si原子采取sp3雜化。切面為長方形,面對角線上3個黑色球共線,面對角線為長方形的長,棱為長方形的寬,內部下方的2個白色球處于切面上,且到晶胞下底面虛線距離相等,圖中(a)符合;
②晶胞中白色球數目為4、黑球數目為![]() ,故晶胞中Si、C原子數目均為4個,晶胞質量m=
,故晶胞中Si、C原子數目均為4個,晶胞質量m=![]() ,晶胞體積V=a3pm3=(a×10-10)cm3,所以晶胞的密度為
,晶胞體積V=a3pm3=(a×10-10)cm3,所以晶胞的密度為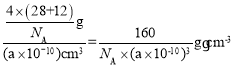 。
。


 新思維假期作業寒假吉林大學出版社系列答案
新思維假期作業寒假吉林大學出版社系列答案科目:高中化學 來源: 題型:
【題目】![]() 、CuCl是重要的化工原料,廣泛地用作有機合成催化劑.實驗室中以粗銅
、CuCl是重要的化工原料,廣泛地用作有機合成催化劑.實驗室中以粗銅![]() 含雜質
含雜質![]() 為原料,一種制備銅的氯化物的流程如下:
為原料,一種制備銅的氯化物的流程如下:

(1)上述流程中固體K溶于稀鹽酸的目的是 ______ ![]() 試劑X、固體J的物質分別為 ______ .
試劑X、固體J的物質分別為 ______ .
A.NaOH![]() B.CuO
B.CuO![]() C.
C.![]()
![]()
![]()
![]()
(2)反應②是向溶液2中通入一定量的![]() ,加熱一段時間后生成CuCl白色沉淀.寫出制備CuCl的離子方程式 ______ .
,加熱一段時間后生成CuCl白色沉淀.寫出制備CuCl的離子方程式 ______ .
(3)以石墨為電極,電解![]() 溶液時發現陰極上也會有部分CuCl析出,寫出此過程中陰極上的電極反應式 ______ .
溶液時發現陰極上也會有部分CuCl析出,寫出此過程中陰極上的電極反應式 ______ .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在恒溫條件下將一定量X和Y的混合氣體通入一容積為2L的密閉容器中,X和Y兩物質的濃度隨時間變化情況如圖。

(1)該反應的化學方程式為(反應物或生成物用符號X、Y表示):_________________________。
(2)a、b、c、d四個點中,表示化學反應處于平衡狀態的點是________________。
素材1:某溫度和壓強下,2L容器中,發生反應2SO2+O2![]() 2SO3,不同時間點測得密閉體系中三種物質的物質的量如下:
2SO3,不同時間點測得密閉體系中三種物質的物質的量如下:

素材2:反應在不同條件下進行時SO2的轉化率:(SO2的轉化率是反應的SO2占起始SO2的百分數,SO2的轉化率越大,化學反應的限度越大)

根據以上的兩個素材回答問題:
(3)根據素材1中計算20~30s期間,用二氧化硫表示的化學反應平均速率為________。
(4)根據素材2中分析得到,提高該化學反應限度的途徑有_______________。
(5)根據素材1、素材2中分析得到,要實現素材1中SO2的轉化率需控制的反應具體條件是__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有A、B、C三種金屬單質和甲、乙、丙三種氣體,及物質D、E、F、G、H,它們之間能發生如圖所示變化(圖中有些反應的產物和反應的條件沒有全部標出)。請回答下列問題:

(1)寫出指定物質的化學式:D____________、G____________、丙____________。
(2)上述反應中既是化合反應,又是氧化還原反應的是____________(填序號)。
(3)寫出反應①的離子方程式:____________________________________。
(4)寫出反應⑤的離子方程式________________________。用于檢驗溶液G中金屬陽離子的試劑是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】近年,一些藥物引起的不良反應引起了人們的關注。因此在開發新藥時如何減少毒副作用是一個很重要的課題。在下列結構簡式中,Ⅰ是撲熱息痛,Ⅱ是阿司匹林,它們都是臨床應用廣泛的解熱鎮痛藥,但Ⅰ易導致腎臟中毒,Ⅱ對胃黏膜有刺激性,多用會引起胃潰瘍。Ⅲ是撲炎痛,它是根據藥物合成中“拼合原理”的方法,設計并合成出的解熱鎮痛藥。這三種物質的結構簡式如下:

試回答:
(1)為什么阿司匹林會有上述的毒副作用?___________
(2)合成撲炎痛的反應屬于有機化學中的哪一類反應?_________
(3)撲炎痛本身并無解熱鎮痛的功效,但口服進入人體內后會產生上述藥理作用,且毒副作用沒有Ⅰ和Ⅱ那么明顯,試加以解_______________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】軟錳礦的主要成分是MnO2,還含有少量金屬鐵、鎂、鋁、鋅、銅的化合物等雜質。黃鐵礦的主要成分是FeS2,還含有硅、鋁的氧化物等雜質。工業上用軟錳礦制備碳酸錳并回收硫酸銨,其主要流程如下:
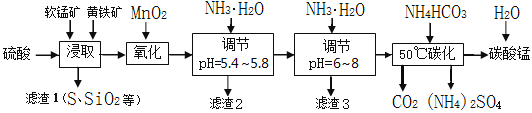
已知金屬離子從開始形成氫氧化物沉淀,到沉淀時溶液的pH如下表:
金屬離子 | Fe2+ | Fe3+ | Al3+ | Cu2+ | Mn2+ |
開始沉淀pH | 7.5 | 2.7 | 4.1 | 5.9 | 8.8 |
完全沉淀pH | 9.5 | 3.7 | 5.4 | 6.9 | 10.8 |
(1)提高浸出率的可采取的措施有_________。
A.適當升高溫度 B.攪拌 C.加適量純堿 D.加壓
(2)浸取完成后,取浸取液少許,加入KSCN溶液無明顯現象,則浸取時發生的主要反應的化學方程式是____________________________________________。
(3)調節pH為5.4~5.8的目的是_____________________________________________。
(4)濾渣3的主要成分的化學式是_____________。
(5)50℃碳化過程發生反應的離子方程式是____________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物M是制備一種抗菌藥的中間體,實驗室以芳香化合物A為原料制備M的一種合成路線如下:

已知:![]()

回答下列問題:
(1)B的結構簡式為_________;E中官能團的名稱為_________。
(2)1mol D與足量氫氧化鈉反應,最多可以消耗氫氧化鈉的物質的量為_______mol。
(3)下列有關說法正確的是____________。
A.用高錳酸鉀溶液可以鑒別B和C
B.D含有3個官能團
C.等物質的量的A和C完全燃燒的耗氧量一樣多
D.M可以發生的反應類型有:取代、加成、氧化、水解、酯化
(4)由F生成M的化學方程式為___________________________________。
(5)E有多種同分異構體,同時滿足下列條件的同分異構體有________種。
①屬于芳香族化合物,且分子中含有的環只有苯環
②能發生銀鏡反應和水解反應
(6)參照上述合成路線和信息,以乙烯和乙醛為原料![]() 無機試劑任選
無機試劑任選![]() ,設計制備聚
,設計制備聚![]() 丁烯的合成路線_______________。
丁烯的合成路線_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知a、b、c、d四種短周期主族元素,在周期表中相對位置如圖,下列說法正確的是
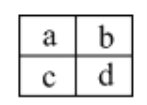
A. a、c兩元素的最高正價一定相等
B. 原子半徑大小順序為:c>d>b>a
C. a、b兩元素可能形成多種共價化合物
D. c、d二種元素氣態氫化物的穩定性比較:c > d
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】
教材插圖具有簡潔而又內涵豐富的特點。請回答以下問題:
(1)第三周期的某主族元素,其第一至第五電離能數據如圖1所示,則該元素對應的原子有_____種不同運動狀態的電子。
(2)如圖2所示,每條折線表示周期表ⅣA ~ⅦA 中的某一族元素氫化物的沸點變化。每個小黑點代表一種氫化物,其中a點代表的是___________。判斷依據是____________。
(3)CO2在高溫高壓下所形成的晶體其晶胞如圖3所示。則該晶體的類型屬于_____________晶體。
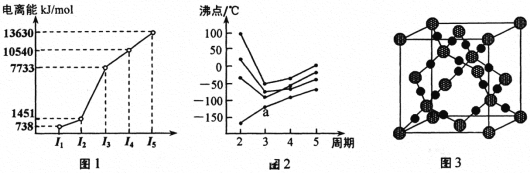
(4)第一電離能介于Al、P之間的第三周期元素有____種。 GaCl3中中心原子的雜化方式為_________,寫出與GaCl3結構相同的一種等電子體(寫離子)______________。
(5)冰、干冰、碘都是分子晶體,冰的結構具有特殊性,而干冰、碘的晶體具有相似的結構特征,干冰分子中一個分子周圍有__________個緊鄰分子。 D的醋酸鹽晶體局部結構如圖,該晶體中含有的化學鍵是_____________(填字母標號)。
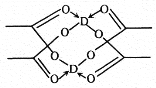
a.極性鍵 b.非極性鍵 c.配位鍵 d.金屬鍵
(6)Fe的一種晶體如甲、乙所示,若按甲虛線方向切乙得到的A~D圖中正確的是_____(填字母標號)。

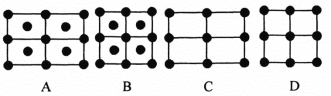
鐵原子的配位數是____________,假設鐵原子的半徑是r cm,該晶體的密度是ρg/cm3 ,則鐵的相對原子質量為________________(設阿伏加德羅常數的值為NA)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com