
【題目】關于電解NaCl水溶液,下列敘述正確的是 ( )
A. 電解時在陽極得到氯氣,在陰極得到金屬鈉
B. 若在陽極附近的溶液中滴入KI溶液,溶液呈棕色
C. 若在陰極附近的溶液中滴入酚酞試液,溶液呈無色
D. 電解一段時間后,將全部電解液轉移到燒杯中,充分攪拌后溶液呈中性
科目:高中化學 來源: 題型:
【題目】如下圖所示,把試管放入盛有25 ℃飽和Ca(OH)2溶液的燒杯中,試管開始放入幾小塊鎂片,再用滴管滴5 mL鹽酸于試管中。請回答下列問題:

(1)實驗中觀察到的現象是________________________________。
(2)產生上述現象的原因是________________________。
(3)寫出有關的離子方程式:_____________________________。
(4)由實驗推知,MgCl2溶液和H2的總能量________(填“大于”“小于”或“等于,下同”)鎂片和鹽酸的總能量,ΔH________0。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】近期發現,H2S是繼NO、CO之后的第三個生命體系氣體信號分子,它具有參與調節神經信號傳遞、舒張血管減輕高血壓的功能。回答下列問題:
(1)下列事實中,不能比較氫硫酸與亞硫酸的酸性強弱的是________(填標號)。
A.氫硫酸不能與碳酸氫鈉溶液反應,而亞硫酸可以
B.氫硫酸的導電能力低于相同濃度的亞硫酸
C.0.10 mol·L-1的氫硫酸和亞硫酸的pH分別為4.5和2.1
D.氫硫酸的還原性強于亞硫酸
(2)下圖是通過熱化學循環在較低溫度下由水或硫化氫分解制備氫氣的反應系統原理。

通過計算,可知系統(Ⅰ)和系統(Ⅱ)制氫的熱化學方程式分別為_______,制得等量H2所需能量較少的是________。
(3)H2S與CO2在高溫下發生反應:H2S(g)+CO2(g)![]() COS(g)+H2O(g)。在610 K時,將0.10 mol CO2與0.40 mol H2S充入2.5 L的空鋼瓶中,反應平衡后水的物質的量分數為0.02。
COS(g)+H2O(g)。在610 K時,將0.10 mol CO2與0.40 mol H2S充入2.5 L的空鋼瓶中,反應平衡后水的物質的量分數為0.02。
①H2S的平衡轉化率α1=________%,反應平衡常數K=________。
②在620 K重復實驗,平衡后水的物質的量分數為0.03,H2S的轉化率α2_______α1,該反應的ΔH________0。(填“>”“<”或“=”)
③向反應器中再分別充入下列氣體,能使H2S轉化率增大的是________(填標號)。
A.H2S B.CO2 C.COS D.N2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)溶質的質量分數為b%的KOH溶液,經加熱蒸發去ag水后,質量分數變成 2b%,體積為VmL,則此時溶液的物質的量濃度為___________。(答案必須為最簡形式)
(2)將6mol/L的鹽酸(ρ=1.19g/cm3)50mL稀釋成3mol/L的鹽酸(ρ=1.10g/cm3),需加水的體積為__________mL。
(3)密度為1.19g/cm3的鹽酸,質量分數為25%。該鹽酸用等體積的水稀釋后,所得溶液中溶質的質量分數_______(填“大于”、“小于”或“等于”)12.5%。
(4)已知20℃時,飽和NaCl溶液的密度為ρg/cm3,物質的量濃度為c mol/L,則飽和NaCl溶液的溶解度為_________g。(答案必須為最簡形式)
(5)相同質量的NO2和N2O4的質子數之比為_______,電子數之比為_______________。
(6)請用單線橋表示化學方程式CaH2+2H2O=Ca(OH)2+2H2↑電子轉移的方向和數目___________。
(7)若將過量的NaOH溶液加入NH4HCO3溶液中,則反應的化學方程式__________________,若將NaOH溶液加入過量的NH4HCO3溶液中,則反應的離子方程式為__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA代表阿伏加德羅常數,下列敘述正確的是
A. 0.1 mol丙烯酸中含有雙鍵的數目為0.1NA
B. 常溫常壓下,Cu-Zn原電池中,正極產生1.12 L H2時,轉移的電子數應為0.1NA
C. 一定條件下定容容器中充入3molH2(g)和1 mol N2(g)發生反應:H2(g)+ N2(g)![]() 2NH3(g);△H= -QkJ/mol,當該反應放出0.25QkJ的熱量時,容器中的氫分子數共有2.25 NA
2NH3(g);△H= -QkJ/mol,當該反應放出0.25QkJ的熱量時,容器中的氫分子數共有2.25 NA
D. 在50 g質量分數為46%的乙醇水溶液中,含有的氫原子總數為3NA
查看答案和解析>>
科目:高中化學 來源: 題型:
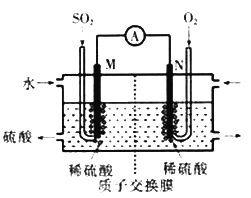
【題目】硫酸工業尾氣中的SOj是常見的大氣污染物,可通過以下幾種方式變廢為寶:
(1)電化學處理法:硫酸工業尾氣中的SO2經分離后,可用于制備硫酸,同時獲得電能,裝置如圖所示(電極均為惰性材料)寫出N極發生的電極反應式________________________;溶液中的陽離子向______極(M或N)移動,標準狀況下,當有22.4LSO2參加反應時,溶液中有________mol陽離子向該極移動。
(2)鈉堿循環法:用Na2SO3溶液作為吸收液來吸收SO2,尾氣通入1mol/L的Na2SO3溶液中,①當溶液的PH約為6時,Na2SO3溶液吸收SO2的能力顯著下降,此時溶液中c (SO32-)的濃度是0.2mol/L,則此時溶液中離子濃度由大到小的順序為_______________。
②當溶液的PH降至約為6時,需送至電解槽再生,再生示意圖如下:
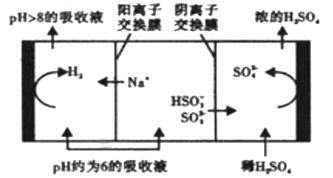
HSO3-在陽極放電的電極反應式是______________________________。
當陰極室中溶液pH升至8以上時,吸收液再生并循環利用。簡述再生原理:___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在2L恒容密閉容器中充入M (g)和N (g),發生反應M (g) +N (g) ![]() 2P (g) +Q (s),所得實驗數據如下表:
2P (g) +Q (s),所得實驗數據如下表:

下列說法正確的是
A. 實驗①中,若5 min時測得n(N) = 0.050 mol,則0~5min時間內平均反應速率v(P) = 0.015 mo1/(L·min)
B. 實驗②中達到平衡后,增大壓強,M的轉化率增大,平衡常數不變
C. 600℃時該反應的平衡常數K=3.0
D. 實驗③中,達到平衡時,x<0.10
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表各選項中,不能利用置換反應通過Y得到W的一組化合物是( )
選項 化合物 | A | B | C | D |
Y | H2O | FeCl3 | H2O | C |
W | HF | CuCl2 | Fe3O4 | Si |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com