
【題目】已知土壤膠體膠粒帶負電荷,又有很大的表面積,因而具有選擇吸附能力,在土壤里施用含氮量相同的下列肥料,肥效較差的是
A. (NH4)2SO4 B. NH4HCO3 C. NH4NO3 D. NH4Cl
科目:高中化學 來源: 題型:
【題目】某同學在實驗報告中有以下實驗數據:①用托盤天平稱取11.7 g食鹽;②用量筒量取5.26 mL鹽酸;③用廣泛pH試紙測得溶液的pH值是3.5,其中數據合理的是 ( )
A. ① B. ②③ C. ①③ D. ②
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏伽德羅常數的數值,下列說法正確的是( )
A.常溫常壓下,8 g O2含有4NA個電子
B.1 L 0.1 molL﹣1的氨水中有NA個NH4+
C.標準狀況下,22.4 L鹽酸含有NA個HCl分子
D.1 mol Na被完全氧化生成Na2O2 , 失去2NA個電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有關下列實驗各裝置圖的敘述,不正確的是( ) 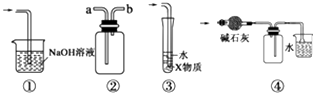
A.裝置①可用于吸收實驗中多余的Cl2
B.裝置②可用于收集H2、NH3、Cl2、HCl、NO2等
C.裝置③中X為苯,可用于吸收氨氣或氯化氫
D.裝置④中可用于收集氨氣,并吸收多余的氨氣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是
A. 可用過濾的方法將懸濁液中的分散質從分散劑中分離出來
B. 任何物質在水中都有一定的溶解度
C. 同一種溶質的飽和溶液要比不飽和溶液的濃度大
D. 布朗運動是膠體粒子特有的運動方式,只用肉眼就可以把膠體、溶液和濁液區別開
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A元素原子的L電子層比B元素原子的L電子層少3個電子,B元素原子核外總電子數比A 元素原子電子總數多5個,則A、B形成化合物可能是
A. 離子化合物ABB. 離子化合物B3A2
C. 離子化合物B2(AO3)3D. 離子化合物A2BO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用如圖1所示裝置可以完成一系列實驗(圖中夾持裝置已略去). 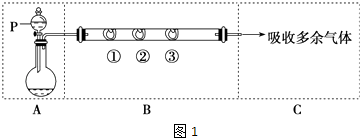
用裝置A由濃硫酸和濃鹽酸混合制取HCl氣體,裝置B中的三處棉花依次做了如下處理:①包有某固體物質,②蘸有KI溶液,③蘸有石蕊溶液.
請回答下列問題:
(1)儀器P的名稱是;
(2)①處包有的某固體物質可能是(填序號); a.MnO2 b.KMnO4 c.KCl d.Cu
反應開始后,觀察到②處有棕黃色物質產生,在實驗過程中,在③處能觀察到;
(3)甲同學為了驗證剩余氣體的主要成分,在C中設計了如圖2裝置,D中裝有銅絲網,裝置E的試管中不加任何試劑,裝置F的燒杯中加入適量的AgNO3溶液 ①實驗過程中,裝置D的作用是
②裝置F中的現象是;
③乙同學認為甲同學的實驗有缺陷,為了確保實驗的可靠性,乙同學提出在和(填裝置字母)之間加裝如圖3所示裝置.你認為如圖3廣口瓶中可加入足量(填字母代號),此試劑的作用是 . 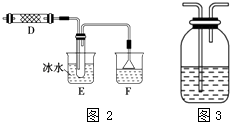
A.淀粉﹣碘化鉀溶液 B.四氯化碳溶液 C.濕潤的有色布條 D.飽和食鹽水.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一位同學為探究元素周期表中元素性質的遞變規律,設計了如下列實驗.
(1)根據題意解答 (i)將鈉、鉀、鎂、鋁各1mol分別投入到足量的同濃度的鹽酸中,試預測實驗結果:與鹽酸反應最劇烈,與鹽酸反應的速度最慢;與鹽酸反應產生的氣體最多.
(ii)向Na2S溶液中通入氯氣出現黃色渾濁,可證明Cl的非金屬性比S強,反應的離子方程式為 .
(2)利用如圖裝置可驗證同主族元素非金屬性的變化規律: 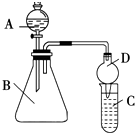
(i)儀器B的名稱為 , 干燥管D的作用為 .
(ii)若要證明非金屬性:Cl>I,則A中加濃鹽酸,B中加KMnO4(KMnO4與濃鹽酸常溫下反應生成氯氣),C中加淀粉碘化鉀混合溶液,觀察到C中溶液的現象,即可證明.從環境保護的觀點考慮,此裝置缺少尾氣處理裝置,可用溶液吸收尾氣.
(iii)若要證明非金屬性:C>Si,則在A中加鹽酸、B中加CaCO3、C中加Na2SiO3溶液,觀察到C中溶液的現象,即可證明.但有的同學認為鹽酸具有揮發性,可進入C中干擾實驗,應在兩裝置間添加裝有溶液的洗氣瓶除去.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某一化學反應中,其產物的總能量為80kJ,如果該反應是放熱反應,那么反應物的總能量可能是( )
A.100KJ
B.60KJ
C.50KJ
D.30KJ
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com