
【題目】
(1)常溫下,0.1mol/L 的CH3COOH溶液中有1%的CH3COOH分子發生電離,則溶液的pH=;可以使0.10 mol·L-1 CH3COOH的電離程度增大的是
a.加入少量0.10 mol·L-1的稀鹽酸
b.加熱CH3COOH溶液
c.加水稀釋至0.010 mol·L-1
d.加入少量冰醋酸
e.加入少量氯化鈉固體
f.加入少量0.10 mol·L-1的NaOH溶液
(2)將等質量的鋅投入等體積且pH均等于3的醋酸和鹽酸溶液中,經過充分反應后,發現只在一種溶液中有鋅粉剩余,則生成氫氣的體積:V(鹽酸)V(醋酸)(填“>”、“<”或“=”)。
(3)0.1mol/L的某酸H2A的pH=4,則H2A的電離方程式為。
(4)25℃時,將pH=9的NaOH溶液與pH=4的鹽酸溶液混合,若所得混合溶液的pH=6,則NaOH溶液與鹽酸溶液的體積比為。
【答案】
(1)3,bcf
(2)<
(3)H2A ![]() H++HA-
H++HA-
(4)9∶1
【解析】解:(1)根據c(H+)=c(HAc)×ɑ,則c(H+)=0.1×1%,pH=3;醋酸溶液中存在電離平衡CH3COOH ![]() CH3COO-+H+。a、加入鹽酸增大了溶液c(H+),對醋酸的電離起抑制作用,a錯誤;b、弱電解質的電離是吸熱反應,加熱,有利用向電離反應方向進行,b正確;c、加水稀釋,降低了濃度,根據勒夏特列原理,平衡向濃度增大的方向進行,即向電離反應進行,c正確;d、加入冰醋酸,電離程度降低,d錯誤;e、加入氯化鈉固體,對電離無影響,e錯誤;f、加入氫氧化鈉,消耗H+,促使平衡向電離方向進行,f正確。答案選bcf;
CH3COO-+H+。a、加入鹽酸增大了溶液c(H+),對醋酸的電離起抑制作用,a錯誤;b、弱電解質的電離是吸熱反應,加熱,有利用向電離反應方向進行,b正確;c、加水稀釋,降低了濃度,根據勒夏特列原理,平衡向濃度增大的方向進行,即向電離反應進行,c正確;d、加入冰醋酸,電離程度降低,d錯誤;e、加入氯化鈉固體,對電離無影響,e錯誤;f、加入氫氧化鈉,消耗H+,促使平衡向電離方向進行,f正確。答案選bcf;
(2)鹽酸是強酸,醋酸是弱酸,相同pH時,弱酸的濃度大于強酸,則鹽酸的物質的量小于醋酸,反應后只有一種溶液中有鋅剩余,此溶液是鹽酸,即產生氫氣的體積V(鹽酸) <V(醋酸);
(3)常溫下,0.1mol/L的某酸H2A的pH=4,說明該酸部分電離,則為弱酸,H2A是二元弱酸,分步電離,第一步電離方程式為:H2A ![]() H++HA-;
H++HA-;
(4)25℃時,將pH=9的NaOH溶液與pH=4的鹽酸溶液混合,若所得混合溶液的pH=6,則鹽酸過量,則有:c(H+)混= ![]() =
= ![]() =10-6,則NaOH溶液與鹽酸溶液的體積比為9∶1。
=10-6,則NaOH溶液與鹽酸溶液的體積比為9∶1。
【考點精析】利用弱電解質在水溶液中的電離平衡對題目進行判斷即可得到答案,需要熟知當弱電解質分子離解成離子的速率等于結合成分子的速率時,弱電解質的電離就處于電離平衡狀態;電離平衡是化學平衡的一種,同樣具有化學平衡的特征.條件改變時平衡移動的規律符合勒沙特列原理.


科目:高中化學 來源: 題型:
【題目】黨的十九大報告中提出加快生態文明體制改革,建設美麗中國,堅持人與自然和諧共生。下列有關觀念或做法不宜提倡的是
A. 青山綠水就是金山銀山 B. 創建環境友好型社會人人有責
C. 大力開發森林資源,發展鄉村旅游 D. 積極做好治沙工作,做到人進沙退
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵、銅的單質及它們的化合物與我們的生產、生活緊密相關。
(1)Cu處于周期表中______區,其最高能層的符號為______,基態銅原子的價電子排布式為________。
(2)向硫酸銅溶液中逐滴滴加氨水,首先形成藍色沉淀,繼續滴加氨水。沉淀溶解,得到深藍色透明溶液,向深藍色溶液中加入乙醇,析出深藍色晶體。
①寫出沉淀溶解,得到深藍色透明溶液的離子方程式:________。
②為什么加入乙醇,能夠析出深藍色晶體?________________
③為什么NH3常在配合物中作配體,而NH4+卻不能作配體?_______。
(3)Fe3+可以與SCN-、CN-、H2NCONH2(尿素)等多種配體形成很多的配合物。
①請寫出一種與SCN-互為等電子體的分子:________。
②CN-的電子式為________。
③H2NCONH2(尿素)中N、C原子的雜化方式分別為_______、_______,組成尿素的4種元素的第一電離能由大到小的順序為__________。
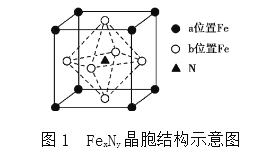
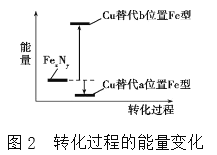
(4)某FeN,的晶胞如圖1所示,Cu可以完全替代該晶體中a位置Fe或者b位置Fe,形成Cu替代型產物Fe(x-n)CunNy。FexNy轉化為兩種Cu替代型產物的能量變化如圖2所示,其中更穩定的Cu替代型產物的化學式為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的數值。下列有關敘述正確的是( )
A. 7.8gNa2O2中陰離子所含的電子數為1.8NA
B. 標準狀況下,22.4LCCl4中所含C—C1鍵的數目為4NA
C. 在含Al3+總數為NA的AlCl3溶液中,Cl-總數為3NA
D. 在11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4反應中,6molCuSO4能氧化白磷的分子數為1.1NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據能量變化示意圖,下列熱化學方程式正確的是( )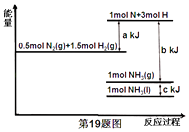
A.N2(g)+3H2(g)=2NH3(g)△H=﹣(b﹣a)kJmol﹣1
B.N2(g)+3H2(g)=2NH3(g)△H=﹣(a﹣b)kJmol﹣1
C.2NH3(l)=N2(g)+3H2(g)△H=2(a+b﹣c)kJmol﹣1
D.2NH3(l)=N2(g)+3H2(g)△H=2(b+c﹣a)kJmol﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈹銅是力學、化學綜合性能良好的合金,廣泛應用于制造高級彈性元件。以下是從某廢舊鈹銅元件(含BeO25%、CuS71%、少量FeS和SiO2)中回收鈹和銅兩種金屬的流程

已知:I.鈹、鋁元素處于周期表中的對角線位置,化學性質相似
Ⅱ.常溫下: Ksp[Cu(OH)2]=2.2×10-20 Ksp[Fe(OH)3]=4.0×10-38 K sp[Mn(OH)2]=2.1×10-13
(1)濾液A的主要成分除NaOH外,還有______________ (填化學式)
寫出反應I中含鈹化合物與過量鹽酸反應的離子方程式____________________________
(2)①溶液C中含NaCl、BeCl2和少量HCl,為提純BeCl2,選擇合理步驟并排序______________。
a加入過量的 NaOH b.通入過量的CO2 c加入過量的氨水
d.加入適量的HCl e.過濾 f洗滌
②從BeCl2溶液中得到BeCl2固體的操作是____________________________。
(3)①MnO2能將金屬硫化物中的硫元素氧化為單質硫,寫出反應Ⅱ中CuS發生反應的化學方程式________________________________________________________。
②若用濃HNO3溶解金屬硫化物,缺點是______________ (任寫一條)。
(4)溶液D中含c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.01mol·L-1,逐滴加入稀氨水調節pH可依次分離,首先沉淀的是______________ (填離子符號),為使銅離子開始沉淀,常溫下應調節溶液的pH值大于______________。
(5)取鈹銅元件1000g,最終獲得Be的質量為81g,則產率是______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用壓強傳感器探究生鐵在pH=2和pH=4醋酸溶液中發生腐蝕的裝置及得到的圖象如下:分析圖象,以下結論錯誤的是( )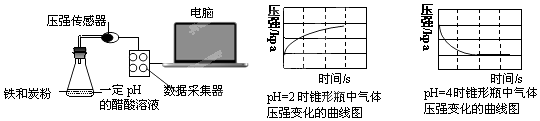
A.溶液pH≤2時,生鐵發生析氫腐蝕
B.生鐵的腐蝕中化學腐蝕比電化學腐蝕更普遍
C.在酸性溶液中生鐵可能發生吸氧腐蝕
D.兩溶液中負極反應均為:Fe﹣2e﹣═Fe2+
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com