
下列說法正確的是
A、氯堿工業是電解熔融的NaCl,陽極產生Cl2
B、氫氧燃料電池可將熱能直接轉變為電能
C、氫氧燃料電池工作時氫氣在負極被氧化
D、工業上電解熔融的AlCl3來制取鋁
科目:高中化學 來源:2016屆黑龍江省雙鴨山市高三上第一次月考化學試卷(解析版) 題型:選擇題
在水溶液中能大量共存的一組離子是
A.NH+、Na+、Cl-、SO42- B.K+、Mg2+、OH-、NO3-
C.H+、Ca 2+、SiO32-、NO3- D.K+、Al3+、ClO-、HCO3-
查看答案和解析>>
科目:高中化學 來源:2016屆湖南省高三上學期入學考試化學試卷(解析版) 題型:選擇題
給定條件下,下列選項中所示的物質間轉化均能一步實現的是
A.粗硅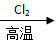 SiCl4
SiCl4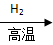 Si
Si
B.Mg(OH)2 MgCl2(aq)
MgCl2(aq) 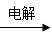 Mg
Mg
C.Fe2O3 FeCl3(aq)
FeCl3(aq) 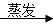 無水FeCl3
無水FeCl3
D.AgNO3(aq) 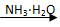 [Ag(NH3)2]OH(aq)
[Ag(NH3)2]OH(aq) 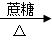 Ag
Ag
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧省高二上化學試卷(解析版) 題型:選擇題
將4 mol A和2 mol B放入2 L密閉容器中發生反應:2A(g)+B(g)  2C(g) ΔH<0。4 s后反應達到平衡狀態,此時測得C的濃度為0.6 mol/L。下列說法正確的是
2C(g) ΔH<0。4 s后反應達到平衡狀態,此時測得C的濃度為0.6 mol/L。下列說法正確的是
A.4 s內,v(B)=0.075 mol/(L·s)
B.當c(A)∶c(B)∶c(C)=2∶1∶2時,該反應即達到平衡狀態
C.達到平衡狀態后,若只升高溫度,則C的物質的量濃度增大
D.達到平衡狀態后,若溫度不變,縮小容器的體積,則A的轉化率降低
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江大慶鐵人中學高二上9月考化學試卷(解析版) 題型:填空題
(16分)甲醇(CH3OH)是一種重要的化工原料,也是一種比較理想的燃料。甲醇在各個領域有著廣泛的應用。
(1)實驗測得:32 g甲醇在氧氣中完全燃燒,生成二氧化碳氣體和液態水時釋放出726.4 kJ的熱量,試寫出甲醇燃燒的熱化學方程式:________________。
(2)燃料電池是一種連續地將燃料和氧化劑的化學能直接轉換成電能的化學電池。下圖是一個化學過程的示意圖。2CH3OH+3O2+4KOH K2CO3+6H2O
K2CO3+6H2O

①A(石墨)電極的名稱是 。
②通入O2的電極的電極反應式是 。
③寫出通入CH3OH的電極的電極反應式是 。
④乙池中反應的化學方程式為 。
⑤當電路中通過0.01mol電子時,丙池溶液的C(H+) = mol/L(忽略電解過程中溶液體積的變化)。
(3)合成甲醇的主要反應是:2H2(g)+ CO(g) CH3OH(g) △H=—90.8 kJ·mol—1。
CH3OH(g) △H=—90.8 kJ·mol—1。
①在恒溫恒容條件下,充入一定量的H2和CO,發生反應2H2(g)+ CO(g) CH3OH(g)。則該反應達到平衡狀態的標志有
CH3OH(g)。則該反應達到平衡狀態的標志有
a.混合氣體的密度保持不變
b.混合氣體的總壓強保持不變
c.CO的質量分數保持不變
d.甲醇的濃度保持不變
e.v正(H2)= v逆(CH3OH)
f.v(CO)= v(CH3OH)
②要提高反應2H2(g)+ CO(g) CH3OH(g)中CO的轉化率,可以采取的措施是:
CH3OH(g)中CO的轉化率,可以采取的措施是:
a.升溫
b.加入催化劑
c.增加CO的濃度
d.加入H2
e.加入惰性氣體
f.分離出甲醇
查看答案和解析>>
科目:高中化學 來源:2015-2016學年北大附中河南分校高二上9月考化學試卷(解析版) 題型:選擇題
下列說法正確的是
A.在101kPa時,1mol物質完全燃燒時所放出的熱量,叫做該物質的燃燒熱
B.酸和堿發生中和反應生成1mol水,這時的反應熱叫中和熱
C.燃燒熱或中和熱都是反應熱的種類之一
D.其他條件一樣時,氫氣與氧氣反應生成液態水和氣態水時所放出的熱量相等
查看答案和解析>>
科目:高中化學 來源:2016屆四川省高三上學期第一次月考化學試卷(解析版) 題型:填空題
(14分)丙烷在燃燒時能放出大量的熱,它也是液化石油氣的主要成分,作為能源應用于人們的日常生產和生活。
已知:①2C3H8(g)+7O2(g)=6CO(g)+8H2O (l)△H1=﹣2741.8kJ/mol
②2CO (g)+O2(g)=2CO2(g)△H2=﹣566kJ/mol
(1)反應C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) 的△H= 。
(2)現有1mol C3H8在不足量的氧氣里燃燒,生成1mol CO和2mol CO2以及氣態水,將所有的產物通入一個固定體積為1L的密閉容器中,在一定條件下發生如下可逆反應:CO(g)+H2O(g) CO2(g)+H2(g)△H=+41.2kJ/mol
CO2(g)+H2(g)△H=+41.2kJ/mol
①下列事實能說明該反應達到平衡的是 。
a.體系中的壓強不發生變化
b.V正(H2)=V 逆(CO)
c.混合氣體的平均相對分子質量不發生變化
d.CO2的濃度不再發生變化
②5min后體系達到平衡,經測定,H2為0.8mol,則v(H2O)= ;此時該反應的平衡常數K為 。
③向平衡體系中充入少量CO則平衡常數K (填“增大”、“減小”或“不變”)
依據(1)中的反應可以設計一種新型燃料電池,一極通入空氣,另一極通入丙烷氣體;燃料電池內部是熔融的摻雜著氧化釔(Y2O3)的氧化鋯(ZrO2)晶體,在其內部可以傳導O2﹣,電池內部O2﹣由 極移向 極(填“正”或“負”);電池的負極電極反應式為 。
(3)用上述燃料電池和惰性電極電解足量Mg(NO3)2和NaCl的混合溶液.電解開始后陰極區的現象為 。
查看答案和解析>>
科目:高中化學 來源:2016屆山東省高三上學期一模化學試卷(解析版) 題型:選擇題
下列關于金屬鈉的敘述錯誤的是
A.金屬鈉可以保存在煤油中
B.金屬鈉著火時,可用泡沫滅火器來滅火
C.鈉與熔融的四氯化鈦反應可制取鈦
D.實驗時用剩的鈉塊應該放回原試劑瓶
查看答案和解析>>
科目:高中化學 來源:2016屆安徽省等六校教研會高三第一次聯考化學試卷(解析版) 題型:填空題
氨氣是一種重要的化工產品,工業上可以按照下圖所示流程生產氨氣:
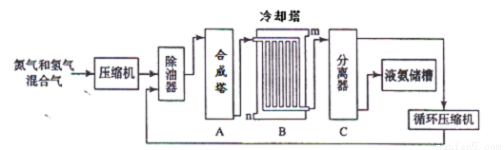
(1)原料氣之一氮氣的工業制取方法是 ,寫出氨氣的工業用途(任答一點) 。
(2)寫出合成塔中發生的反應的化學反應方程式 。在冷卻塔中對混合氣體進行冷卻,冷水的入口 (答m或n)。
(3)設備C的作用 。其分離器中的過程對整個工業合成氨的意義 (試結合平衡移動原理回答)。
(4)在原料氣制備過程中混有 CO對催化劑有毒害作用,欲除去原料氣中的 CO,可通過如下反應來實現:CO(g)+H2O(g) CO2 (g)+ H2 (g),已知1000K時該反應的平衡常數K=0.627,若要使CO的轉化超過80%,則起始物中c(H2O):c(CO)不低于 (精確到小數點后一位)。
CO2 (g)+ H2 (g),已知1000K時該反應的平衡常數K=0.627,若要使CO的轉化超過80%,則起始物中c(H2O):c(CO)不低于 (精確到小數點后一位)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com